臭氧对纯化水杀菌文档格式.docx
《臭氧对纯化水杀菌文档格式.docx》由会员分享,可在线阅读,更多相关《臭氧对纯化水杀菌文档格式.docx(22页珍藏版)》请在冰豆网上搜索。
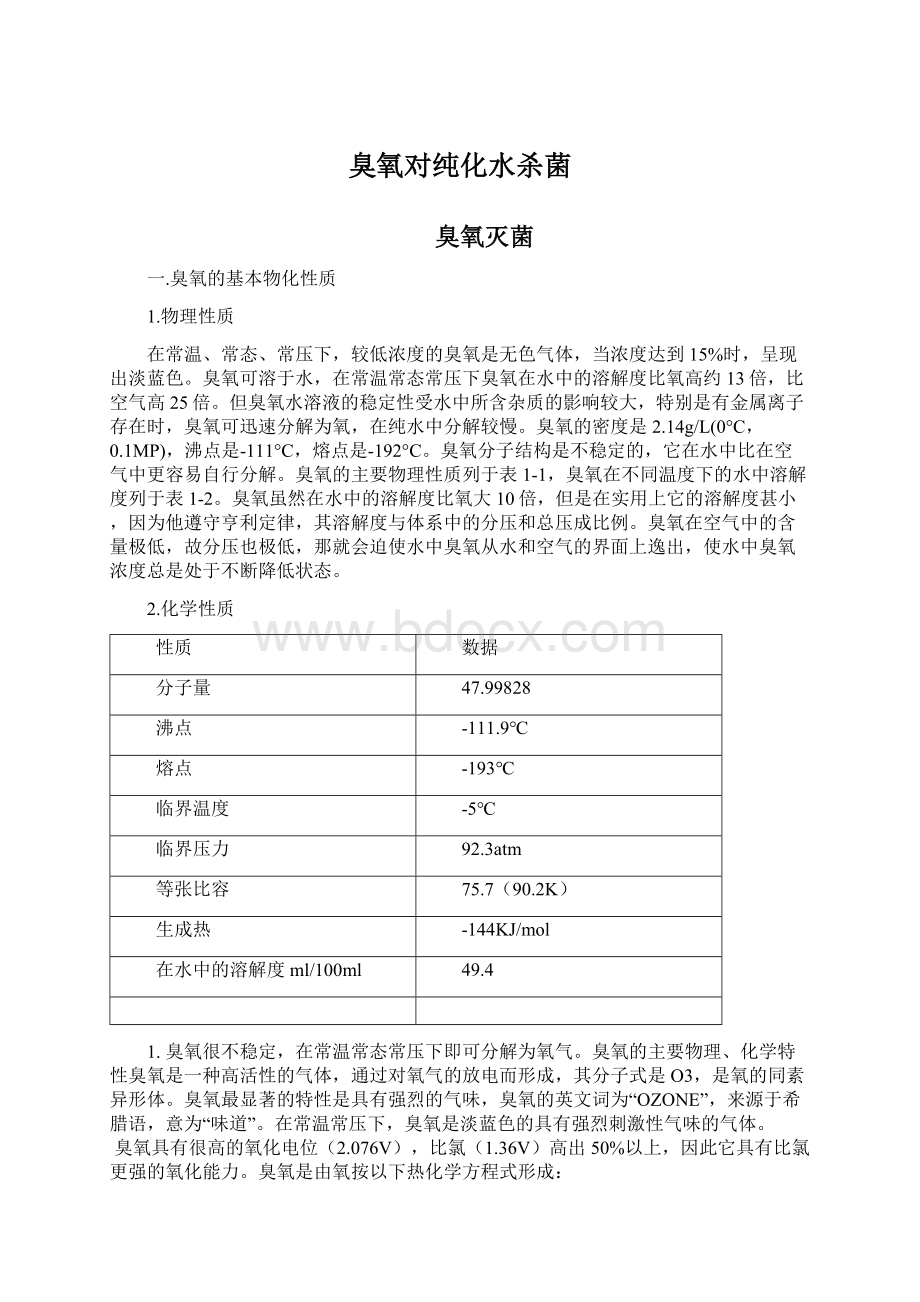
生成热
-144KJ/mol
在水中的溶解度ml/100ml
49.4
1.臭氧很不稳定,在常温常态常压下即可分解为氧气。
臭氧的主要物理、化学特性臭氧是一种高活性的气体,通过对氧气的放电而形成,其分子式是O3,是氧的同素异形体。
臭氧最显著的特性是具有强烈的气味,臭氧的英文词为“OZONE”,来源于希腊语,意为“味道”。
在常温常压下,臭氧是淡蓝色的具有强烈刺激性气味的气体。
臭氧具有很高的氧化电位(2.076V),比氯(1.36V)高出50%以上,因此它具有比氯更强的氧化能力。
臭氧是由氧按以下热化学方程式形成:
3O3→2O3-69kcal由上式可见臭氧的形成是吸热过程,因此,臭氧分子极不稳定,可自行分解,伴随着分解过程全放出能量因此,臭氧比氧具有更高的活性和氧化能力。
臭氧、氯和二氧化氢的氧化势(还原电位)分别是2.07.1.36.1.28伏特,可见臭氧在处理水中是氧化力量最强的一种。
臭氧的氧化作用导致不饱和的有机分子的破裂。
使臭氧分子结合在有机分子的双键上,生成臭氧化物。
臭氧化物的自发性分裂产生一个羧基化合物和带有酸性和碱性基的两性离子,后者是不稳定的,可分解成酸和醛。
其反应式为:
2O?
→3O?
+285kJ(1-2)
由于分解时放出大量热量,故当其含量在25%以上时,很容易爆炸。
但一般臭氧在空气中,臭氧的含量很难超过10%以上,在臭氧用于饮用水处理的较长过程中,还没有一例氧爆炸的事例。
含量为1%以下的臭氧,在常温常态常压的空气中分解半衰期为16h左右。
随着温度的升高,分解速度加快,温度超过100℃时,分解非常剧烈,达到270℃高温时,可立即转化为氧气。
臭氧在水中的分解速度比空气中快。
在含有杂质的水溶液中臭氧迅速回复到形成它的氧气。
如水中臭氧浓度为6.25×
10-5mol/L(3mg/l)时,其半衰期为5~30min,但在纯水中分解速度较慢,如在蒸馏水或自来水中的半衰期大约是20min(20℃),然而在二次蒸馏水中,经过85min后臭氧分解只有10%,若水温接近0℃时,臭氧会变得更加稳定。
2.臭氧的氧化能力
臭氧的氧化能力极强,其氧化还原电位仅次于F?
,在其应用中主要用这一特性。
3.臭氧的氧化反应
a、与无机物的氧化反应
臭氧与亚铁、Mn2+、硫化物、硫氰化物、氰化物、氯等均发生反应
如:
O3+SO2==SO3+O2O3+CO==CO2+O2O3+NO==NO2+O2O3+4NH3==NH4NO3+2NH4O?
4O3+PbS==PbSO4+4O2Ag+O3==AgO+O2
XeO3+4OH-+O3==XeO6(4-)+O2+2H2O3CN-+O3==3OCN22OCN2+O3==CO2+O2+N2
b、臭氧与有机物的反应
臭氧在水溶液中与有机物的反应极其复杂,
⑴臭氧与烯烃类化合物的反应臭氧容易与具有双链的烯烃化合物发生反应,反应的最终产物可能是单体的、聚合的、或交错的臭氧化物的混合体。
臭氧化物分解成醛和酸。
⑵臭氧和芳香族化合物的反应臭氧和芳香族化合物的反应较慢,在系列苯<
萘<
菲<
嵌二萘<
蒽中,其反应速度常数逐渐增大。
⑶对核蛋白(氨基酸)系、有机氨也都发生反应
臭氧在下列混合物的氧化顺序为
链烯烃>
胺>
酚>
多环芳香烃>
醇>
醛>
链烷烃
c、臭氧的毒性和腐蚀性
臭氧属于有害气体,浓度为6.25×
10mol/L(0.3mg/m3)时,对眼、鼻、喉有刺激的感觉;
浓度(6.25-62.5)×
10-5mol/L(3~30mg/m3)时,出现头疼及呼吸器官局部麻痹等症;
臭氧浓度为3.125×
10-4~1.25×
10-3mol/L(15~60mg/m3)时,则对人体有危害。
其毒性还和接触时间有关,例如长期接触1.748×
10-7mol/L(4ppm)以下的臭氧会引起永久性心脏障碍,但接触20ppm以下的臭氧不超过2h,对人体无永久性危害。
因此,臭氧浓度的允许值定为4.46×
10-9mol/L(0.1ppm)8h.由于臭氧的臭味很浓,浓度为4.46×
10-9mol/L(0.1ppm)时,人们就感觉到,因此,世界上使用臭氧已有一百多年的历史,至今也没有发现一例因臭氧中毒而导致死亡的报道。
臭氧具有很强的氧化性,除了金和铂外,臭氧化空气几乎对所有的金属都有腐蚀作用。
铝、锌、铅与臭氧接触会被强烈氧化,但含铬铁合金基本上不受臭氧腐蚀。
基于这一点,生产上常使用含25%Cr的铬铁合金(不锈钢)来制造臭氧发生设备和加注设备中与臭氧直接接触的部件。
臭氧对非金属材料也有了强烈的腐蚀作用,即使在别处使用得相当稳定得聚氯乙烯塑料滤板等,在臭氧加注设备中使用不久便见疏松、开裂和穿孔。
在臭氧发生设备和计量设备中,不能用普通橡胶作密封材料,必须采用耐腐蚀能力强的硅橡胶或耐酸橡胶等。
3.化学性质及功效
臭氧(O3)是氧气(O2)的同素异形体,它是一种具有特殊气味的淡蓝色气体。
分子结构呈三角形,键角为116°
,其密度是氧气的1.5倍,在水中的溶解度是氧气的10倍。
臭氧是一种强氧化剂,它在水中的氧化还原电位为2.07V,仅次于氟(2.5V),其氧化能力高于氯(1.36V)和二氧化氯(1.5V),能破坏分解细菌的细胞壁,很快地扩散透进细胞内,氧化分解细菌内部氧化葡萄糖所必须的葡萄糖氧化酶等,也可以直接与细菌、病毒发生作用,破坏细胞、核糖核酸(RNA),分解脱氧核糖核酸(DNA)、RNA、蛋白质、脂质类和多糖等大分子聚合物,使细菌的代谢和繁殖过程遭到破坏。
细菌被臭氧杀死是由细胞膜的断裂所致,这一过程被称为细胞消散,是由于细胞质在水中被粉碎引起的,在消散的条件下细胞不可能再生。
应当指出,与次氯酸类消毒剂不同,臭氧的杀菌能力不受PH值变化和氨的影响,其杀菌能力比氯大600-3000倍,它的灭菌、消毒作用几乎是瞬时发生的,在水中臭氧浓度0.3-2mg/L时,0.5-1min内就可以致死细菌。
达到相同灭菌效果(如使大肠杆菌杀灭率达99%)所需臭氧水药剂量仅是氯的0.0048%。
臭氧对酵母和寄生生物等也有活性,例如可以用它去除以下类型的微生物和病毒。
①病毒已经证明臭氧对病毒具有非常强的杀灭性,例如Poloi病毒在臭氧浓度为0.05-0.45mg/L时,2min就会失去活性。
②孢囊在臭氧浓度为0.3mg/L下作用2.4min就被完全除掉。
③孢子由于孢衣的保护,它比生长态菌的抗臭氧能力高出10-15倍。
④真菌白色念珠菌(candidaalbicans)和青霉属菌(penicillium)能被杀灭。
⑤寄生生物曼森氏血吸虫(schistosomamansoni)在3min后被杀灭。
此外,臭氧还可以氧化、分解水中的污染物,在水处理中对除嗅味、脱色、杀菌、去除酚、氰、铁、锰和降低COD、BOD等都具有显著的效果。
应当注意,虽然臭氧是强氧化剂,但其氧化能力是有选择性的,像乙醇这种易被氧化的物质却不容易和臭氧作用。
二.臭氧的氧化反应和消毒机理
臭氧一经溶解在水里,会出现下列两种反应:
一种是直接氧化,它是较缓慢的且有明显选择性的反应;
另一种则是在水中羟基、过氧化氢、有机物、腐殖质和高浓度的氢氧根诱发下自行分解成羟基自由基,间接地氧化有机物、微生物或氨等。
后一种反应相当快,且没有选择性,另外还能将重碳酸根氧化成重碳酸和碳酸。
这两种反应中后一种反应更强烈,氧化能力更强。
由于氢氧根和有机物等能诱发臭氧自行分解成羟基自由基,所以低ph条件下有利于臭氧直接氧化反应,而高ph值和有机物含量高的条件下则有利于羟基自由基的间接氧化反应。
臭氧的自行分解率在很大程度上取决于ph值、温度、UV值、臭氧浓度以及水中存在的其他可去除物。
其分解速率可由余臭氧的含量来间接表示。
由于重碳酸盐和碳酸盐(尤其是碳酸盐)具有较强的缓冲性能,因此在低PH和高缓冲性能的余臭氧可维持较长时间。
臭氧可杀菌消毒的作用主要与它的高氧化电位和容
易通过微生物细胞膜扩散有关。
臭氧能氧化微生物细胞的有机物或破坏有机体链状结构而导致细胞死亡。
因此,臭氧对顽强的微生物如病毒、芽孢等有强大的杀伤力。
此外,臭氧在杀伤微生物的同时,还能氧化水中的各种有机物,去除水中的色、嗅、味和酚等
三.操作控制点
臭氧的瞬时灭菌以广泛用于水的消毒,同时有除臭,水色以及铁锰。
臭氧会自行分解为氧气,臭氧灭菌不产生附加的化学物质污染是种较好的方法。
臭氧的用量及使用方法的正确与否,直接影响到使用效果。
在水生产的过程中臭氧的是用主要是灭菌,而各种菌类的耐臭氧能力差别很大,在一定臭氧浓度下,各种菌类被杀死的时间从1~10分钟达到灭菌程度,分布范围很宽。
某些细菌形成的孢子或芽孢杆菌或霉菌的芽孢都有很强的耐臭氧能力。
因此,在水的生产过程中就涉及如何使用臭氧的工艺技术问题。
一般条件下,合理的掌握下列4个操作,通常是可以正确的达到灭菌的目的的。
1.流量
指的是单位时间给出的臭氧量和单位时间给出的水的量。
这两个数值在操作中必须根据当地的效果把它确定下来,也就是说在操作的过程中每升的水需要用多少毫克的臭氧,臭氧水消毒的投加量一般为1mg/ml,接触的时间大于10分钟。
臭氧水使用环境空气中臭氧浓度不高于0.16mg/m3。
(臭氧水使用环境空气中臭氧浓度的测试方法:
在一103的房间内,使连续运行10分钟后,测试出水口上方25cm距离处环境空气中的臭氧浓度,不得超过0.16mg/m3。
)
2.界面
指臭氧与水接触的面积。
通常气体接触面积越大越好,行程越长越好。
在臭氧氧化塔里增加填充物,设有分配板或强制湍流隔板都是为了使用臭氧和水充分的接触。
接触反应是臭氧消毒系统生产运行的核心,它的作用是将由臭氧发生器发生的臭氧气体迅速有效的扩散到处理水中,并稳定可靠地完成预定工艺所要求的反应。
接触反应形式的确定主要依赖于工艺目标及其相应的反应。
臭氧接触是通过一定的方式使氧气扩散到液体中,并使之与液体全面接触和完成预期反应的过程.这一过程一般通过臭氧接触器来完成。
不同的工艺目标和相同的反应决定了接触器的形式和接触时间。
2.1臭氧接触器的主要形式有:
传统的微气泡扩散接触器、吸气式涡轮扩散接触器、带有接触填料的密闭式接触柱以及吸气式水射器扩散接触器。
对于净水消毒而言,采用的形式主要是微气泡扩散和吸气式涡轮扩散型。
臭氧接触时间对于不同的反应通常在1到12min之间。
在需要有可靠灭病毒的场合,通常需要维持剩余臭氧达0.4mg/L的4min接触时间,由于水中除细菌外通常还会含有与臭氧发生快速反应的物质(如构成水中色度和嗅味等物质)。
因此,消毒接触时间一般采用10min。
采用微起泡扩散消毒接触器时,通常布置成双格间和三格间接触室。
第一格间是为了水的化学需臭氧量(降低色和味)通常以0.4—1.0mg/L的用量和4---6min的接触时间为基础。
而后续格间的功能主要是杀灭病毒,在此格间的进口处剩余臭氧的水平至少必须有0.4mg/L,而且此格间的低部应注入足够的臭氧以保持这一水平达到4min的时间。
后续格间臭氧的注入量通常为0.4—0.6mg/L。
采用微气泡扩散方式时,为了保证臭氧向水中有较高的传输率,通常需要有至少5.5-6m的设计水深。
采用吸气式涡轮扩散接触器时,由于这种形式的接触器尤如一个完整的快速混合器,为了满足消毒所需要的时间和剩余臭氧的水平,通常需要设置停留池或采用多级布置方式。
由于涡轮机具有使臭氧气体与水高效混合的优点,因此,这种接触器的设计水深不需要很深。
2.2臭氧气体向水中的传递能力
臭氧气体向水中的传递能力也可表示为:
单位时间内的传递能力=传递系数×
交换面积×
交换电位这里所指的交换电位不仅与气液的浓度差有关,而且与臭氧和水中物质发生直接化学反应的活性有关。
许多实验表明,臭氧气体要溶解在水中,首先必须在与之接触的液体表面上完全扩散进而溶解在表面的液体中,最终扩散到液体的内部。
因此,气液两相间的传递率主要由下列因素所决定。
1.首先必须在与之接触的液体表面上完全扩散进而溶解在表面的液体中,最终扩散到液体的内部;
因此,气液两相间的传递率主要由下列因素所决定。
2.臭氧的氧化反应和消毒机理臭氧一经溶解在水里,会出现下列两种反应:
由于重碳酸盐和碳酸盐(尤其是碳酸盐)具有较强的缓冲性能,因此在低PH和高缓冲性能的余臭氧可维持较长时间。
臭氧可杀菌消毒的作用主要与它的高氧化电位和容易通过微生物细胞膜扩散有关。
此外,臭氧在杀伤微生物的同时,还能氧化水中的各种有机物,去除水中的色、嗅、味和酚等。
(1)气液两相的物理特性;
(2)气体通过气液界面的浓度差;
(3)气体湍流的程度。
2.2目前常用的三种接触装置
前节已提到接触装置的根本目的是保证臭氧在水中有尽量大的溶解度,为此,就需使臭氧气与水的接触面尽量大,有足够的接触时间,因而对接触装置的基本要求是:
1、能保证最优化的臭氧吸收效果。
2、接触装置工作时,工艺参数控制容易,工作稳定,安全性好。
3、能耗(搅拌或输送水、气所需动力)最低。
4、最小的体积下有最大的生产能力。
5、结构简单,用料便宜,制造与维修成本低。
一般常用的接触装置有三种:
鼓泡塔或池:
水射器(文丘里管)与固定螺旋混合器(单用或合用):
搅拌器或螺旋泵:
也有两种以上串联使用的,简介如下:
l、鼓泡法:
大型水处理用鼓泡池,小型水处理则常用鼓泡塔,它要求鼓泡器有小(几个微米到几十微米孔径)的孔径以增加臭氧的比表面积,而且要求孔径布气均匀,以使水、气全面接触,尤其是在鼓泡池中用多个布气器时,同时一般要求从水面到布气器表面,水深不小于4-5m,以利于气、水充分接触。
它的优点是:
操作方便,可以很容易改变运行参数而不影响投加效果和工作的稳定,动力消耗少,鼓泡塔结构简单,维修方便。
但其体积过于庞大,池式占地面积大,塔式要求较高厂房成本较高。
2、水射器(文丘里管)是利用高速水流在变径管道中流动造成的负压区吸入臭氧气,并形成湍流起到混合效果。
而在文丘里管后设置固定螺旋混合器则可进一步起搅拌水、气作用,在较长的距离内保持湍流状态以加强吸收。
这种装置由于混合时间很短,所以在其输出管道后常常还需加设贮水罐,以增加水、气接触时间,并使水流速降低以使尾气析出。
它的结构比鼓泡塔大大减小,生产成本低,但需加设水泵以保证水的喷射速度,而且工艺参数不易掌握,处理水量不能随意调节,否则将发生气、液两相分离,影响吸收效果。
3、搅拌法:
早期生产的搅拌器类似单缸洗衣机,只是电机上置、外筒做成多角型,利用搅拌造成的涡流使气泡打碎,溶入液体。
此类搅拌法效果差,动力消耗大,比鼓泡法体积小但成本并不低,由于有机械运动及臭氧腐蚀,所以机器寿命低,维修费用高。
近年有涡轮泵上市,混合效果很好,而且体积小巧,工r艺参数操作容易,但结构复杂成本高,动力消耗大,维修复杂,在它的管路后而也需设置贮水罐。
3.流速
指供给臭氧在单位时间的流速和进水,出水在单位时间内的流速。
它与流量是相关的,流速不能忽快忽慢。
进出水一般都以泵输送,水泵的功率的大小和联接管道的粗细都会影响流速,特别是供用水的不足而人为的造成流速的变化。
尤其是臭氧与水作用的氧化塔或容器中,流速的变化往往破坏了正常的操作,失去了应有的效应。
4.时效
时效是指保留的时间,即在一定臭氧浓度下与水作用的有效时间。
这里有两个控制点,臭氧浓度和与水作用时间。
不能满足满足臭氧与水接触保持一定的时间,等于没起到灭菌的作用,没有臭氧浓度的接触也是无效的。
4.1臭氧在水中的溶解
臭氧在水中的溶解一般遵循亨利定律。
(是英国的Henry(亨利)在1803年研究气体在液体中的溶解度规律时发现的,可表述为:
“在等温等压下,某种气体在溶液中的溶解度与液面上该气体的平衡压力成正比。
”)对臭氧在水中的溶解度的主要影响因素是温度和供气压力。
由于臭氧采用在使用现场利用空气或氧气就地制备,制备出来的臭氧气体实际上是一种臭氧化气体,属于混合气体,其中含有大量的空气和氧气。
而亨利定律表示的是某一单纯气体在水中的溶解规律,所以,臭氧在水中的溶解特性除了与上述的温度和供气压力有关外,还与供气中含臭氧的浓度有关。
此外,在一定的大气压力下,臭氧在水中的浓度与供气中的臭氧浓度有关。
虽然臭氧在水中的溶解度大于氧,但溶于水中的臭氧极不稳定,很容易分解臭氧在水中可自然分解,在20℃时,在pH7.6时,臭氧在水中的半衰期为21~22分钟。
目前,多数饮料厂都在用0.3~0.5mg/L的臭氧,这个数值只能作为参考值。
4.2水溶臭氧浓度与保持时间
军事医学科学院军队卫生研究所马义伦教授等经过对炭疽杆菌,枯草杆菌黑色变种进行臭氧处理试验,总结出杀菌动力学经验公式:
dN/dt=-KNtMCN
其中:
N:
菌数t:
时间C:
水中臭氧浓度m、n是t与c的指数K:
效率常数,也可表示细菌抗力。
由以上公式可以看出单位时间的灭菌量是与水中臭氧浓度及处理时间的若十次疗成止比,可见K与N在不变动的情况下要达到杀菌的目的,必须保证臭氧在水中浓度与一定的接触时间。
4.2.1保证水中臭氧浓度的必要性
要保证臭氧在水中的浓度需要很多条件,大致有水温、气压、气液的相对运动速度、臭氧气作用在液体表面的分压、臭氧气的表面积、水的粘度、密度、表面张力等,其中有些因素,如水温、气压、臭氧气作用在液体表面的分压至关重要。
也有的,如水的密度、粘滞度、表面张力等,在某一具体条件下是不变的,就可以不予考虑,现将其中关系简单介绍如下:
气液两相间的传质强度取决于分子与湍流的扩散速度,可以用一般传质公式表示:
u=dG/dt=KF·
△C
u:
传质速度,可用在t时间内从气相传入液相的臭氧量G确定,即dG/dt。
K:
传质系数,F:
气相与液相的接触表面积,△C传质过程中的动力,可用臭氧在实际情况下与平衡时的浓度差决定(即水中臭氧浓度与臭氧源中臭氧浓度差别越大,传质速度越大)。
分析一般传质方程式可以知道,首先要使臭氧尽多地溶入水中,就要尽量加大臭氧与水的接触表面积F,而这是接触装置决定的。
其次,△C说明臭氧发生器的浓度越高,越有利于水对臭氧的吸收·
4.2.2传质系数K
传质系数K则与多种因素有关,K(总传质系数)为气相传质系数K气与液相传质系数K液之和,而臭氧属于低溶解度气体,K气可忽略不计.而根据亨利一道尔顿定律,K液是多种物理参数的复合函数。
K液=f(T,P,u,w,p,ó
其中臭氧溶解量与气体压力P成正比而与水温T成反比。
随着两相相对线速度的增大,气液两相接触表面积F及其更新速度也增大,但每个气泡与液体接触的时间会减小,因此从综合效果来看,气体-液体的相对线速度应维持在一个范围内较好.
液体的粘滞度u,密度p及气液间介面表面张力。
的提高可使相间表面更新速度降低,并相应使K液减小,所以Km与u,p,o成反比,对于各种饮用水,此项可忽略不计。
在应用中,我们应关注温度、气压两个参数,而在设计接触装置时则应注意到水流、气流的相对速度,尤其是其中的温度,因为温度高了不但使水对臭氧的吸收效果下降,而且臭氧本身会因温度过高而分解。
国内就曾发生过试图用臭氧处理70·
℃的水温而没有取得任何效果的例证。
1894年梅尔费特(Mailfert)根据前人的实验报告求出以下臭氧在水中的浓度:
温度(摄氏度)
11.8
15
19
27
40
55
60
溶解度(L气/L水)
0.64
0.5
0.456
0.381
0.27
0.112
0.031
这组数据大致里线性,而且表明臭氧在水中的溶解度大约是氧的10-15倍。
威诺萨(venosa)与奥帕特金(Opatken)指出,决定臭氧(或任何气体)在某液体中的溶解度的基本关系式是亨利定律.即在一定温度下,任何气体溶解于已知体积的液体中的重量,将与该气体作用在液体上的分压成正比。
而且此定律可推导出结论:
在标准温度与压力下,臭氧是氧溶解度的13倍。
从亨利定律可以得出结论:
要提高臭氧在水中的溶解度,必须提高臭氧气在整个气源中分压,即提高臭氧源的浓度,如果臭氧源的浓度不够,处理时间再长,水中臭氧浓度也提不高(因已达到浓度平衡)。
4.3从以上论述,可以得到结论:
1、为保证杀菌效果,必须保证水中臭氧的一定浓度与处理时间。
2、为保证水中臭氧的一定浓度就需保证:
a.臭氧源的浓度。
b.一定的气温。
c.水温不能过高。
d.投入水中臭氧气的比表面积尽量大,使臭氧与水的接触机会更多。
根据国内外应用经验一般水质的饮用水消毒处理参数推荐为:
水溶臭氧浓度O.4mg/L,接触时间为4分钟,即CT值为1.6。
臭氧投加量1-2mg/L,水温最好在25摄氏度以下。
前苏联标准规定饮用水中臭氧浓度不低于O.3mg/L。
我国瓶装水行业推荐灌装时瓶内水臭氧浓度0.3mg/L.
四.臭氧发生器的性能试验条件和技术要求
1臭氧发生器的性能试验条件
试验条件为:
温度20~25℃,相对湿度60~70%。
2臭氧发生器的技术要求
2.1稳定性检测:
臭氧发生器工作过程中间,产量不小于标称值的90%。
2.2臭氧发生器的寿命:
臭氧发生器正常使用累计时间不小于1000小时。
2.3臭氧发生器臭氧发生单元发生每公斤臭氧耗电量如下:
工业用可收集式臭氧发生器:
电耗(kW.h/kg(O3)≤22(发生腔)
其它臭氧发生器:
电耗(kW.h/kg(O3)≤30(发生腔)
3臭氧发生器产生的臭氧浓度和产量、臭氧发生器的电耗和寿命测量方法。
3.1臭氧发生器产生的臭氧浓度