人教版九年级第二学期第一次检测化学试题A卷Word格式.docx
《人教版九年级第二学期第一次检测化学试题A卷Word格式.docx》由会员分享,可在线阅读,更多相关《人教版九年级第二学期第一次检测化学试题A卷Word格式.docx(12页珍藏版)》请在冰豆网上搜索。
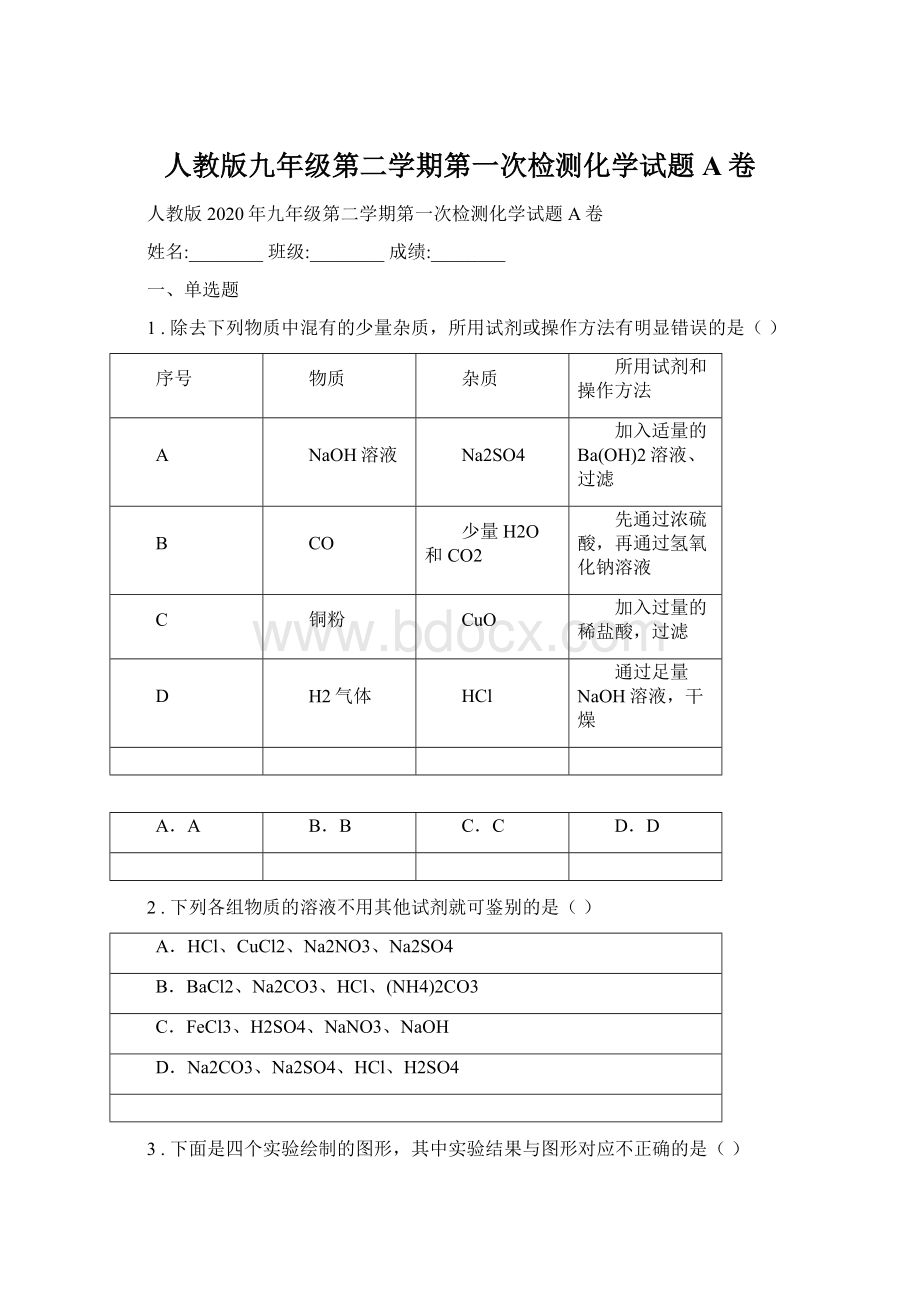
加入过量的稀盐酸,过滤
D
H2气体
HCl
通过足量NaOH溶液,干燥
A.A
B.B
C.C
D.D
2.下列各组物质的溶液不用其他试剂就可鉴别的是()
A.HCl、CuCl2、Na2NO3、Na2SO4
B.BaCl2、Na2CO3、HCl、(NH4)2CO3
C.FeCl3、H2SO4、NaNO3、NaOH
D.Na2CO3、Na2SO4、HCl、H2SO4
3.下面是四个实验绘制的图形,其中实验结果与图形对应不正确的是()
A.
等质量的镁粉和锌粉与足量的溶质质量分数相同的稀硫酸反应
B.
向含有稀盐酸和硫酸铜的溶液中滴加NaOH溶液
C.
敞口放置的浓硫酸
D.
向稀盐酸中不断滴加烧碱溶液至过量
4.区分下列各组物质,两种操作方法均不正确的是()
5.有X、Y、Z三种金属,如果把Z和Y分别放入稀盐酸中,Z溶解并产生氢气,Y不反应;
如果把X和Y分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而X没有变化,根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为
A.X、Y、Z
B.Z、Y、X
C.Y、X、Z
D.X、Z、Y
6.甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是
A.t1℃时,甲、乙的溶解度相等
B.t1℃时,甲、乙两物质形成的溶液溶质质量分数相等
C.t2℃时,在l00g水中放入100g甲,所得溶液的溶质质量分数为50%
D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,乙先达到饱和
7.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用。
常利用NaOH溶液来“捕捉”CO2,过程如下图所示(部分条件及物质未标出)。
下列说法正确的是()
A.该方法的优点是没有能耗
B.“反应、分离”中,分离物质的基本操作是蒸发、结晶
C.整个过程中,只有一种物质可以循环利用
D.该方法可减少碳排放
8.下列物质能在pH=1的无色溶液中大量共存的是
A.NaNO3、NaCl、KNO3、(NH4)2SO4
B.KOH、BaCl2、KCl、NaNO3
C.KCl、Na2SO4、Fe2(SO4)3、NaNO3
D.K2CO3、K2SO4、CaCl2、NaNO3
9.除去下列各组物质中的杂质,所用试剂和方法均正确的是
除杂质所用试剂和方法
O2
HCl气体
先通过NaOH溶液,再通过浓硫酸
Ca(OH)2溶液
先通过过量的Na2CO3溶液,再过滤
NaCl
Na2CO3
加入澄清石灰水,过滤
CaCO3
加入适量的盐酸,蒸发
10.“检测土壤浸出液的酸碱性”实验操作示意图如下,其中不正确的是()
土壤加水搅拌
过滤
检验酸碱性
测定pH
11.如图所示,向试管里的水中加入某物质后,U型管中原来相平的红墨水出现如图所示的情况,则加入的物质可能是()
A.氢氧化钠
B.生石灰
C.浓硫酸
D.硝酸铵
12.向AgNO3和Cu(NO3)2的混合溶液中加入一定量锌粉,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生。
则滤液中的溶质是()
A.Cu(NO3)2
B.Zn(NO3)2和AgNO3
C.Zn(NO3)2
D.AgNO3、Cu(NO3)2和Zn(NO3)2
13.下列实验现象描述错误的是()
A.将一氧化碳通入灼热的氧化铁,红棕色粉末逐渐变为黑色粉末
B.将氢氧化钠溶液加入硫酸铜溶液中,有红褐色沉淀产生
C.铁丝在氧气中燃烧时,火星四射,生成黑色固体
D.铁丝插入硫酸铜溶液中,银白色固体表面产生紫红色固体,溶液由蓝色逐渐变为浅绿色
14.氢氧化铝是一种不溶于水的白色固体,能与稀盐酸反应,也能与氢氧化钠溶液反应.氢氧化铝与氢氧化钠溶液反应的化学方程式为:
Al(OH)3+NaOH═NaAlO2+2H2O.下列有关说法错误的是()
A.氢氧化铝属于氧化物
B.在NaAlO2中铝元素的化合价为+3价
C.向稀盐酸中加入氢氧化铝,发生复分解反应
D.向氯化铝溶液中逐滴加入氢氧化钠溶液,先产生白色沉淀,后来白色沉淀又消失
15.电解饱和氯化钾溶液的化学方程式:
下列说法中不正确的是()
可用于自来水生产中杀菌消毒
B.农业上常用
改良酸性土壤
B.反应中有2中元素化合价发生改变
D.
可由海水蒸发结晶、精制获得
16.下列物质中,均是由原子构成的是
A.纳米铜、氦气
B.氢气、氯化钠
C.二氧化碳、铁
D.硫酸铜、水
17.以下实验操作中出现的现象叙述正确的是()
A.打开浓硫酸的试剂瓶塞,在瓶口出现白雾
B.铁丝在空气中燃烧火星四射
C.将50℃的饱和石灰水降温至20℃,溶液变浑浊
D.碳酸钠放入滴有酚酞的水中,溶液变红
18.下列能反映相关实验过程中量的变化的图象是()
A.煅烧石灰石
B.在变质的NaOH溶液中滴加稀盐酸
C.稀释NaC1溶液
D.稀H2SO4滴入BaC12溶液中
二、填空题
19.化学与我们的生活息息相关。
请从:
A.二氧化硫
B.二氧化碳
C.氢氧化钠
D.氢氧化铝
E.水
F.酒精
G.石油 H.煤八种物质中选择适当的字母序号填空:
①治疗胃酸过多的药剂是_____
②被誉为“工业的血液”的是_____
③能产生酸雨的气体是_____
20.请同学们搭乘“化学地铁”一起畅游物质世界吧!
如下图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。
“2~5号站”各站的对应物质属于不同类别的纯净物。
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变__________色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠的化学方程式为____________________________。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为___(填一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为____________(写一个)。
③“稀盐酸”列车途经“1、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质必须更换为__________(写一种物质),“稀盐酸”列车方能走完。
21.下列反应中属于化合反应的是_____,属于氧化反应的____,既是化合反应又是氧化反应的是_____。
A铜+氧气
氧化铜
B氨气+氧气
一氧化氮+水
C氢气+氧气
水
D甲烷+氧气
二氧化碳+水
E氨气+氯化氢
氯化铵
F一氧化碳+氧气
二氧化碳
三、简答题
22.对于氢氧化钙进行如下实验(状态②有剩余固体,状态③上层为红色溶液,状态④为无色澄清溶液):
(1)能说明氢氧化钙的性质是微溶于水的实验现象是________(用序号回答)。
(2)对状态④实验现象的原因解释是__________。
四、流程题
23.碳酸亚铁(FeCO3)是生产补血剂的原料.以下是某同学设计的利用铁矿烧渣(主要成分是Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和__.
(2)滤液Ⅰ中含有的金属阳离子:
Fe2+、__
(填离子符号).
(3)滤液Ⅰ中加入铁粉后可能发生的化学反应方程式:
①__;
②Fe+H2SO4=FeSO4+H2↑.
(4)“调节滤液Ⅱ的pH”的操作用__测定加入氨水后溶液的pH.
(5)加入碳酸铵得到碳酸亚铁的反应化学方程式:
__.
五、科学探究题
24.CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?
某化学兴趣小组的同学们对此进行了探究。
(查阅资料)①通常情况下,1体积水溶解1体积的CO2。
②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生。
(实验探究)小红同学设计了下图所示的实验装置(锥形瓶内充满CO2),并进行实验。
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面______(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,理由是___________。
请根据初中化学知识写出CO2与NaOH溶液反应的化学方程式:
____________。
(反思与评价1)小明认为小红的实验方案不严密,理由是_______________________。
(拓展实验)兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究。
请填写表中的空格。
实验方法
操作过程
现象
实验结论
方法一
取小红实验后锥形瓶内的溶液适量,加入足量CaCl2溶液
有白色沉淀生成
CO2与NaOH发生了反应
方法二
取小红实验后锥形瓶内的溶液适量,加入足量稀硫酸
______________
(反思与评价2)同学们经过讨论,认为(拓展实验)的______(填“方法一”或“方法二”)依然不严密,理由是___________________________(用化学方程式表示)。
六、计算题
25.实验室有一瓶失去标签的NaOH溶液。
为测定溶液中NaOH的质量分数,取m2gNaOH溶液于量热器中,加入m1g质量分数为10.0%的盐酸,进行若干次实验(实验中始终保持m1+m2=50g),测量并记录每次实验溶液均匀混合后的最高温度,实验结果如图所示。
(1)图中____点表示盐酸与NaOH溶液恰好完全反应(填标号)。
(2)计算溶液中NaOH的质量分数(结果精确到0.1%)。
____
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
16、
17、
18、