届高考化学二轮复习7+5小卷练五作业全国通用Word文件下载.docx
《届高考化学二轮复习7+5小卷练五作业全国通用Word文件下载.docx》由会员分享,可在线阅读,更多相关《届高考化学二轮复习7+5小卷练五作业全国通用Word文件下载.docx(14页珍藏版)》请在冰豆网上搜索。
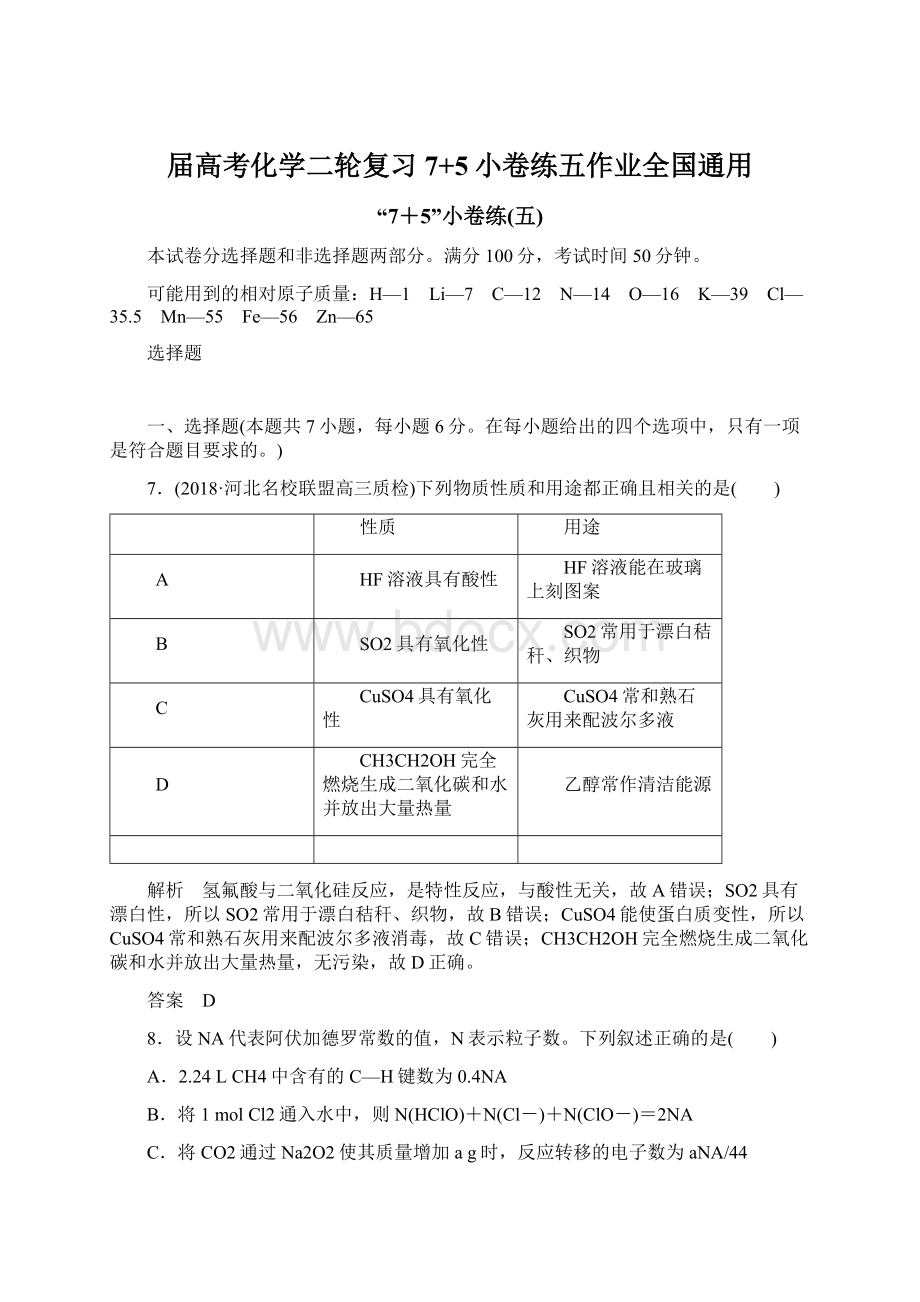
答案 D
8.设NA代表阿伏加德罗常数的值,N表示粒子数。
下列叙述正确的是( )
A.2.24LCH4中含有的C—H键数为0.4NA
B.将1molCl2通入水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA
C.将CO2通过Na2O2使其质量增加ag时,反应转移的电子数为aNA/44
D.3.0g含甲醛(HCHO)的冰醋酸中含有的原子总数为0.4NA
解析 甲醛(HCHO)、冰醋酸(CH3COOH)的最简式相同,均为CH2O,因此3.0g含甲醛的冰醋酸中所含原子总数为×
4×
NA=0.4NA(或设HCHO的质量为ag,则3.0g含甲醛的冰醋酸中所含原子总数为×
NA+×
8×
NA=0.4NA),D项正确。
没有指明温度、压强,2.24LCH4的物质的量无法确定,因此其所含C—H键的数目无法确定,A项错误;
将1molCl2通入水中,发生反应:
Cl2+H2O
HCl+HClO,该反应为可逆反应,根据物料守恒知,N(HClO)+N(Cl-)+N(ClO-)<
2NA,B项错误;
根据反应2Na2O2+2CO2===2Na2CO3+O2知,转移2mol电子时,Na2O2质量增加56g,则当Na2O2质量增加ag时,反应转移的电子数为×
a×
NA=,C项错误。
9.(2018·
济南一中高三月考)下列有关有机物的说法正确的是( )
A.蛋白质溶液中加Na2SO4可使其变性
B.乙烷、苯、葡萄糖溶液均不能使酸性KMnO4溶液褪色
C.有机物CH2===CHCH(CH3)Cl能发生加成反应、取代反应、缩聚反应、氧化反应
D.分子式为C4H7ClO2且能与NaHCO3反应放出气体的有机物结构有5种(不包含立体异构)
解析 A.Na2SO4为钠盐,不属于重金属盐,不能使蛋白质发生变性,则在鸡蛋白溶液中加入浓Na2SO4溶液,蛋白质发生盐析,故A错误;
B.葡萄糖中的—CHO、—OH,能被高锰酸钾氧化,葡萄糖能使酸性高锰酸钾溶液褪色,故B错误;
C.有机物CH2=CHCH(CH3)Cl碳碳双键能发生加成反应、卤原子可取代反应、碳碳双键能发生氧化反应,不能发生缩聚反应,故C错误;
D.分子式C4H8O2并能与NaHCO3溶液反应放出CO2的有机物是丁酸:
CH3—CH2—CH2—COOH或CH3—CH(COOH)—CH3,烃基上一氯代物分别有3种、2种,共5种,故D正确;
故选D。
10.钼(Mo)的主要用途是制造特种钢,用CO还原MoO3(白色粉末,加热时变黄)制备单质Mo的装置如图所示,下列说法正确的是( )
A.装置②中盛有饱和碳酸钠溶液,装置③中盛有浓硫酸,均起到净化CO2的作用
B.装置①中的稀盐酸可用稀硫酸代替,石灰石可用碳酸钠粉末代替
C.装置④的作用是制备CO,装置⑤的作用是CO还原MoO3
D.装置⑥能达到检验MoO3是否被CO还原的目的
解析 选项A,盐酸与碳酸钙反应制备的CO2中含HCl杂质,除去HCl杂质,用饱和NaHCO3溶液,而不是饱和Na2CO3溶液,错误;
选项B,启普发生器中的固体反应物不能呈粉末状,错误;
选项C,装置④中CO2与炽热的C反应生成CO,装置⑤中CO与MoO3发生氧化还原反应,正确;
选项D,装置④中未反应的CO2也能使装置⑥中澄清石灰水变浑浊,错误。
答案 C
11.几种短周期元素的原子半径及主要化合价如图所示,下列叙述不正确的是( )
A.X、Y的最高价氧化物都可以作耐火材料
B.Z的非金属性小于W
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.X的单质可分别与Z、W的单质发生氧化还原反应
解析 依据题图可知元素X、Y、Z、W分别为Mg、Al、N、O,氧化镁和氧化铝的熔点都较高,都可作耐火材料,A项正确;
同一周期主族元素从左到右,非金属性逐渐增强,O的非金属性强于N的,B项正确;
氢氧化铝不能溶于稀氨水,C项错误;
镁能分别与氮气、氧气发生氧化还原反应,D项正确。
12.在一恒温恒压的密闭容器中发生反应:
M(g)+N(g)
2R(g) ΔH<
0,t1时刻达到平衡,在t2时刻改变某一条件,其反应过程如图所示。
下列说法不正确的是( )
A.t1时刻的v(正)小于t2时刻的v(正)
B.t2时刻改变的条件是向密闭容器中加R
C.Ⅰ、Ⅱ两过程达到平衡时,M的体积分数相等
D.Ⅰ、Ⅱ两过程达到平衡时,反应的平衡常数相等
解析 恒温恒压下t2时刻改变某一条件,逆反应速率瞬间增大,再次建立的平衡与原平衡等效,根据等效平衡原理,t2时刻改变的条件是向密闭容器中加R,B项正确;
t1时刻反应达到平衡,v(正)=v(逆),而t2时刻加R,v(正)瞬间不变,v(逆)瞬间增大,故t1时刻的v(正)等于t2时刻的v(正),A项错误;
Ⅰ、Ⅱ两过程达到的平衡等效,M的体积分数相等,C项正确;
Ⅰ、Ⅱ两过程的温度相同,则反应的平衡常数相等,D项正确。
答案 A
13.常温下,将NaOH溶液滴加到某一元酸(HA)溶液中,测得混合溶液的pH与离子浓度变化关系如图所示[已知:
p=-lg]。
下列叙述不正确的是( )
A.Ka(HA)的数量级为10-5
B.滴加NaOH溶液过程中,保持不变
C.m点所示溶液中:
c(H+)=c(HA)+c(OH-)-c(Na+)
D.n点所示溶液中:
c(Na+)=c(A-)+c(HA)
解析 根据题图,m点时p=0,知=1,即c(A-)=c(HA),m点所示溶液pH=4.76,则c(H+)=10-4.76mol·
L-1,Ka(HA)==c(H+)=10-4.76=100.24×
10-5,0<
100.24<
10,故Ka(HA)的数量级为10-5,A项正确;
==,滴加NaOH溶液过程中,温度不变,Ka(HA)、Kw不变,故保持不变,B项正确;
m点所示溶液中的电荷守恒式为c(H+)+c(Na+)=c(OH-)+c(A-),则c(H+)=c(OH-)+c(A-)-c(Na+),C项正确;
n点所示溶液呈酸性,根据电荷守恒式c(H+)+c(Na+)=c(OH-)+c(A-),得c(Na+)-c(A-)=c(OH-)-c(H+)<
0,故c(Na+)<
c(A-),不可能有c(Na+)=c(A-)+c(HA),D项错误。
非选择题
二、非选择题(包括必考题和选考题两部分。
第26~28题为必考题,每道题考生都必须作答。
第35、36题为选考题,考生根据要求作答。
(一)必考题(共43分)
26.(14分)(2018·
成都龙泉中学月考)某同学旅游时发现,苗族人的银饰美丽而富有民族文化,制作银饰时可以选用Fe(NO3)3溶液做蚀刻剂。
受此启发,该同学所在的化学兴趣小组在实验室选用Fe(NO3)3溶液清洗做过银镜反应的试管,发现不但银镜溶解,而且较少产生刺激性气体。
化学兴趣小组对Fe(NO3)3溶液溶解银的原理进行探究:
【提出假设】
假设1:
Fe(NO3)3溶液显酸性,在此酸性条件下NO能氧化Ag;
假设2:
Fe3+具有氧化性,能氧化Ag
【验证假设】
(1)甲同学验证假设1。
①用淡紫色的Fe(NO3)3·
9H2O晶体(分析纯,Mr=404)配制1.5mol/L的Fe(NO3)3溶液100mL。
需要称取________gFe(NO3)3·
9H2O晶体,配制过程中所用到的仪器除烧杯、玻璃棒外还必需:
_________________________________。
②测得1.5mol/L的Fe(NO3)3溶液pH约为1,其原因用化学用语表示为________。
③将pH=1的HNO3溶液加入到镀有银镜的试管中,振荡,观察到银镜慢慢溶解,产生无色气体并在液面上方变为红棕色,溶液中发生反应的离子方程式应是________________________________________________________________
_____________________________________________________________。
④将1.5mol/L的Fe(NO3)3溶液加入到镀有银镜的试管中,振荡,观察到银镜很快溶解,并且溶液颜色加深。
(2)乙同学为验证假设2。
分别用溶质的质量分数为2%、10%的足量FeCl3溶液加入到镀有银镜的试管中,振荡,都看不出银镜溶解。
乙同学由此得出结论,假设2不成立。
你是否同意乙的结论?
_______________________________________,
简述理由:
_______________________________________________。
【思考与交流】
甲同学的实验④中,溶液颜色为什么会加深?
查阅资料得知,Fe2+能与NO形成配离子:
Fe2++NO===[Fe(NO)]2+(棕色)。
已知,同浓度的硝酸氧化性比Fe3+略强。
根据以上信息综合分析,浓、稀Fe(NO3)3溶液溶解银镜时,发生的反应有何不同?
解析 [验证假设]
(1)①用淡紫色的Fe(NO3)3·
9H2O晶体配制1.5mol/L的Fe(NO3)3溶液100mL,依据硝酸铁溶质物质的量为0.15mol,所以需要晶体质量=0.15mol×
404g/mol=60.6g;
配制溶液的过程和步骤分析可知需要的仪器除烧杯、玻璃棒外还必需100mL的容量瓶,胶头滴管;
②测得1.5mol/L的Fe(NO3)3溶液pH约为1说明溶液呈酸性,是铁离子水解的原因,反应的离子方程式为:
Fe3++3H2O
Fe(OH)3+3H+;
③将pH=1的HNO3溶液加入到镀有银镜的试管中,振荡,观察到银镜慢慢溶解,产生无色气体并在液面上方变为红棕色,溶液中发生反应的离子方程式应是:
3Ag+NO+4H+===3Ag++NO↑+2H2O;
(2)假设2中,铁离子的氧化性和铁离子的浓度大小有关,且生成的银离子在溶液中生成氯化银沉淀阻止反应进行,可能是浓度小或阻止反应进行,需要验证亚铁离子的存在证明铁离子是否发生还原反应:
没有检验是否生成了Fe2+,可能是Fe3+与Ag发生了反应,但生成的Ag+与Cl-形成沉淀阻止了反应继续进行,也可能是FeCl3溶液浓度太小而不能溶解银,所以不同意乙的结论;
[思考与交流]已知,同浓度的硝酸氧化性比Fe3+略强,根据以上信息综合分析,浓、稀Fe(NO3)3溶液溶解银镜时的原理不同,Fe(NO3)3浓溶液中,Fe3+、NO都氧化了Ag,Fe(NO3)3稀溶液中可能只有NO氧化了Ag。
答案 【验证假设】
(1)①60.6 100mL容量瓶、胶头滴管 ②Fe3++3H2O
Fe(OH)3+3H+ ③3Ag+NO+4H+===3Ag++NO↑+2H2O
(2)不同意 没有检验是否生成了Fe2+,可能是Fe3+与Ag发生了反应,但生成的Ag+与Cl-形成沉淀阻止了反应继续进行,也可能是FeCl3溶液浓度太小而不能溶解银
【思考与交流】已知,同浓度的硝酸氧化性比Fe3+略强,根据以上信息综合分析,浓、稀Fe(NO3)3溶液溶解银镜时的原理不同,Fe(NO3)3浓溶液中,Fe3+、NO都氧化了Ag,Fe(NO3)3稀溶液中可能只有NO氧化了Ag
27.(14分)我国电池的年市场消费量约为80亿只,其中70%是锌锰干电池,利用废旧锌锰干电池制备硫酸锌晶体(ZnSO4·
7H2O)和纯MnO2的工艺如下图所示:
已知:
①锌皮的主要成分为Zn,含有少量Fe;
炭包的主要成分为ZnCl2、NH4Cl、MnO2、碳粉等,还含有少量的Cu、Ag、Fe等。
②Ksp[Zn(OH)2]=2.0×
10-16;
Ksp[Fe(OH)2]=8.0×
Ksp[Fe(OH)3]=4.0×
10-38。
(1)除去炭包中碳粉的操作为________。
A.酸浸B.过滤
C.焙炒D.焙烧
(2)粗MnO2转化为MnSO4时,主要反应的离子方程式为_________________
___________________________________________________________________。
(3)焙烧时发生反应的化学方程式为__________________________________。
(4)制备硫酸锌晶体流程中,用ZnO调节溶液pH的目的是_________________,
若溶解时不加H2O2带来的后果是______________________________________。
(5)“草酸钠-高锰酸钾返滴法”可测定MnO2的纯度,取agMnO2样品于锥形瓶中,加入适量稀硫酸,再加入V1mLc1mol·
L-1Na2C2O4溶液(足量),最后用c2mol·
L-1的KMnO4溶液滴定剩余的Na2C2O4,达终点时消耗V2mL标准KMnO4溶液。
①MnO2参与反应的离子方程式为____________________________。
②该样品中MnO2的质量分数为________(假定杂质不参与反应,列出表达式即可)。
答案
(1)C(提示:
焙炒过程中碳粉与空气中的氧气可生成CO2而除去)
(2)MnO2+H2O2+2H+===Mn2++O2↑+2H2O
(3)2MnCO3+O22MnO2+2CO2
(4)除去溶液中的Fe3+杂质 Fe2+与Zn2+不能分离[或当Fe(OH)2沉淀完全时,Zn(OH)2也沉淀完全]
(5)①MnO2+4H++C2O===Mn2++2CO2↑+2H2O
②×
100%
28.(15分)已知借助太阳能-热化学循环分解水的示意图如图1:
(1)反应Ⅱ需要两步能量转化才能实现,太阳能转化为________,再转化为________。
(2)反应Ⅳ由(a)、(b)两步反应组成:
H2SO4(l)===SO3(g)+H2O(g) ΔH=+177kJ·
mol-1(a)
2SO3(g)
2SO2(g)+O2(g) ΔH=+196kJ·
mol-1(b)
H2O(l)===H2O(g) ΔH=+44kJ·
mol-1(c)
则H2SO4(l)分解为SO2(g)、O2(g)及H2O(l)的热化学方程式为_____________________________________________________________。
(3)在恒容的密闭容器中进行不同温度下的SO3分解实验[原理按反应(b)],SO3起始物质的量均为dmol,图2中L曲线为SO3的平衡转化率与温度的关系,M曲线表示不同温度下反应经过相同反应时间且未达到化学平衡时SO3的转化率。
①反应(b)的平衡常数表达式为K=________。
②随温度的升高,M曲线逼近L曲线的原因是__________________________。
③若X点时总压为0.1MPa,列式计算SO3分解反应在图2中X点时的平衡常数Kp=________(用平衡分压代替平衡浓度计算,分压:
总压×
物质的量分数,保留2位有效数字)。
解析
(1)据题图1分析,反应Ⅱ是太阳能转化为电能,电解亚硫酸铵生成硫酸铵和氢气,故太阳能转化为电能,再转化为化学能。
(2)根据盖斯定律,由2(a)+(b)-2(c)得:
2H2SO4(l)
2SO2(g)+O2(g)+2H2O(l) ΔH=+462kJ·
mol-1。
(3)②温度升高,反应速率加快,达到平衡所需的时间缩短。
③起始时充入dmolSO3,由题图2可知X点时SO3的平衡转化率为60%,转化的三氧化硫的物质的量为dmol×
0.6=0.6dmol,利用三段式法进行计算,则:
故Kp===0.052MPa。
答案
(1)电能 化学能
(2)2H2SO4(l)
mol-1
(3)① ②温度升高,反应速率加快,达到平衡所需的时间缩短(或温度升高,反应速率加快,相同时间内更快达到平衡) ③0.052MPa
(二)选考题:
共15分。
请考生从给出的2道题中任选一题作答。
如果多做,则按所做第一题计分。
35.【选修3:
物质结构与性质】
(15分)(2018·
河北省五个一联盟第二次联考)我国南京理工大学胡炳成教授团队在N5合成上取得了里程碑性研究成果——世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。
时隔不久,他们在该领域再次取得突破,成功制得全氮阴离子(N)金属盐Co(N5)2(H2O)4·
4H2O。
这是一种配合物分子,其结构式为
回答下列问题:
(1)基态氮原子最高能层电子所占用能级的电子云形状为________。
(2)元素的基态气态原子得到一个电子形成气态-1价离子时所放出的能量称作第一电子亲和能(E),-1价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如下表所示。
元素
Cl
Br
I
O
O-
电子亲和能
(kJ/mol)
349
343
295
141
-780
①图中数据显示,同主族元素E1自上而下依次减小,试说明原因_____________________________________________________;
②下列说法正确的是________。
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O2-时放出141kJ的能量
C.氧元素的第二电子亲和能是-780kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
(3)从结构角度分析,按顺序写出R中两种阳离子的立体构型:
________。
(4)试就上述两种盐进行有关分析:
①热分析结果显示盐(N5)6(H3O)3(NH4)4Cl分解温度高达116.8℃,具有非常好的热稳定性。
这与其结构中含有类似苯分子中的大π键有关。
N中的N原子的杂化轨道类型为________,N中的σ键总数为________个。
②金属盐Co(N5)2(H2O)4·
4H2O中,中心原子的配位数为________,试画出金属盐Co(N5)2(H2O)4·
4H2O中钴离子的价电子的排布图________。
(5)R的晶体密度为dg·
cm-3其立方晶胞参数为anm,晶胞中含有y个[(N5)6(H3O)3(NH4)4Cl]单元,该单元的相对质量为M,则y的计算表达式为________(用NA和字母表示)。
解析
(1)基态氮原子的电子排布为1s22s22p3,所以其最高能层电子所占用的能级为2s和2p,s电子云为球形,p电子云为哑铃形。
(2)①同主族元素自上而下原子半径逐渐增大,原子核和最外层电子之间的距离增大,所以原子核对于最外层电子的吸引能力减弱,即得电子能力减弱,所以同主族元素E1自上而下依次减小。
②电子亲和能越大代表原子得电子时放出能量越多,所以电子亲和能越大,说明越容易得到电子,选项A错误。
一个基态的气态氧原子得到一个电子时应该成为O-,所以选项B错误。
氧原子得到1个电子生成O-放出的能量是氧元素的第一电子亲和能,O-再得到1个电子生成O2-时放出的能量是氧元素的第二电子亲和能,所以氧元素的第二电子亲和能就是O-的第一电子亲和能,即为-780kJ/mol,选项C正确。
气态氧原子得到1个电子放出141kJ的能量生成O-,O-再得到1个电子需要吸收780kJ的能量,所以气态氧原子得到两个电子成为O2-需要吸收能量,选项D正确。
(3)根据价层电子对互斥理论,H3O+的中心氧原子有(6+3-1)÷
2=4个电子对,所以O以sp3杂化成四面体构型,其中三个电子对成键,一个为孤对电子,所以H3O+三角锥构型。
NH的中心N原子有(5+4-1)÷
2=4个电子对,所以N以sp3杂化成四面体构型,其中四个电子对都成键,所以NH为正四面体构型。
(4)①N结构中含有类似苯分子中的大π键,所以N一定是平面封闭环状结构(
),所以N原子的杂化类型一定是sp2杂化,这样才能保证其形成平面环状结构。
根据两个原子之间成键一定有且只有1个σ键的原理,得到N的平面环状结构中一定有5个σ键。
4H2O中,N和H2O都是单齿配体,所以中心原子的配位数为6。
Co是27号元素,其电子排布为1s22s22p63s23p63d74s2,所以Co2+的价电子为3d7,价电子排布图为
(5)(或×
10-21)
36.【选修5:
有机化学基础】
(15分)党的十九大报告中明确了“加快生态文明体制改革,建设美丽中国”,把“推进绿色发展”放到了首位,强调“加快建立绿色生产和消费的法律制度和政策导向,建立健全绿色低碳循环发展的经济体系”。
化工生产中倡导原料尽量多地转化为目标产物,提高原子利用率。
利用下列合成路线可以制备对羟基苯甲酸:
①该合成路线中,生成G、F的物质的量之比为n(G)∶n(F)=1∶3,且1molG与足量的Na反应产生33.6L(标准状况)H2。
②同一碳原子上连两个羟基不稳定。
(1)下列关于对羟基苯甲酸的说法中正确的是________(填序号)。
a.能发生聚合反应生成聚酯
b.能与FeCl3溶液发生显色反应
c.1mol对羟基苯甲酸最多能与1molNaOH反应
d.对羟基苯甲酸能发生酯化反应和水解反应
(2)H的化学名称是________。
(3)A生成B的反应类型是________,A中含氧官能团的名称是________。
(4)B生成C和D的化学方程式为________________________________。
(5)满足下列条件的对羟基苯甲酸的同分异构体共有________种(不包括立体异构),其中核磁共振氢谱中有4种不同化学环境氢原子的同分异构体有________种。
①能与银氨溶液发生银镜反应;
②与FeCl3溶液发生显色反应。
(6)写出由H制备G的合成路线(无机试剂任选)。
解析 1molG与足量Na反应产生H2的物质的量为=1.5mol,结合G的分子式可知G中含有3个羟基,结合已知信息②可推知G为
,结合N的分子式及N在碱性条件下水解、酸化后生成的n(G)∶n(F)=1∶3可知,F为CH3COOH,N为
。
由E的结构简式为
可逆推知A中含有苯环,A与Cl2在光照条件下发生取代反应生成B,B在氢氧化钠水溶液、加热条件下发生水解反应生成C与D,D酸化后得到F(乙酸),则D为CH3COONa,C中含有7个C