第二章化学平衡文档格式.docx
《第二章化学平衡文档格式.docx》由会员分享,可在线阅读,更多相关《第二章化学平衡文档格式.docx(14页珍藏版)》请在冰豆网上搜索。
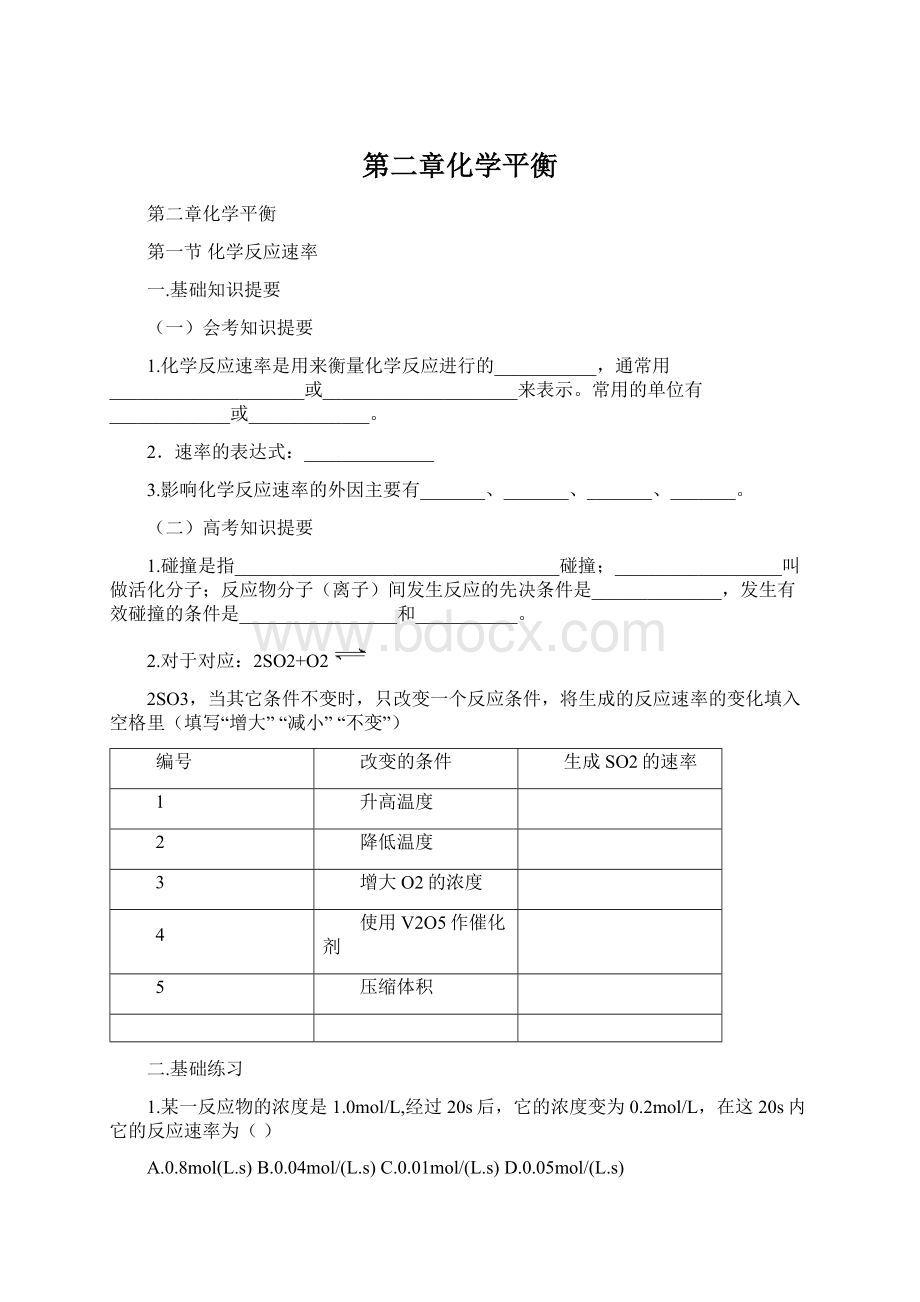
其中反应速率最大的是()
A.20ml3mol·
L-1的x溶液B.20ml2mol·
L-1的x溶液
C.10ml4mol·
L-1的x溶液D.10mL2mol·
4.在2L密闭容器中,发生反应3A(g)+B(g)
2c(g),若最初加入A和B都是4mol,A的平均反应速率为0.12mol·
(L·
S)-1,则10秒钟后容器中的B有()
A.2.8molB.1.6molC.3.2molD.3.6mol
5.NO和CO都是汽车尾气里出有害物质,它们能缓慢起反应,生成氮气和二氧化碳,对此反应,下列叙述正确的是()
A.使用催化剂不改变反应速率
B.降低压强能加大反应速率
C.升高温度能加快反应速率
D.改变压强对反应速率无影响。
6.根据化学反应A+B
2C,填写下表中的空白:
A
B
C
反应开始时浓度
mol/L
2.7
2.5
2min后的浓度
2.3
化学反应速率mol/(L.min)
三.提高练习
1.反应N2+3H2
2NH3刚开始时,N2的浓度为3mol/L,H2的浓度5mol/L,3min后测得NH3浓度为0.6mol/L,则此时间内,下列反应速率表示正确的是()
A.v(NH3)=0.6mol/(L.min)B.v(N2)=0.1mol/(L.min)
C.v(H2)=0.2mol/(L.min)D.v(NH3)=0.1mol/(L.min)
2.已知某反应的各物质浓度数据如下:
aA(g)+bB(g)
2C(g)
起始浓度(mol/L)
2s末浓度(mol/L)
据此可推算出上述方程式中各物质的计量数之比是()
A.9:
3:
4B.3:
1:
2C.2:
3D.3:
2:
3.可逆反应:
A+3B
2C+2D在4种不同的情况下的反应速率分别为①v(A)=0.15mol/L·
s②v(B)=0.6mol/L·
s③v(C)=0.4mol/L·
s④v(D)=0.45mol/L·
s该反应进行速率最快的是()
A.①B.②和③C.④D.①和④
4.在密闭容器中进行可逆反应,A跟B反应生成C,反应速率v(A).v(B).v(C)之间存在以下关系:
v(B)=3v(A),v(C)=2v(A),3v(C)=2v(B),则该反应可表示为()
A.A+B
CB.2A+2B
3C
C.3A+B
2CD.A+3B
2C
5.下列说法中正确的是()
A.0.1mol/LHCl和0.1mol/LHAC与2mol/LNaOH溶液反应速率相同
B.大理石块与大理石粉分别同0.1mol/LHCl反应速率相同
C.Mg.Al在相同条件下分别与0.1mol/LHCl反应,其反应速率相同
D.0.1mol/LHCl和0.1mol/LHNO3与相同形状和大小的大理石反应,速率相同
6.将等物质的量的A.B混合于2L的密闭容器中,发生如下反应:
3A(g)+B(g)
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):
c(B)=3:
5,C的平均反应速率为0.1mol/(L.min)。
试求:
(1)此时A的浓度及反应开始前容器中A.B的物质的量;
(2)B的平均反应速率;
(3)x的值。
第二节化学平衡
1.化学平衡状是指____________的______反应里,______和______的速率相等,反应混合物中各组分的______保持不变的状态。
1.一定温度下,在10L密闭容中加入3molSO2和2molO2,反应达到平衡时生成2.5molSO3,平衡时SO2的转化率是_______;
容器内各物质总的物质是_______;
平衡时容器内的压强是反应前压强的______倍。
2.将等物质的量的A.B.C.D四种物质混和,发生如下反应:
aA+bB
cC(固)+dD
当反应进行一定时间后,测得A减少了n摩,B减少了1/2n摩,C增加了3/2n摩,D增加了n摩,此时达到化学平衡:
(1)该化学方程式中各物质的系数为:
a=______b=______c=______d=______。
(2)若只改变压强,反应速度发生变化,但平衡不发生移动,该反应中各物质的聚集状态:
A________B________C_________D_________
(3)若只升高温度,反应一段时间后,测知四种物质其物质的量又达到相等,则该反应为__________________反应(填“放热”或“吸热”)
二.基础提要
1.可逆反应达到平衡的重要标志是()
A.反应停止了
B.正反应速率均为零
C.正逆反应都还在继续进行
D.正逆反应的速相等
2.在一定条件下,使N2和H2在一密闭容器中进行反应,下列说法中不正确的是()
A.反应开始时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后为零
C.随着反应的进行,逆应速率逐渐增大,最后不变
D.随着反应的进行,正反应速率逐渐减小,最后不变
3.在一定条件下,对于密闭容中进行的反应P(g)+Q(g)
R(g)+S(g)。
下列说法中可能充分说明这一反应己达到化学平衡的是()
A.P、Q、R、S的浓度相等
B.P、Q、R、S在密闭容器中共存
C.P、Q、R、S的浓度不再变化
D.用P的浓度表示的化学反应速率与用Q的浓度表示的化学反应速率相等
4.对于达到平衡状态的可逆反应:
N2+3H2
2NH3,下叙述正确的是()
A.反应物和生成物浓度不再发生变化B.反应物和生成物的浓度相等
C.N2和NH3的质量分数相等D.正反应和逆反应不再进行
5.当可逆反应2SO2+O2
2SO3达平衡后通入18O2,再次达到平衡时,18O存在于()
A.SO2、O2B.SO2、SO3C.SO2、SO3、O2D.SO3、O2
6.K2Cr2O7是橙红色晶体,K2CrO4是黄色晶体,若将K2Cr2O7配成一定浓度的溶液,可以发生的离子反应方程式为:
Cr2O72-+H2O
2CrO42-+2H+,当达到平衡时,溶液的颜色在橙色和黄色之间,试回答:
(1)向盛有2mL的上述K2Cr2O7溶液的试管中滴入10滴2mol/L的氢氧化钠溶液,则试管中的溶液呈_____色。
原因是_____________________。
(2)向
(1)所得的溶液中滴入5滴2mol·
L-1的硫酸溶液,试管中溶液呈____色,理由是_______。
(3)另取上述K2Cr2O7溶液2mL于试管中,小心加热,接近沸腾时,试管中的溶液颜色会有何变化_______,理由是_________。
三.提高提要
1.在一定条件下,向2L密闭容器中充入3molx气体和1moly气体,发生下列反应:
2X(g)+Y(g)
3Z(g)+2W(g)在某时刻测定出的下列各生成物的浓度,一定不正确的是()
A.[z]=0.45mol/LB.[z]=1.50mol/L
C.[W]=1.60mol/LD.[W]=0.80mol/L
2.在一定温度下,下列叙述不是可逆反应A(g)+2B(g)
3C(g)达到平衡的标志的是()
(1)C的生成速率与C的分解速率相等;
(2)单位时间生成amolA,同时生成3amolB;
(3)A.B.C的浓度不再变化;
(4)A.B.C的压强不再变化;
(5)混合气体的总压强不再变化;
(6)混合气体的物质的量不再变化;
(7)单位时间消耗amolA,同时生成3amolB;
(8)A.B.C的分子数目比为1:
3:
2。
A.
(2)(8)B.(7)(4)
C.
(1)(3)D.(5)(6)
3.在密闭容器中通人一定量的HI气体,使其在一定条件下发生反应:
2HI(g)
H2(g)+I2(g)。
下列叙述中一定属于平衡状态的是()
A.HI.H2.I2的浓度相等 B.混合气体的颜色不变化时
C.混合气体的总压不变时 D.v(HI):
v(H2):
v(I2)=2:
1:
1时
4.一定温度下,向一固定容积的容器中放入1molA和1molB,待反应
A(S)+B(g)
C(g)+2D(g)达到平衡时,C的质量分数是M%,在相同的条件下,若按以下配比开始反应,平衡时C的质量分数比仍为M%的是()
A.2molA+2molBB.1molD+2molC
C.2molD+1molA+1molBD.0.5molA+0.5molB+0.5molC+1.0molD
5.有一可逆反应2A(g)+3B(g)
4C(g)+D(g),已知起始浓度[A]=2mol/L,[B]=3mol/L,[C]=[D]=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是()
A.前20min的平均反应速率
B.A的转化率为50%
C.C的平衡浓度[C]=4mol/L
D.B的平衡浓度[B]=1.5mol/L
6.某温度时,在2L容器中某一反应的A.B物质的量随时间变化的曲线如右图所示,由图中数据分析得:
(1)该反应的化学方程式为
。
(2)反应开始时至4min时,A的平均反应速率为。
(3)4min时,正逆反应速率的大小关系为:
v正v逆(填“>
”.“<
”或“=”);
8min时,v正v逆。
第三节影响化学平衡的条件
(一)会考知识提要
1.对于反应mA(g)+nB(g)
pC(g)+qD(g)
条件改变
反应类型
反应速率
平衡移动方向
增大反应物浓度
__________________
减小反应物浓度
增大生成物浓度
减小生成物浓度
增大压强
m+n>
p+q
m+n<
m+n=p+q
减小压强
放热反应
吸热反应
结论:
如果改变影响平衡的一个条件,平衡就向能减弱这种改变的方向移动。
(二)高考知识提要
1.一定条件下,反应2A+B
2C在密闭容器中达到平衡。
己知A为气态物质,当其他条件不变时,改变压强,平衡不发生移动,则B为态物质,C为态物质。
如果升高温度,A的物质的量增加,则正反应是(放热或吸热)反应。
2.在一定条件下,下列反应达到化学平衡:
H2(g)+I2(g)(正反应为吸热反应)
(1)如果升高温度,平衡混合物的颜色。
(2)如果加入一定的H2,平衡移动。
(3)如果使密闭容器的体积增大,平衡移动。
1.反应2A(气)
2B(气)+E(气)达到平衡时,要使平衡朝正反应方向移动,下列措施中正确是是()
A.加压B.增加B的浓度C.减少A的浓度D.减少E的浓度
2.Cl2+H2O
HCl+HClO达到平衡后,要使HClO的浓度增大,可加入()
A.H2OB.Cl2C.NaOH(固)D.NaCl(固)
3.漂白粉的有效成分在溶液中存在下列平衡:
ClO-+H2O
HClO+OH-。
下列措施中能增强漂白粉漂白效果的是()
A.降低温度B.加H2OC.加入适量盐酸D.加入适量烧碱溶液
4.能确认发生了化学平衡移动的是()
A.化学反应速率发生了变化
B.可逆反应达到平衡后,使用了催化剂
C.有气体物质参加的可逆反应达到平衡后,增大对容器的压强
D.由于某一条件的改变,使平衡混合物中各组分的浓度发生了不同程度的改变。
5.在一个密闭容器中,下列反应达到平衡:
aA(g)+bB(g)
cC(g)+dD(g)。
如果升高温度或降低压强,则C物质的量都增大,试判断下列各组中关系正确的是()
A.a+b<
c+d正反应为吸热反应
B.a+b>
C.a+b<
c+d正反应为放热反应
D.a+b=c+d正反应为吸热反应
6.下列平衡体系中,改变某条件平衡将如何移动?
(1)CO+NO2
CO2+NO(正反应放热反应)。
升高温度,增大压强。
(2)3NO2+H2O
2HNO3+NO。
通入O2,增大压强。
(3)2SO2+O2
2SO3(正反应为放热反应)增加V2O5,降低温度。
1.溴水中存在着下列平衡Br2+H2O
HBr+HBrO,若要使溴水橙色褪去,可加()
A.H2OB.盐酸C.NaOH溶液D.溴化钠溶液
2.图中表示外界条件(t.p)的变化对下列反应的影响:
L(固)+G(气)
2R(气)(正反应为吸热反应),y轴表示的是()
A.平衡时,混合气中R的百分含量
B.平衡时,混合气中G的百分含量
C.G的转化率
D.L的转化率
3.下列事实中不能应用勒沙特列原理来解释的是()
A.向H2S水溶液中加入NaOH有利于S2-增多
B.加入催化剂有利于氨的氧化反应
C.高压对合成氨有利
D.500℃左右比室温更有利于合成氨的反应
4.对于达平衡的可逆反应X+Y
W+Z,增大压强则正.逆反应速度(v)的变化如上图,分析可知X,Y,Z,W的聚集状态可能是()
A.Z、W为气体,X、Y中之一为气体
B.Z、W中之一为气体,X、Y为非气体
C.X、Y、Z皆为气体,W为非气体
D.X、Y为气体,Z、W中之一为气体
5.在体积不变的密闭容器中,在一定的条件下发生下列反应:
2A
B(气)+C(固),达到化学平衡后,升高温度使容器内气体的密度增大,则下列叙述中正确的是:
()
A.正反应是吸热反应,则A为非气体
B.若正反应为放热反应,则A为气态
C.在平衡体系中加入少量的C,该平衡向逆反应方向移动
D.改变压强对该平衡的移动无影响
6.在2L的密闭容器中,充入1molN2和3molH2,在一定的条件下反应,2分钟后达到平衡状态,相同温度下,测得平衡时混合气体的压强比反应前混合气体的压强减小了1/10,填写下列空白:
(1)平衡时混合气体中三种气体的物质的量比为_________________
(2)N2的转化率为_______________
(3)2分钟内,NH3的平均反应速率为_______________
第四节合成氨条件的选择
1.目前合成氨生产中,混合气N2.H2进入铁触媒室前的温度约为________,从铁触媒室逸出的气体温度比进入铁触媒时________(填高或低),这是因为________________________________________________________。
1.对于反应N2+3H2
2NH3(正反应放热),达到化学平衡时若增大N2的浓度,H2的转化率将________;
若增大压强,NH3在反应混合物中的质量分数将________;
若升高温度,H2的转化率将________,反应速率________;
加入催化剂,平衡(发生或不发生)________移动,单位时间内NH3的产量会________。
2.在1L密闭容器中,充入amolN2和bmolH2,在一定温度下N2+3H2
2NH3,达到平衡,容器中还剩余CmolN2,则平衡时N2的转化率是,H2的转化率是,生成NH3是mol,容器中H2的平衡浓度是。
1.下列各项中,理由不能解释做法的是()
A.合成氨的正反应是一个体积缩小的反应,采取高压有利于NH3的生成。
B.合成氨是一个放热反应,采取较高的温度有利于提高单位时间内氨的产量。
C.减小生成物浓度有利于平衡向右移动,所以生产中不断将NH3分离出去。
D.催化剂可能缩短到达平衡的时间,合成氨要使用催化剂。
2.对于反应N2+3H2
2NH3(正反应放热),低温有利于平衡向右移动,但工业上采取较高温度(500℃),其原因是()
A.低温下反应速度慢B.低温下转化率不高
C.低温下不易将NH3分离出来D.低温下催化剂活性不高
3.反应NH4HS(S)
NH3(g)+H2S(g)在某一温度达到平衡时,下列各种情况中,不能使平衡发生移动的是()
A.其它条件不变,通入SO2气体B.移动一部分NH4HS固体
C..容器的体积不变,加入H2SD.压强不变,充入N2
4.从化学反应速率和化学平衡两方面考虑,合成氨应采用的条件是()
A.低温.高压.催化剂
B.低温.低压.催化剂
C.高温.高压.催化剂
D.适当温度低温.高压.催化剂
5.工业上用氢气和氮气合成氨,氢气的主要来源是()
A.水和燃料B.电解水
C.锌和稀H2SO4D.液化空气
6.1molN2和3molH2在一定温度和压强下反应达到平衡,生成0.3molNH3。
如果维持温度和压强不变,达平衡时混合气体的体积是反应前N2和H2的总体积的几分之几?
1.下列反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是()
A.2NO2
N2O4(正反应为放热反应)
B.C(S)+CO2
2CO(正反应为吸热反应)
C.N2+3H2
2NH3(正反应为放热反应)
D.H2S
H2+S(s)(正反应为吸热反应)
2.在密闭容器中充入1molN2和3molH2,一定条件下反应达到平衡状态时,有60%的H2转化为NH3,则混合气体在反应前与达到平衡后的物质的量之比为()
A.10:
7B.7:
10C.5:
3D.3:
3.在密闭容中通入5molN2和5molH2,在一定条件下反应达到平衡,测得平衡体系中有2molNH3,则此时容器中压强是反应前的()
A.1.2B.0.8C.0.6D.0.4
4.在密件闭容器中进行合成氨反应,N2+3H2
2NH3达到平衡后,当其他条件不变时,将平衡体系中各物质浓度都增加到原来的2倍,下列叙述不正确的是()
A.平衡向正反应方向移动
B.达到新平衡时,c(N2)比原平衡大
C.达新平衡时正.逆反应速率均比原平衡大
D.达到新平衡时,混合气体的密度变小
5.对于mA(g)+nB(g)
pC(g)+qD(g)的平衡体系,当升高温度时,体系的平均相对摩尔质量从26变为29,则下列说法正确的是()
A.m+n>p+q,正反应是放热反应
B.m+n>p+q,正反应是吸热反应
C.m+n<p+q,逆反应是放热反应
D.m+n<p+q,逆反应是吸热反应
6.在一定条件下,将N2和H2的混合气体100mL通入密闭的容器中,到达平衡时,容器内的压强比反应前减小
,又测得此时混合气体的平均式量为9,试求:
(1)原混合气体中N2和H2各为多少mL?
(2)H2的转化率是多少?