BactoBac杆状病毒表达系统Word文档下载推荐.docx
《BactoBac杆状病毒表达系统Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《BactoBac杆状病毒表达系统Word文档下载推荐.docx(33页珍藏版)》请在冰豆网上搜索。
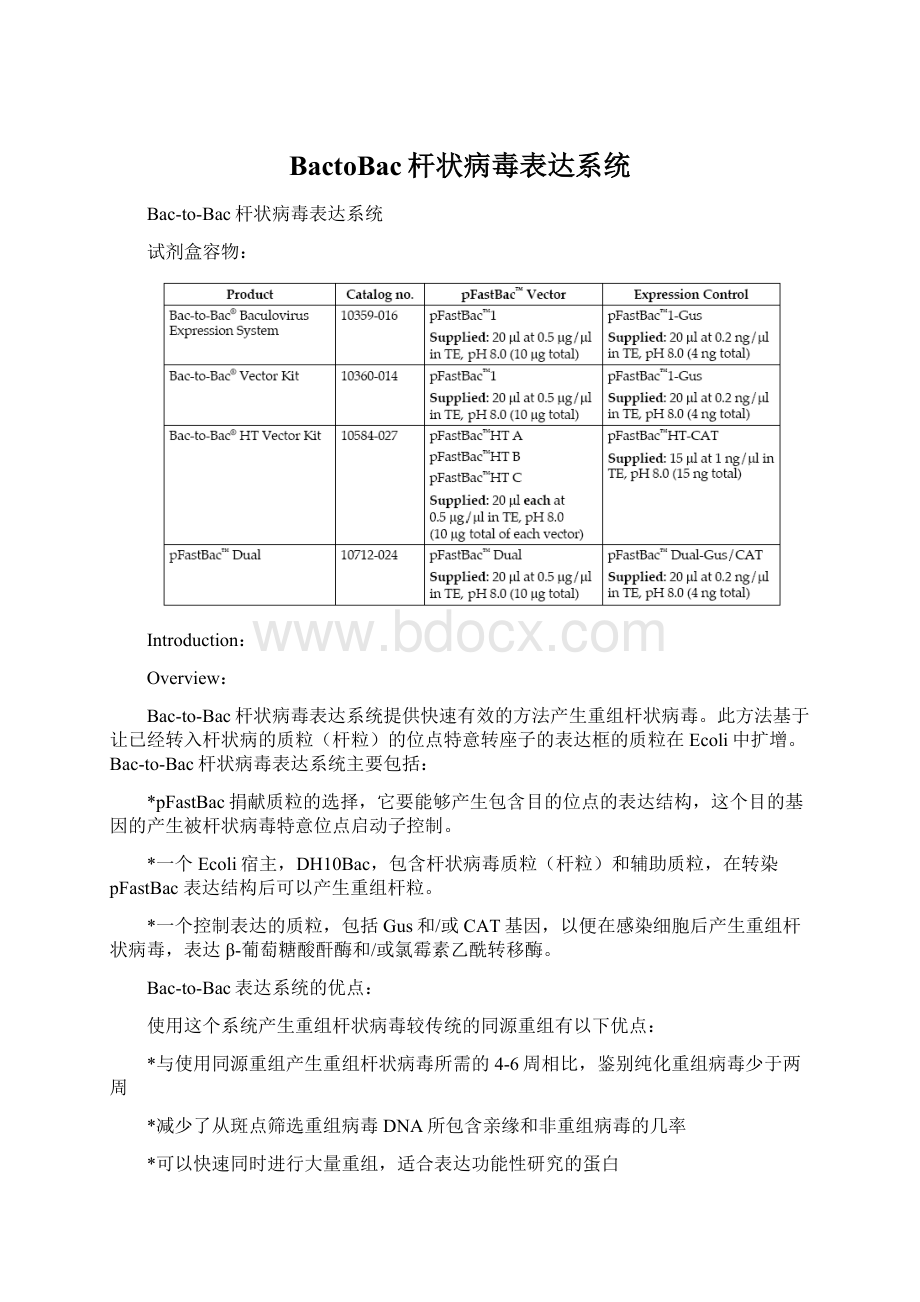
指南提供了一个对于Bac-to-Bac表达系统的概述,并对以下提供指导:
1、克隆目的基因到pFastBacTM供体质粒的选择
2、转化pFastBacTM结构到最高效的DH10BacTM产生重组质粒
3、转染重组质粒DNA到昆虫细胞产生重组杆状病毒
4、扩增滴定(Amplifyandtiter)杆状病毒株,使用病毒株感染昆虫细胞表达目的重组蛋白
重要的:
Bac-to-Bac杆状病毒表达系统是用来帮助你产生重组杆状病毒,在昆虫细胞中进行高水平表达目的基因的系统。
虽然他可以帮助你很容易的产生杆状病毒表达你的重组蛋白,但是使用这系统更倾向于有杆状病毒生物学和昆虫表达背景的使用者。
我们高度推荐使用者具有病毒和组织培养的技术和知识。
Bac-to-Bac表达系统
表达系统的成分:
表达系统简单高效的产生重组杆状不能给党。
基于Luckow1993年的方法,此系统利用了位点特意的专座子Tn7区简化和提高重组质粒DNA
*系统的第一个成分是用来克隆目的基因的pFastBacTM菌株。
基于pFastBacTM菌株的选择,表达基因被AcMNPV的PH或p10启动子控制,在昆虫细胞高水平表达表达框被Tn7的左右臂包围,并且包含一个庆大霉素抗性点和SV40多腺苷酸化信号,形成一个微型的Tn7
*第二个主要结构是Ecoli的DH10BacTM品系,用来作为pFastBacTM菌株的宿主。
DH10BacTM细胞包含带有微型-attTn7靶位点的病毒质粒和辅助质粒(详细见下文)。
一旦pFastBacTM表达质粒转入DH10Bac细胞,转化就会发生在pFastBacTM菌株的微型Tn7单位和微型-attTn7的靶位点之间产生重组质粒。
这个转化反应发生在辅助质粒提供的转化蛋白处。
如果你已经完成了转化反应,你需要分离这个高分子量的重组质粒DNA并将质粒DNA转染如昆虫细胞趋产生重组杆状病毒,用来进行初步表达实验。
在杆状病毒株扩增和滴定后,高效价的病毒株可以用来感染细胞,进行大规模的重组蛋白的表达。
杆状病毒菌株:
病毒菌株(杆粒),bMON14272(136KB),在DH10BacEcoli中包括:
*一个低拷贝的微型F复制子
*卡那霉素的抗性标记
*一个来自于pUC载体的编码LacZa肽的DNA片段,用来接触病毒转座子,Tn7(微型attTn7)已经被插入。
插入的微型attTn7不会中断LacZa肽的阅读框。
杆粒在具有卡那抗性的大的质粒EcoliDH10Bac中扩增,在显色物质如Bluo-gal或X-gal和诱导剂IPTG存在时,能补充染色体LacZ的缺失形成蓝斑(LacZ+)
辅助质粒:
DH10BacEcoli也包含辅助质粒,pMON7124(13.2kb),他编码转移酶和四环素抗性基因。
这个辅助质粒提供Tn7转化功能。
图示Bac-toBac系统:
下图刻画了重组病毒的产生和目的基因的表达
实验轮廓:
流程:
下图揭示了表达目的基因的一般步骤
1、pFastBacdonor质粒(步骤:
目的基因的克隆)得到
2、pFastBac重组体(转化至DN10Bac细胞(含有杆粒和helper))得到
3、含有重组杆粒的Ecoli细胞(重新划线)得到
4、验证过的含有重组杆粒的Ecoli细胞(过夜培养,分离重组杆粒DNA)得到
5、重组杆粒DNA(使用Cellfectin试剂感染细胞)得到
6、P1重组杆状病毒株(>106pfu/ml)(感染昆虫细胞扩增病毒)得到
7、P2重组杆状病毒株(>107pfu/ml)(滴定感染昆虫细胞)得到
8、蛋白的表达
培养昆虫细胞:
一般指导:
介绍:
对于您的杆状病毒转移菌,我们推荐使用Sf9和Sf21昆虫细胞作为宿主。
在开始你的转化试验和表达之前,确定你有收获的Sf9和Sf21,并将其冻存。
使用无血清的介质:
昆虫细胞可能在无血清的条件下收获。
我们推荐使用Sf900ⅡSFM。
Sf900ⅡSFM对于维持Sf9和Sf21以及对于大规模生产重组蛋白,都是无蛋白的最优的介质。
昆虫细胞培养参考指导:
维持和传代昆虫细胞在贴壁和悬浮条件下
冷冻细胞
使用无血清的介质
按比例增加细胞产量
昆虫细胞对于环境很敏感,此外化学和营养因素,物理因素都可以影响昆虫细胞的成长。
需要优化以得到最大产量。
考虑以下培养条件:
*温度:
细胞的感染和成长的最适合围是27-28度
*PH:
对于许多培养系统6.1-6.4时合适的围。
Sf900ⅡSFM在此围支持一般的空气和开盖培养
*同渗重摩:
鳞翅类细胞使用介质的最优同渗重摩是345-380mOsm/kg
*通风:
对于最优生长条件和蛋白的表达,昆虫细胞要求被动的通氧。
积极的通氧系统要求溶氧饱和在10%-50%
*剪切力:
悬浮培养产生机械剪切力。
生长的昆虫细胞在含有血清的介质中(10%-20%FBS),对于细胞的剪切力一般会得到足够的保护。
如果你的细胞在无血清条件下生长,加入剪切力保护剂例如PluronicF-68。
注意:
在Sf900ⅡSFM中生长的细胞不需要加入剪切力保护剂。
转染的细胞:
你需要的是对数期的细胞>95%发育能力,可以完成成功的转染。
产生重组的pFastBacTM菌株(Vector)
一般信息:
为了产生包含目的基因的重组质粒,使用Bac-to-Bac杆状病毒表达系统,你需要使用限制酶消化和连接,将你的目的基因克隆进入pFastBac菌的其中一种。
一般分子生物学技术:
为了帮助限制酶消化和连接DNA的序列,需要其他一般的分子生物学技术
扩增和保存质粒:
pFastBac菌种和他的相应的表达对照质粒包含氨苄青霉素抗性基因,可以使用Ecoli进行Amp筛选。
为了扩增和保存pFastBac和pFastBac对照质粒,使用以下方法:
1、使用载体株系感染一个recA,endAEcoli株,例如Top10,DH10B或者DH5α
2、在含有100ug/mlAmp的LB琼脂糖平板选择转化株。
3、选择含有质粒的转化子制备甘油菌以便长期保存
克隆进入pFastBacTM1
为了帮助你设计策略克隆你的目的基因进入pFastBacTM1,参考以下建议和表格
克隆考虑事项:
pFastBacTM1菌株是非融合菌株(无融合标签)。
为了保证重组蛋白的表达,你的插入必须含有:
*一个ATG起始密码子用于转录起始
*一个终止密码子。
终止密码子包含在所有三个阅读框中的多克隆位点中
重组蛋白的产生要求你的插入包含一个转录起始ATG。
一般来说,转移载体包含完整的PH引导序列,可以提高表达的产量。
蛋白翻译能够起始于多克隆位点上游突变的ATG(ATT),尽管如此,从这个位点起始的效率是低的,而且一般不干涉表达和重组蛋白的检测。
pFastBacTM1的多克隆位点:
下图是pFastBacTM1的多克隆位点。
限制位点标出来以便显示实际切刻位点。
潜在的终止密码子下划线表示。
pFastBacTM1的全序列可以从下载。
pFastBacTM1的图谱和描述见后缀
克隆进入pFastBacTMHTA,B,C
pFastBacTMHT载体由三个读码框(A,B,C)提供的多克隆位点从而实现克隆目的基因,并且在N端带有6XHis。
克隆:
pFastBacTMHT菌株是融合菌株。
为了保证表达重组蛋白,你必须:
*克隆你的基因要带有ATG,位于4050-4052碱基对间。
这个将会产生融合表达,带有6XHis标签,可以用TEV切除
*你的插入要含有终止密码
蛋白翻译能够起始于多克隆位点上游突变的ATG(ATT),尽管如此,从这个位点起始的效率是低的,而且一般不干涉表达和重组蛋白的检测
pFastBacTMHTA的多克隆位点:
下图是pFastBacTMHTA的多克隆位点。
其实ATG用黑体标出。
限制性位点标出来以便显示实际切刻位点。
pFastBacTMHTB的多克隆位点:
框住的核苷酸显示出的是易变区域。
pFastBacTMHTC的多克隆位点:
注意pFastBacTMHTC在XbaⅠ位点有一个终止密码子,他在N端标签框。
确定你的基因的5`端是在XbaⅠ位点上游开始。
克隆进入pFastBacTMDual
pFastBacTMDual包含两个多克隆位点,可以同时表达两个异源基因,一个通过PH启动子控制,另一个通过P10启动子控制。
参见下列建议以便有助于你的基因克隆
克隆事项:
pFastBacTMDual是一个非融合载体。
为了保证重组蛋白的表达,你的插入必须含有以下两点
*一个ATG起始密码子
*如果你不使用多克隆位点中的终止密码子,就必须要有一个终止密码子
对于插入克隆上游的聚乙烯启动子,注意到蛋白翻译能够起始于多克隆位点上游突变的ATG(ATT),尽管如此,从这个位点起始的效率是低的,而且一般不干涉表达和重组蛋白的检测。
PH启动子下游的多克隆位点:
下图是pFastBacTMDual中PH启动子下游的多克隆位点的图示。
限制性位点标记出来显示了实际的切刻位点。
潜在的终止密码子有下划线标出。
P10启动子下游的多克隆位点:
下图是pFastBacTMDual的AcMNPVp10启动子下游的多克隆位点。
限制性位点标记出来以便显示实际切刻位点。
潜在的终止密码子标记下划线。
转化和分析
如果你已经完成了你的连接反应,你就要准备把你的pFastBacTM结构转化进Ecoli了。
很多Ecoli宿主菌和转化程序都是可以使用的。
一般推荐转化Ecoli和分析转化在下面列出
Ecoli宿主:
一旦你把你的插入序列克隆进入了pFastBacTM,你需要转化连接反应到Ecoli,并选择优Amp抗性的转化株。
你可以使用任何recA,endAEcoli菌。
包括Top10,DH10B或者DH5α进行转化。
不要转化连接反应进入DH10Bac细胞。
注意TOP10和DH10B感受态细胞可以从Invitrogen得到
转化方法:
你可以选择使用任何方法对Ecoli进行转化。
化学转化是最便利的方法,而电转对大质粒是最有效的方法。
选择好转化株,使用含有100ug/mlAmp的LB平板。
转化株分析:
一旦你得到Amp抗性转化株,我们有以下推荐:
1、选出10个转化株,在含有100ug/ml的Amp的LB或S.O.B培养基过夜培养
2、使用你选的方法分离质粒DNA。
我们推荐使用公司的试剂盒
3、使用限制性方法分析质粒,证明是重组质粒并证明插入起始的正确。
使用限制性酶或者酶化合物对Vector和插入端各进行一次酶切。
使用PCR对转化株进行分析:
你也可以使用PCR方法对阳性转化株进行分析。
使用合适的PCR引物和Amp条件。
如果你是第一次使用此方法,你最好使用限制性分析作平行试验。
使用错误的引物或污染的平板可能会得到假象。
以下方法可以给你提供便利。
其他方法也是可用的。
需要的材料:
高保真PCRSuperMix,合时的PCR前后引物
过程:
1、对于每个样品,在0.5ml的小离心管加入48ul的高保真PCRSuperMix和各1ul的前后引物。
2、选出10个克隆,在上述离心管中进行重悬(记得做一个Patch板保护克隆以便进行更深的分析)
3、94度10分钟溶解细胞灭活核酸酶
4、20-30个循环进行扩增
5、延伸使用72度10分钟。
4度储存
6、琼脂糖凝胶电泳检测
测序:
对于你的结构需要进行测序证明目的基因是正确的起始以便表达。
如果你是将基因克隆进入了pFastBacTMHT,证明的基因进入了N末端标签的读框中。
长期保存:
一旦你证明了测序的正确,确定克隆的纯度并制作甘油菌长期保存。
推荐储存质粒DNA在-20度
1、在含有100ug/ml的LB平板上对原始的克隆进行划线培养
2、挑单克隆在1-2ml含有Amp的LB抚育
3、培养至稳定期
4、在0.85ml的培养物中混合0.15ml的过滤甘油,转到冷冻小管
5、-80度储存
重组质粒的产生
转化到DH10BacEcoli
一旦你有了你的pFastBacTM结构,你就可以准备转化纯化的质粒DNA进入DH10BacTMEcoli,转变成为杆粒。
你可以使用蓝/白斑选出含有重组杆粒的克隆。
Bac-toBac表达系统提供高效DH10BacTM感受态细胞。
阳性对照:
每个pFastBacTM质粒都提供相应的阳性对照用来作为阳性转染和表达对照(下表)。
根据pFastBacTMVecctor的使用,我们推荐在你的DH10Bac转染试验中作相应的对照。
所需材料:
开始之前你需要有以下材料
*纯化的pFastBacTM结构(200pg/ul储存于PH8.0的TE)
*阳性表达对照
*高效DH10BacTM感受态细胞(表达系统提供,每个转化试验使用1管细胞)
*pUC19(与DH10Bac一起提供,用来做对照)
*LB平板,包含Kan,Gen(庆大),Tetracycline(四环素),Bluo-gal(卤代吲哚基-beta-D-半乳糖苷)和IPTG。
(每个转化3个板,使用新鲜平板,推荐见下文)
*LB板含有100ug/mlAmp(用于pUC19转化对照)
*S.O.C介质
*15ml圆底塑料管
*42度水域和37度摇床及37度培养箱。
你需要准备LB琼脂糖平板,包含50ug/mlKan,7ug/mlGentamicin,10ug/mltetracycline,100ug/mlBiuo-gal,40ug/mlIPTG,用来进行DH10BacTM转化株的筛选。
可以从我公司预订抗生素,Bbluo-gal,IPTG,在后面有制备平板的指导。
如果你正准备的LB平板使用的是事先混合好的,我们推荐使用LuriaBrothBase代替LB。
使用LB板将会降低颜色敏感度,并可能降低克隆的数量。
在蓝/白斑筛选中使用Bluo-gal代替X-Gal。
Bluo-gal产生的蓝斑颜色要比X-Gal深。
准备转化:
对于每个转化,你都需要一小瓶感受态细胞和三个平板。
*42度水域平衡*37度烘板30分钟*室温放置SOC介质*对于每个转化试验预冷一个15ml管子
转化过程:
按照以下过程用高效DH10BacTM感受态细胞转化pFastBacTM结构。
我们推荐做阳性对照的转化来帮助你证明你的结果。
1、整管高效DH10BacTM感受态细胞冰上解冻。
2、每个转化试验,轻轻地混合,将100ul高效DH10BacTM感受态细胞倒入预冷的15ml管子
3、向细胞中加入适量的质粒DNA,轻轻混合。
千万不要上下吹吸混合
*pFastBacTM结构:
1ng(5ul)
*pFastBacTM对照质粒:
1ng
*pUC19对照:
50pg(5ul)
4、冰上抚育30分钟
5、42度热激45秒
6、立即冰上2分钟
7、加入900ul室温的SOC培养基
8、pFastBacTM转化:
37度225转震荡培养4小时。
pUC19转化:
37度225转震荡培养1小时
9、对于每个pFastBacTM的转化:
准备10折连续(不知道什么意思)用SOC稀释的细胞(10-1,10-2,10-3),每个稀释用100ul铺一个LB平板,平板包含50ug/mlKan,7ug/mlGentamicin,10ug/mltetracycline,100ug/mlBiuo-gal,40ug/mlIPTG。
对于pUC19转化:
用SOC培养基1:
100稀释细胞,铺100ul稀释物在含有100ug/mlAmp的LB平板。
10、37度抚育48小时。
分析筛选的克隆(参见推荐)。
我们不推荐早于48小时挑单克隆,因为这样可能会难于区分蓝白斑。
微型Tn7插入到微型attTn7附属位点会干扰LacZa肽的表达,所以包含重组质粒的克隆在蓝色背景下是白色的,可能隐藏在未改变的质粒中。
选择白斑分析。
真正的白斑克隆比较大;
因此为了避免选择成假阳性,选择最大的,最独立的白斑。
避免挑出现灰色的或者在中间的菌落,因为他们可能是包含空质粒的细胞核重组细胞的混合。
验证显性:
1、挑10个白色的克隆,重新划线在新鲜LB平板(50ug/mlKan,7ug/mlGentamicin,10ug/mltetracycline,100ug/mlBiuo-gal,40ug/mlIPTG)。
37度过夜培养。
2、在包含Bluo-Gal和IPTG的重新划线的平板上选出单克隆证明是白色的显性,嫁接至有50ug/mlKan,7ug/mlGentamicin,10ug/mltetracycline的液体中
3、使用我公司的试剂盒抽提重组质粒DNA。
选择性的,你可以使用附录提供的操作步骤。
这个过程源于抽提大的质粒DNA(>100kb),适用于分离质粒DNA。
4、分析重组质粒DNA证明成功转化到了杆粒中。
我们推荐使用PCR分析杆粒DNA。
注意:
适用琼脂糖凝胶电泳可以证明转化的成功与否,他可以分出高分子量的DNA。
这个方法要比PCR分析可信度低,因为高分子量DNA是很难见到的。
使用PCR分析重组质粒
重组杆粒DNA要大于135kb。
既然限制性分析很难完成这么大的DNA分析,我们推荐使用PCR分析鉴定重组杆粒中的目的基因。
杆粒包含M13正负引物位点,位于LacZa互不区域的微型attTn7位点两侧,可以完成PCR检验。
本节提供使用M13引物的PCR检验指导。
使用M13引物进行PCR分析:
使用PCR法证明你的目的基因在重组杆粒中,你可能会:
*使用M13Forward(-40)和M13Reverse引物
*使用M13Forward(-40)或M13Reverse引物于你的插入片段杂交成联合物
DNA聚合酶:
你可能会使用任何DNA聚合酶在你的PCR试验中,包括PlatinumTaq酶。
如果希望PCR产物>4kb,我们推荐使用聚合酶混合物。
例如高保真的PlatinumTaq酶
得到PCR产物:
使用下面过程扩增重组杆粒DNA,适用M13正反引物和PlatinumTaq酶。
如果你使用M13F或M13R与一个你的基因特意引物混合,你需要自己决定扩增的条件。
如果你使用其它的聚合酶,依照供应商提供的建议。
如果你的插入片段>4kb扩增条件需要被优化.
1、每个样品,在0.5ml微型管子中装入50ul的量进行PCR反映
重组杆粒DNA(100ng)1ul
10XPCRBuffer5ul
10mMdNTPMix5ul
50mMMgCl21.5ul
PCR引物(1.25ul/10uM)2.5ul
蒸馏水38.5
总体积50ul
2、一滴矿物油覆盖
3、一下参量进行扩增
4、从反应产物吸取5-10ul进行琼脂糖电泳分析
你将会看到:
如果转化发生了,而且你使用的是M13正负引物扩增,你将会在电泳上看到下列PCR产物大小
如果你使用的是M13和你的特异引物进行的扩增,你需要决定PCR产物是否是希望的。
12页的图有助于你计算。
重组杆状病毒的产生
转染昆虫细胞:
一旦你证明了你的重组杆粒含有你的目的基因,就可以准备进行昆虫细胞的转染了,以产生重组杆状病毒。
本章提供指导和建议以便完成昆虫细胞的转染
准备质粒:
你可以使用任何方法准备纯化的重组杆粒DNA。
杆粒DNA必须没有酚和NaCl的污染,他们会杀死细胞,盐类会干扰脂类复合物,降低转染效率。
我们推荐使用本公司产品提质粒。
转染方法:
推荐使用一个阳离子脂质体,例如Cellfectin试剂进行转染。
此试剂用来提供给表达系统使用。
Cellfectin试剂:
不做翻译
昆虫细胞系:
推荐使用Sf9和Sf21进行转染。
HighFive™andMimic™Sf9不推荐因为他们转染效率低下。
不过,如果你有了你的杆状病毒株,你可以进行HighFive™andMimic™Sf9表达试验。
转染介质:
为了高效的转染,我们推荐在无Grace的昆虫细胞培养基中完成转染。
注意Grace的昆虫细胞培养基应该不含有FBS(血糖),因为蛋白在血糖和其补充物中会与Cellfectin试剂互作,影响转染。
如果你在Sf-900ⅡSFM中收获了Sf9或Sf21,你可以在不含有Grace的培养基中完成转染,转染后可以容易的将Sf-900ⅡSFM转变回去
如果你有了从pFastBac对照质粒中得到的重组杆粒,我们推荐,包括这个阳性对照在你的试验中和转化中能够评估你的结果。
在这些杆粒中,包括β-葡糖甘酶(Gus)和/或氯霉素乙酰转移酶(CAT)将会在PH或者P10启动子控制下表达。
在转染过后,表达的Gus和CAT可以适当进行验证。
开始之前需要有下列材料:
*从pFastBacTM结构(500ng/ulTE溶解,PH8.0)中纯化的重组杆粒DNA
*从合适的pFastBacTM对照结构中纯化的重组杆粒DNA
*合适培养基收获的Sf9或者Sf21
*Cellfectin试剂(4度保存)
*G