辽宁省版九年级下学期学生竞赛化学试题A卷Word格式文档下载.docx
《辽宁省版九年级下学期学生竞赛化学试题A卷Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《辽宁省版九年级下学期学生竞赛化学试题A卷Word格式文档下载.docx(10页珍藏版)》请在冰豆网上搜索。
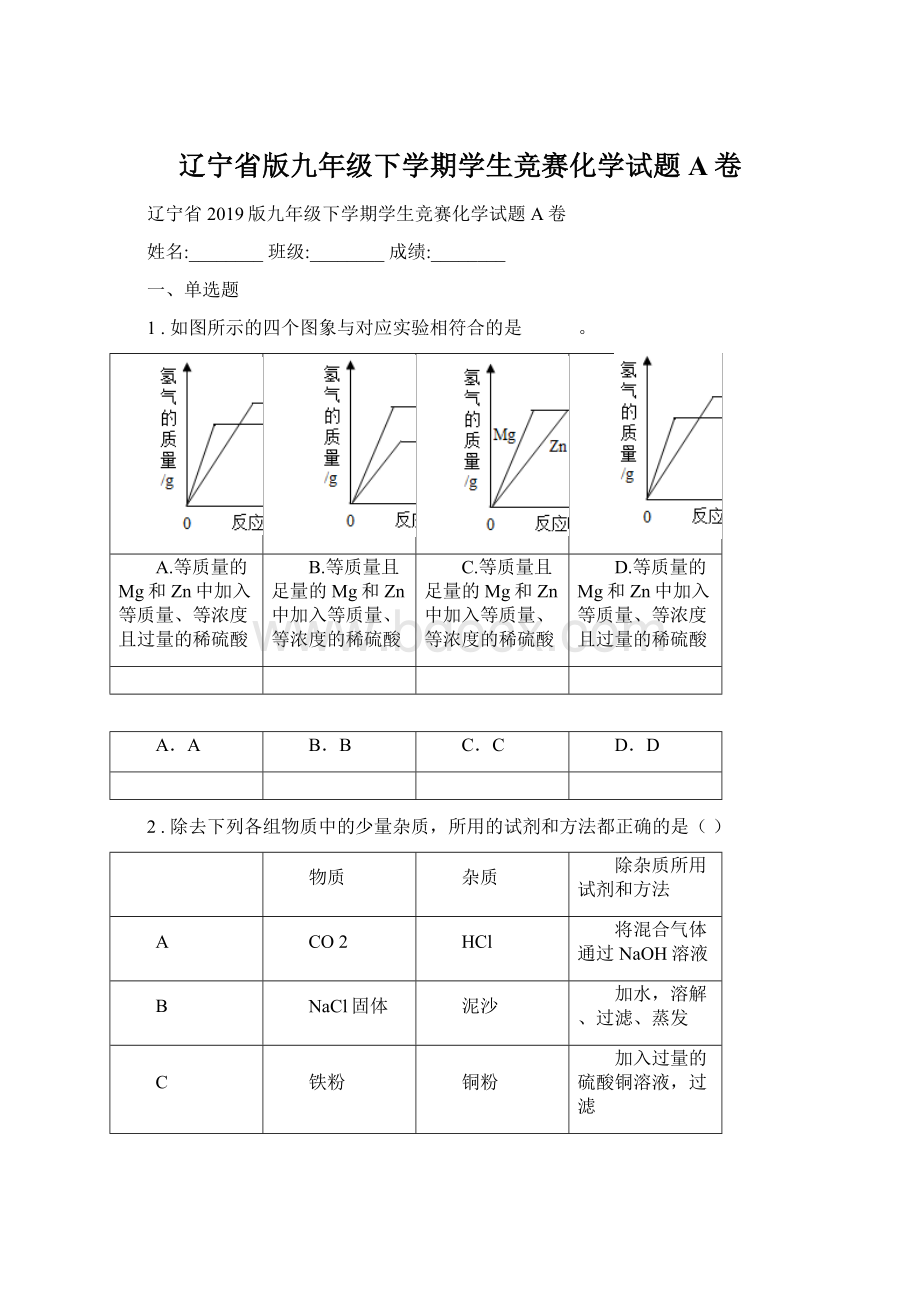
HCl
将混合气体通过NaOH溶液
B
NaCl固体
泥沙
加水,溶解、过滤、蒸发
C
铁粉
铜粉
加入过量的硫酸铜溶液,过滤
D
Na2SO4溶液
H2SO4溶液
加入适量BaCl2溶液
3.将一定量的Zn放入100g稀硫酸恰好反应,得到112.6g溶液,则稀硫酸的质量分数为()
A.9.8%
B.19.6%
C.10%
D.无法确定
4.已知:
Mg(OH)2
MgO+H2O.一定质量的Mg(OH)2和MgO的混合物加热一段时间后,将生成的气体通入到浓硫酸中,增重1.8g,已知剩余固体的质量为13.8g,剩余固体中Mg元素的质量为7.2g,下列说法错误的是()
A.剩余固体为混合物
B.原混合物中Mg元素的质量为7.2g
C.混合物中Mg(OH)2与MgO的质量之比为29:
20
D.加热前后的固体分别与相同浓度稀盐酸恰好完全反应所消耗盐酸质量相等
5.按下图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是
A.甲:
NaHCO3、稀HCl;
乙:
NaOH溶液
B.甲:
Al、稀H2SO4;
Ba(NO3)2溶液
C.甲:
MgO、稀盐酸;
AgNO3
D.甲:
Cu、稀H2SO4;
BaCl2溶液
6.向某硫酸和硫酸铜的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示,下列说法正确的是()
A.加入氢氧化钠溶液的溶质质量分数为20%
B.
点溶液中含有两种溶质
C.
段发生的反应为中和反应
D.混合溶液中硫酸和硫酸铜的质量比为1∶1
7.在2.48gNa2CO3和Na2SO4的混合物中,加入足量的BaCl2溶液,得到沉淀4.3g,在此沉淀中加入足量的硫酸,沉淀的质量变为4.66g,则2.48g混合物中Na2CO3的质量分数是()
A.24.7%
B.42.7%
C.37.9%
D.32.6%
8.一定质量的硫铁矿(主要成分是FeS2),高温灼烧发生如下反应(杂质不参加反应):
4FeS2+11O2
8SO2+2Fe2O3,生成的SO2经过一系列反应全部变成H2SO4,把生成的H2SO4稀释后加入足量BaCl2溶液完全反应生成4.66t的沉淀,则硫铁矿中FeS2的质量为
A.1.2t
B.2.28t
C.1.28t
D.2.4t
9.对有关实验现象的描述正确的是()
A.木炭在空气中燃烧,发出白光
B.红磷在空气中燃烧,产生大量白雾
C.铁钉放入硫酸铜溶液中,铁钉表面覆着一层红色物质
D.硫在氧气中燃烧发出淡蓝色的火焰
10.将过量的铁粉投入硫酸和硫酸铜的混合溶液中,充分反应后过滤,滤出剩余的铁和生成的铜,在滤液里含有的溶质是()
A.FeSO4
B.CuSO4
C.Fe2(SO4)3
D.H2SO4
二、填空题
11.写出下列化学方程式,并简答有关内容:
化学反应
化学方程式
简
答
铁丝在氧气中燃烧
___________________
反应类型__________
煅烧石灰石
__________________
镁带在空气中燃烧
生成物状态_______
硫酸铜和氢氧化钠溶液混合
产生_____色沉淀
12.向盛有一定质量AgNO3和Cu(NO3)2的混合溶液中的烧杯中逐渐加入Zn粉,并边加边搅拌,溶液质量与加入Zn的质量关系如下图所示。
﹙1﹚a点的溶液中含有的溶质有_______种。
﹙2﹚写出b~c(不包括b点)段反应的化学方程式___________________。
﹙3﹚d点的固体中含有____________。
13.现有一包白色固体样品,可能含有BaCl2、Na2SO4、Na2CO3、NH4HCO3、KCl、CuSO4中的一种或几种,取样品进行如下实验:
(1)B的化学式为__________________________________。
(2)原白色固体中可能含有什么物质?
三、推断题
14.A-G是初中化学常见的物质,其中A为难溶性钙盐,B为酸,G为微溶性碱,D为气体单质,C、E、F为氧化物,H是一种有机化合物。
已知各物质间能发生下图所示的系列变化:
请回答:
(1)反应①的化学方程式____________________________________。
(2)反应②的基本反应类型____________________________________。
(3)反应③的一条用途____________________________________。
(4)反应④的能量转化____________________________________。
四、科学探究题
15.某班同学在学习了铁的冶炼后,欲探究炼铁高炉气体中有害气体的成分。
于是他们分成甲乙两个小组,收集炼铁高炉不同时间段的气体进行探究。
回答下列问题。
已知:
高炉气体中一定含有二氧化碳、氮气、极少量的氧气、稀有气体等,还可能含有一氧化碳、二氧化硫等有害气体。
[提出问题]高炉气体中的有害成分是什么?
[作出猜想]猜想一:
只有CO;
猜想二:
只有SO2;
猜想三:
CO和SO2都有。
甲实验小组
[查阅资料]SO2与CO2具有许多相似的化学性质:
①都能与水反应。
(亚硫酸);
②SO2也能使澄清石灰水变浑浊,生成亚硫酸钙(CaSO3)白色沉淀;
③都能与氢氧化钠溶液反应,分别生成可溶性的碳酸钠、亚硫酸钠(Na2SO3)和水。
不同之处:
二氧化硫能使红色品红溶液褪色,可被酸性高锰酸钾溶液吸收。
[实验探究]甲组同学设计组装如下装置进行实验。
(1)A中品红溶液的作用是检验二氧化硫,B中酸性高锰酸钾溶液的作用是_____,C中品红溶液的作用是_____。
(2)观察现象发现:
A中品红溶液褪色,C中品红溶液不褪色,E中澄清石灰水变浑浊。
得出结论:
高炉气体中含有SO2和CO。
反思评价:
部分同学认为上述结论不够准确,理由是_____。
[实验改进]同学们经过讨论后,在原有基础上改进了实验装置,如下图所示。
(3)用氢氧化钠溶液代替酸性高锰酸钾溶液的优点是_____,写出二氧化硫与氢氧化钠溶液反应的化学方程式_____。
乙实验小组
[查阅资料]一氧化碳能与红色氯化钯(PdCl2)溶液反应,生成黑色的金属钯(Pd)沉淀、盐酸和二氧化碳。
[实验探究]乙组同学设计如下实验装置并进行实验。
(4)B中反应的化学方程式为_____,结合已有知识和该反应可以判断:
金属钯的活动性比铁_____,(填“强”或“弱”)。
[实验结论]炼铁厂排放的高炉气体中含有CO和SO2,直接排放会造成大气污染,需净化达标后才能排放。
[延伸拓展]二氧化硫排放到空气中会导致酸雨。
二氧化硫与水反应生成亚硫酸,亚硫酸会被氧气进一步氧化生成硫酸。
为了研究酸雨的危害,同学们设计了如下实验探究:
②将硫燃烧的产物溶于水后,通入氧气,用所得溶液模拟硫酸型酸雨。
②模拟实验如下:
实验序号
所加物质
实验现象
1
树叶、果皮
树叶、果皮被腐蚀
2
细铁丝、镁条
产生气泡
3
石灰石、大理石碎片
实验结论:
酸雨具有较强的危害性。
(5)实验室制取二氧化碳时,不能使用大理石与稀硫酸反应,但硫酸型酸雨却能腐蚀大理石雕像,其原因是_____。
(6)同学们经过讨论认为,酸雨还会加剧“温室效应”。
这种说法的依据是_____。
16.红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”。
其标签如图所示,某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究。
品名:
504双吸剂
成分:
铁粉、生石灰等
(提出问题):
久置固体的成分是什么?
(查阅资料):
铁与氯化铁溶液在常温下发生反应:
Fe+2FeCl3=3FeCl2打开固体包装观察:
部分固体呈黑色,部分固体呈白色,另有少量红棕色的块状固体。
(作出猜想):
久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
其中可能含有Fe2O3的依据是_____________。
(实验探究):
甲同学的方案:
实验操作
实验结论
(1)取少量久置固体于试管中,滴加足量的蒸馏水,搅拌
固体溶解,试管外壁发烫
固体中一定含有______
(2)过滤,在滤液中滴加无色酚酞溶液
溶液变红色
固体中一定含有氢氧化钙
(3)取滤渣放入试管中,滴加足量的________
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液
固体中一定含有______,一定不含氧化铁
(实验质疑)乙同学认为甲同学在实验中得出“一定不含氧化铁”的结论是错误的,理由是______________。
你认为甲同学哪一步实验操作得出的结论也不合理:
__________,理由是___________(用化学方程式表示。
)
(继续探究)乙同学另取久置的固体进行实验探究:
乙同学对滤渣B进行探究:
取滤渣B于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水
固体逐渐消失、______有气泡冒出、______
固体中一定含有CaCO3和Fe2O3。
写出Fe2O3和稀盐酸反应的化学方程式_______
(计算得出结论):
如上述实验流程,乙同学现取5g久置固体研碎,用磁铁吸引,得残留固体3g,加足量水充分溶解过滤,得滤渣B的质量为1.8g。
在滤液A中加足量碳酸钠溶液后过滤得滤渣C的质量为2g,通过计算后得出残留固体的成分为:
__________。
五、计算题
17.有一份铜锌合金粉末样品(设只含铜、锌),为认识其组成等,某学习小组进行了以下探究,请参与并完成有关计算:
(1)取样品20g,和足量稀硫酸充分混合,待反应完全后过滤,将滤渣洗涤,干燥后称得其质量为13.5g。
该样品中铜的质量分数为______。
(2)再取三份不同质量的样品,分别加入到三份100g相同浓度的硫酸溶液中,充分反应后,测得的数据如下表:
①
②
③
样品的质量/g
10
30
生成气体的质量/g
0.1
0.2
0.25
试计算所用硫酸溶液的溶质质量分数(写出计算过程,结果精确到0.01%)。
_______