北京市届初三专题复习各城区一模化学试题分类汇编生产实际分析word版含答案文档格式.docx
《北京市届初三专题复习各城区一模化学试题分类汇编生产实际分析word版含答案文档格式.docx》由会员分享,可在线阅读,更多相关《北京市届初三专题复习各城区一模化学试题分类汇编生产实际分析word版含答案文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
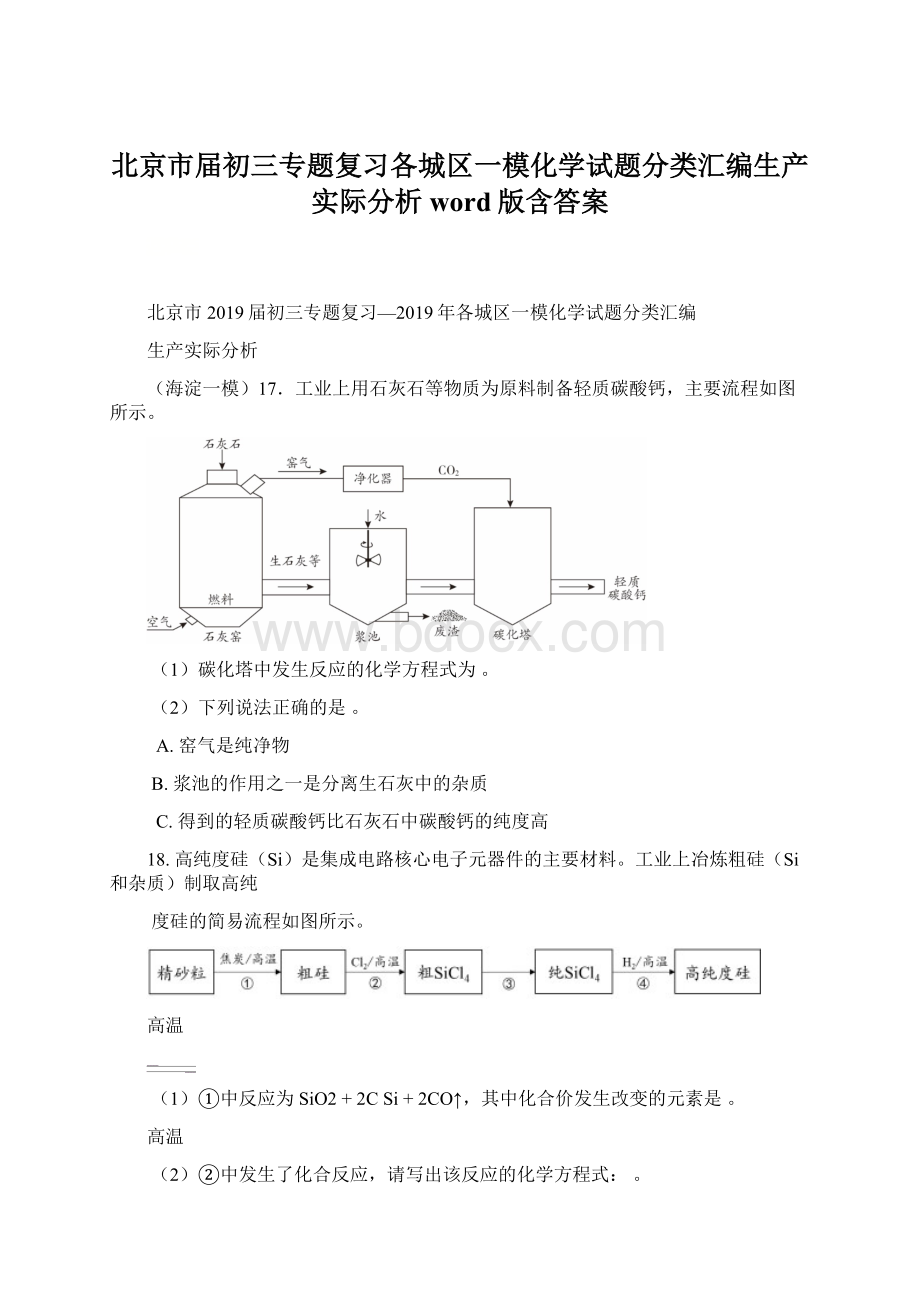
(1)“燃烧室”中CH4燃烧的作用是。
(2)整个流程中,化合价发生改变的元素有种。
(3)若用CO还原含160tFe2O3的赤铁矿,则炼出铁的质量为 t。
(东城一模)17.工业上用菱锰矿[主要成分为MnCO3,含FeCO3、Cu2(OH)2CO3、SiO2等杂质]为原料
来制取二氧化锰,其生产流程示意图如下:
回答下列问题:
(1)将滤液与滤渣分离的操作是。
(2)向菱锰矿中加入盐酸,MnCO3、FeCO3、Cu2(OH)2CO3都溶解并转化为MnCl2、FeCl2、CuCl2。
盐酸与MnCO3反应的化学方程式为。
(3)加入生石灰将溶液pH调至4,此时溶液呈(填“酸性”或“碱性”)。
(4)加入双氧水将铁元素转化为Fe(OH)3沉淀,其反应为:
2FeCl2+H2O2+4H2O=2Fe(OH)3↓+4HCl,该反应化合价发生变化的元素是氧和。
(5)加入Na2S、MnS等硫化物,均可将MnCl2中混有的CuCl2转化为CuS沉淀除去,但实际生
产中选用MnS,其原因是。
(西城一模)17.SCR技术可降低柴油车尾气中氮氧化物的排放,部分转化过程如下:
催化剂
(1)反应
为化合反应,反应前后化合价发生改变的元素是______。
(2)反应
为:
4CO(NH2)2+6NO2=====4CO2+7N2+8H2O。
若使用60kgCO(NH2)2,可消耗NO2的质量为______kg。
18.为保护绿水青山,可将工业含铜废酸液(主要成分为CuSO4和H2SO4)进行无害化处理,制取硫酸钡(BaSO4)和硫化铜(CuS)。
主要流程如下:
资料:
BaSO4、CuS难溶于水且不与稀硫酸反应;
Cu(OH)2难溶于水,可与稀硫酸反应。
(1)反应釜1中需不断搅拌,其目的是______。
(2)从过滤器中分离出滤渣的成分为______。
(3)反应釜3中发生复分解反应的化学方程式为______。
(丰台一模)17.由钛精矿(主要成分为TiO2)制备纯TiCl4的流程示意图如下:
已知:
TiCl4中钛元素的化合价为+4。
点燃
(1)流程中,蒸馏塔的作用是。
(2)沸腾炉中发生了反应TiO2+2Cl2====TiCl4+O2,其中化合价发生改变的元素是。
18.化学链燃烧是一种绿色的、高效的燃烧方式,燃料不直接与空气接触。
下图是某科研组利用金
属镍(Ni)进行化学链燃烧的流程图:
(1)空气反应器中,Ni在一定条件下转化成NiO的化学方程式为。
(2)燃料反应器中发生的部分化学反应如下:
Ⅰ.H2+NiO
Ni+H2O;
Ⅱ.CO+NiO
Ni+CO2,
其中属于置换反应的是(填“Ⅰ”或“Ⅱ”)。
(3)该流程中可以循环利用的物质是 。
(房山一模)绿水青山就是金山银山,发展科技的同时要注重保护环境。
17.氢气是最理想的清洁能源,煤制氢是目前解决大规模氢来源的重要途径。
煤制氢过程中发生的主要反应为:
①C+H2O====CO+H2②CO+H2O====CO2+H2
(1)上述反应中的各物质,碳元素呈现种化合价。
(2)从上述反应①或②中任选一个,在下列两个方框中补全其反应物和生成物相应微粒的图示。
18.氨法脱硫可防治二氧化硫(SO2)污染,同时制得化肥(NH4)2SO4。
(1)吸收塔中,氨水采用喷淋方式注入,其目的是。
(2)吸收塔中发生的反应为:
2NH3+H2O+SO2====(NH4)2SO3,若利用此反应吸收64kg二氧化硫,则参加反应的氨气(NH3)的质量为kg。
(3)氧化塔中通入氧气的目的是将(NH4)2SO3转化为___________。
(顺义一模)烟道气无害化处理是保护绿水青山的重要措施。
回答17-18题。
17.烟道脱硫的工艺不仅能消除SO2,还能将其转化为石膏(CaSO4·
2H2O)等产品,实现“变废为宝”。
主要物质转化关系如下:
的基本反应类型是__________。
中化合价发生变化的元素有__________。
(3)下列说法正确的是_________。
a.为更好的脱硫应使用石灰石粉末
b.反应
为复分解反应,有CO2生成
c.脱硫后的烟气对环境无害
18.烟道气中的CO2经“捕捉”可用于甲醇(CH3OH)。
反应的微观示意图如下:
(1)上述物质中,属于氧化物的是__________。
(2)用该方法生产16吨甲醇,消耗二氧化碳的质量为。
(石景山一模)17.许多制药厂、化工厂在生产中会产生大量的铁泥(主要含Fe,FeO,Fe2O3等物质),若以铁泥为原料制备FeSO4·
7H2O,可实现废物利用。
其主要流程如下。
已知:
FeO+H2SO4===FeSO4+H2O;
Fe+Fe2(SO4)3===3FeSO4
(1)酸浸过程中铁发生反应的化学方程式为______。
(2)还原过程中,元素化合价发生改变的是。
(3)产品在结晶前需要调节pH。
若pH过高需要加入______进行调节。
18.中科院大连化学物理研究所研制出新型多功能复合催化剂,可将二氧化碳转化为汽油,过程示意如下图。
(1)X是一种单质,该物质是______。
(2)在一定条件下,I中反应生成的另外一种物质为生活中常见的化合物,该反应的化学方程式为______。
(门头沟一模)18.近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与储存。
过程如下:
(1)反应Ⅰ的化学方程式为。
(2)反应Ⅲ为S+O2====SO2,其中化合价发生改变的元素是。
19.中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%。
工业上利用钛白粉制备海绵钛的工艺流程如下:
(1)反应Ⅱ发生置换反应生成海锦钛,则物质X的化学式为。
(2)反应Ⅲ属于基本反应类型中的反应。
(3)该工艺流程中,可以循环使用的物质有。
(平谷一模)17.近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。
(1)反应Ⅱ中化合价发生变化的元素是。
(2)反应Ⅲ属于基本反应类型中的。
18.某化工厂利用含有1%—2%BaCO3的废料制取BaCl2(废料中其他物质不溶于水和稀盐酸、且不与稀盐酸反应,重金属对环境有一定的污染)。
其部分流程如下:
(1)步骤Ⅱ中发生的化学反应是(化学方程式表示)
(2)步骤Ⅲ的操作名称是
(延庆一模)17.烟道气中含有大量CO2,经“捕捉”可用于生产尿素、甲醇等产品。
(1)检验烟道气中CO2的方法是(用化学方程式表示)。
(2)用“捕捉”的CO2生产甲醇(CH3OH)。
生产32千克甲醇需要乙的质量为千克。
18.工业上用黄铁矿(主要成分是FeS2)制备硫酸,主要流程如下:
(1)向沸腾炉中加入黄铁矿时需要将矿石粉碎,目的是________________________。
(2)接触室里的反应中,化合价升高的元素有_______________。
(3)吸收塔中生成硫酸的化学方程式为_______________________________。
(密云一模)17.高纯氧化铁[Fe2O3]又称“引火铁”,在现代工业上有广泛应用前景。
以下是用赤铁矿(含少量不溶于水的SiO2等)为原料,制备高纯氧化铁的生产流程示意图。
小贴士:
氨水呈碱性(主要成分NH3•H2O是一种碱);
(NH4)2CO3溶液呈碱性,40℃以上易分解。
(1)①处发生反应的化学方程式为____________。
(2)加入(NH4)2CO3后,该反应必须控制的条件是________。
18.“打好蓝天保卫战、治理大气污染”是提升人民生活质量的重要工作。
二氧化硫(SO2)是一种大气污染物。
工业上可以利用海水对二氧化硫进行吸收利用,变害为宝。
其工艺流程见图:
(1)流程中将石灰石加水制成石灰石浆的目的是_________。
(2)其中硫元素的化合价在反应前后的变化为___________。
.
(3)为了提升脱硫率(脱硫率是指已除去的二氧化硫的量占总二氧化硫量的百分比)
与温度、烟气中SO2浓度的关系,技术人员进行了探究实验。
实验结果如下:
实验序号
温度/℃
烟气中SO2浓度/10-2g•L-1
脱硫率
Ⅰ
23
2.5%
99.5
Ⅱ
3.2%
97.1
Ⅲ
40
94.3
由表中实验数据可得出的结论是_______________。
(通州一模)17.工业制备蔗糖的流程如下图所示。
(1)操作A名称是________。
(2)关于工业制备蔗糖,下列说法正确的是________(选填序号)。
A.由甘蔗制得蔗糖的整个过程中主要是物理变化
B.在实验室中进行操作A、C都要用到玻璃棒,其作用不同
C.为得到更多的蔗糖固体,进行操作C时应将水分蒸干再停止加热
18.工业烟气脱硫中采用“双碱法”脱硫的工业流程如下:
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水,则Na2SO3中硫元素的化合价为______。
(2)沉淀室中发生了复分解反应,请写出此反应的化学方程式。
(燕山一模)17.
某兴趣小组在实验室中模拟炼铁的化学原理,用一氧化碳还原氧化铁粉末,分别设计A、B套实验装置
AB
(3)澄清石灰水变浑浊原因(用化学方程式表示)。
(4)从保护环境和节约能源的角度来说,你认为装置(填A、B)更合理。
(怀柔一模)17.燃油汽车安装的触媒转换器可以将有害气体转化成无害气体,其过程可表示如下:
(1)触媒转换器可以将等有害气体转化为无害气体。
(2)在转化过程中化合价变化的元素是。
18.工业上生产高纯度CaO的主要流程示意图如下:
(1)反应釜中发生反应的反应类型是______。
(2)若进入焙烧炉内的碳酸钙是500kg,理论上能生产出kg氧化钙。
生产实际分析参考答案
(海淀一模)
17.
(1)Ca(OH)2+CO2CaCO3↓+H2O
(2)BC
18.
(1)Si、C
(2)Si+2Cl2SiCl4
(3)4
(朝阳一模)17.
(1)置换反应
(2)CO、CO2
18.
(1)提供高温条件
(2)4
(3)112
(东城一模)17.
(1)过滤
(2)MnCO3+2HCl=MnCl2+CO2↑+H2O
(3)酸性
(4)铁(或Fe)
(5)除杂不引入新的杂质
(西城一模)17.
(1)N、O
(2)69
18.
(1)使反应物充分接触,加快反应速率
(2)BaSO4
(3)CuSO4+H2S===CuS↓+H2SO4
一定条件
(丰台一模)17.
(1)分离提纯TiCl4
(2)Cl和O
△
18.
(1)2Ni+O2====2NiO
(2)Ⅰ(3)Ni
(房山一模)17.
(1)3
(2)略
18.
(1)增大反应物间接触面积,使反应更充分
(2)34(3)(NH4)2SO4
(顺义一模)17.
(1)化合反应
(2)O、S(3)ab
18.
(1)AD
(2)22吨
(石景山一模)17.
(1)Fe+H2SO4==FeSO4+H2↑
(2)Fe(或Fe和H)(3)硫酸
18.
(1)H2
(2)CO2+H2一定条件CO+H2O
(门头沟一模)18.
(1)2H2SO4===2SO2↑+2H2O+O2↑
(2)S、O
19.
(1)Mg
(2)分解反应(3)Mg、Cl2
(平谷一模)17.
(1)S
(2)化合
18.
(1)2HCl+Ba(OH)2===BaCl2+2H2O
(2)过滤
(延庆一模)17.
(1)CO2+Ca(OH)2==CaCO3↓+H2O
(2)6
18.
(1)增大矿石与空气的接触面积,使反应更充分
(2)S(3)H2O+SO3==H2SO4
(密云一模)17.
(1)Fe+H2SO4==FeSO4+H2↑
(2)温度低于40℃,容器内呈中性或碱性
18.
(1)增大接触面积,使反应更易发生
(2)+4变为+6
(3)浓度相同的情况下温度越高脱硫率越低;
或在温度相同的情况下,SO2的浓度越高脱硫率越低
(通州一模)17.
(1)过滤
(2)AB
18.
(1)+4
(2)Ca(OH)2+Na2SO3=CaSO3↓+2NaOH
(燕山一模)17.
(1)略
(2)N2CO2CO(3)方程式略(4)B
(怀柔一模)17.
(1)CO、NO、NO2
(2)C、N
18.
(1)复分解反应
(2)280