铁盐沉淀法从马铃薯渣中提取果胶工艺的研究Word格式文档下载.docx
《铁盐沉淀法从马铃薯渣中提取果胶工艺的研究Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《铁盐沉淀法从马铃薯渣中提取果胶工艺的研究Word格式文档下载.docx(17页珍藏版)》请在冰豆网上搜索。
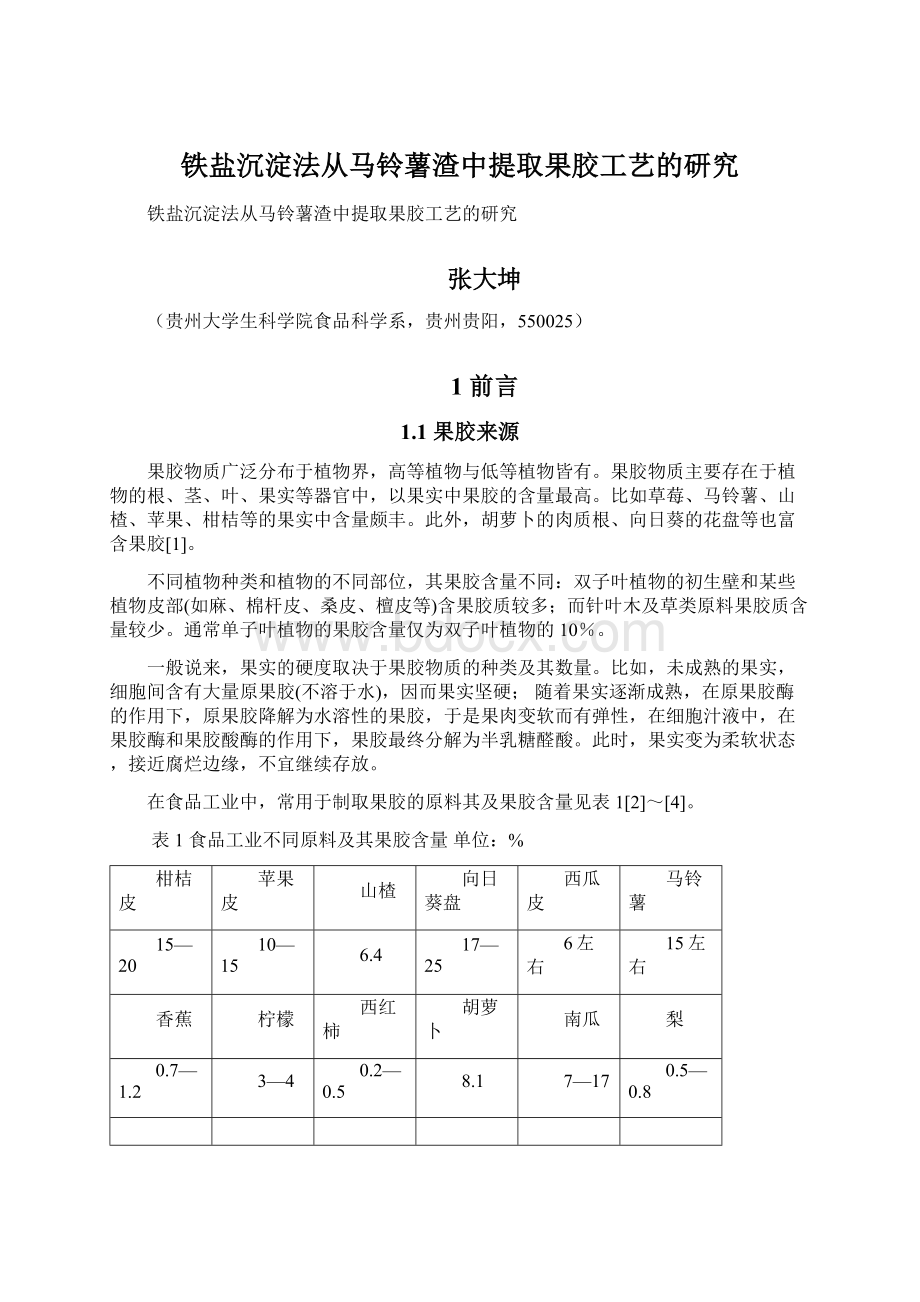
17—25
6左右
15左右
香蕉
柠檬
西红柿
胡萝卜
南瓜
梨
0.7—1.2
3—4
0.2—0.5
8.1
7—17
0.5—0.8
1.2果胶的化学结构及基本特性
1.2.1果胶的化学结构
果胶物质是一种多糖类高分子化合物,其结构单元为D一吡喃半乳糖醛酸以1,4等键连接成长链状通常以部分甲醇化状态存在。
在果胶类物质的主链上还连有其它糖类,包括L一阿拉伯糖、D一半乳糖、D一山梨糖、L一鼠李糖,分子量为1~40万[2]。
果胶物质通常以原果胶、果胶酯酸、果胶酸的形态广泛存在于植物的果实、根、茎、叶中,是细胞壁的一种组成成分,它们伴随纤维素而存在,构成相邻细胞中间层粘结物,使植物组织细胞紧紧粘结在一起。
原果胶是指果胶物质相互间或他与半纤维及钙盐以机械方式或化学方式相结合,形成一种不溶于水的物质,在酶的作用下或在水或酸性溶液中加热时,转变为果胶酯酸。
果胶酯酸是指被甲基酯化了的多聚半乳糖醛酸,当酯化程度为100%时,甲氧基(CH3O—)含量为16.32%,称完全甲基化了的果胶脂酸。
甲基含量大于7%的称高甲氧基果胶,果胶含量小于7%的称低甲氧基果胶(又称低酯果胶)。
果胶酯酸与糖、酸在适当的条件下能形成凝胶,是良好的稳定剂。
果胶酸是甲氧基含量少于1%的果胶,果胶酸的基本结构为聚半乳糖醛酸,它的游离羧基能与金属离子形成正盐或酸式盐[3]。
1.2.2果胶的基本特性
1.2.2.1果胶物质的溶解性
纯品果胶物质为白色或淡黄色的粉末,略有特异气味。
在20倍的水中几乎完全溶解,形成一种带负电荷的粘性胶体溶液:
但不溶于乙醚、丙酮等有机溶剂。
如果用蔗糖糖浆或与3倍以上砂糖混合则更易溶于水。
一般认为,果胶及果胶酸在水中的溶解度与自身的分子结构有关:
一是随链的增长而降低;
二是随酯化程度的增大而升高,(其衍生物甲酯、乙酯较易溶于水)。
其原因可能是,果胶物质的分子不是以直线形存在,而是多呈折叠形式,极易形成分子内氢键;
而酯化程度较高时,分子内氢键相对减弱,因此溶解反会有一定的增加。
1.2.2.2果胶物质的酸碱性
在不加任何试剂的条件下,果胶物质水溶液呈酸性,主要是果胶酸和半乳糖醛酸。
因此,在适度的酸性条件下,果胶稳定。
但在强酸与强碱作用下,易引起果胶分子降解,使长链变成短链。
1.2.2.3果胶物质的凝胶性
果胶物质最重要的性质就是凝胶化作用。
由于果胶溶液具有很高的粘度,故在一定温度下,当果胶、糖、酸的比例适宜时,就会形成凝胶,给人们带来风味独特的各种果酱、果冻等食品。
按果胶中甲氧基(—OCH3)含量,可将由果胶物质形成的凝胶分为两类。
1.3果胶的用途
果胶的主要用途是作为食品用添加剂。
果胶在水溶液中由于负电荷的高分子作用,可以使其凝胶化、增粘、蛋白质稳定化等改变食品的物性。
果胶作为一种植物胶,具有胶凝和乳化作用,在食品工业中主要用作胶凝剂、增稠剂及稳定剂,广泛用于糖果、果冻、果汁、罐头及各种饮料中。
由于果胶具有抗菌、止血、消肿、解毒、止泻、降血脂、抗辐射等作用,还是一种优良的药物制剂基质,近年来,其在医药领域的应用较为广泛[6]。
果胶是亲水胶状物质,具有良好的胶凝性和乳化稳定作用,主要用于食品工业,如果酱和果冻类,婴儿食品,冰淇淋及果汁的稳定剂,蛋黄乳化剂和增稠剂。
在医学上,果胶是铅,汞和钴等金属中毒的良好解毒剂和预防剂,果胶和果胶的铝盐可抑制肠道对胆固醇和三酸甘油酯的吸收,可用作动脉硬化等心血管疾病的
辅助治疗。
果胶可分为HM果胶(即高甲氧基果胶)及LM果胶(即低甲氧基果胶)。
HM果胶即普通果胶,须在可溶性物质含量达50%以上时方可形成凝胶体,其甲氧基含量愈多凝胶力愈大;
而LM果胶只要有多价离子如钙,镁等存在,即使可溶物质低至1%,仍可因架桥反应而形成果胶酸盐的凝胶体,在食品中不仅可增加凝胶力,还可以大大节减用糖。
由于果胶是果实的成分,所以特别适合做果冻、果酱、蜜饯、果汁、水果罐头等果味食品的添加剂,此外,在可乐和啤酒行业中的使用也取得很好的效果。
有关研究显示,果胶能使人进餐后升高的血糖降低,每人每天摄入6~8g果胶,能有效地降低胆固醇。
因此,果胶对高胆固醇患者和糖尿病患者是大有裨益的,果胶是一种具有优良胶凝化和乳化作用的天然产物,可作为食品胶凝剂、增稠剂、稳定剂和乳化剂,随着功能性多糖的开发研究,果胶作为水溶性膳食纤维。
另外果胶还可以用来制轻泻剂、止血剂、毒性金属解毒剂、代血浆用品及延长抗菌素的作用等[7]。
高甲氧基果胶可以有效地稳定酸牛奶制品并改善它的风味,特别是对人工发酵的酸乳和使用化学方法酸化的牛奶饮料效果更好。
在果汁奶生产中所遇的pH值范围内,牛奶中酪蛋白沉淀出来,产品分离成两相;
加热杀菌时分层现象更加严重。
作为一种稳定剂,高甲氧基果胶可使牛奶和果汁结合成一种含牛奶蛋白、矿物质及果汁的饮料。
pH低于酪蛋白的等电点时(pH=4.6)加人果胶,酪蛋白胶体微粒带阳电荷,而果胶带负电荷,而产生稳定的酪蛋白一果胶溶和物,于是果胶起着抑制酪蛋白沉淀的作用,这样可以使产品保持良好的稳定性。
所以对果胶的提取越来越受到重视,应用必定会越来越广泛。
1.4果胶的提取
提取果胶的原料很多,主要有桔皮,桔汁液,桔囊衣、柚皮、葡萄皮、鲜苹果皮、马铃薯、向日葵、山楂、胡萝卜等。
天然果胶质中的原果胶不溶于水,但可在酸、碱、盐等化学试剂作用下水解成水溶性果胶;
果胶酸是水溶性的。
果胶可分为水溶性和水不溶性两种,水不溶性的果胶可溶于六偏磷酸钠溶液或盐酸溶液,依照酯化度的不同,酯化度大于50%(甲氧基含量>
7%)称为高甲氧基果胶(HM一果胶),低于5O(甲氧基含量<
7%)称为低甲氧基果胶(LH一果胶)。
随着甲氧基含量的增加,果胶溶解度减小。
因此,果胶的提取就是一个把不溶性高酯果胶转化成可溶性低酯果胶和可溶性果胶向液相转移的过程[8]。
果胶结构在很大程度上取决于提取原料的种类和提取方法。
结构中的部分羧基可被甲醇酯化,果胶的酯化度(DE)可因提取原料的种类、生长和采割期及加工方法等的不同而有很大差别。
例如,由柠檬等柑橘类外果皮和苹果渣所制得的是酯化度为5O%~75%的高酯果胶(HM),由向日葵盘所制得的为酯化度2O%~50%的低酯果胶(LM),由甜菜渣所制得的则是部分乙酰化的果胶。
高酯果胶在氨存在的条件下,可制得酰胺化果胶[9]。
目前,果胶的主要提取方法大致有3种:
离子交换树脂法、微波法和酸法。
1.4.1离子交换树脂法
离子交换树脂法,以柑桔皮为例,这种方法的基本步骤为:
柑桔皮→浸泡→加入离子交换剂→调节pH值→搅拌加热→分离→醇沉淀→分离一洗涤一干燥
国内外关于用离子交换树脂法提取果胶的报道极少。
据Hanng等介绍,加入3价离子交换树脂,可使柑桔皮果胶的提取得率高达22%~3O%,胶凝度在130~300之间,其中树脂主要为具有一SO3H、一C02H、一PO4H、一C02IxH3、一SO3、一CO2一、一PO43-等活性基团的交换树脂。
有研究报道,以柑桔皮为原料,树脂采用聚苯乙烯型磺酸基阳离子交换树脂(732),用阳离子树脂交换法,进行了提取果胶的系统性实验,同时又对生产果胶的几种方法作了比较。
发现离子交换法能提高果胶产率,增大胶凝力,改善产品的颜色[10]。
1.4.2微波法
用传统的加热方法提取果胶需要高温和长时间加热,原料中的果胶不可避免地产生变性和分解破坏,且提取的果胶数量和质量也不理想。
微波是频率0.3~300GHz之间的电磁波,即波长在1O0~0.1cm范围内的电磁波,用于天然成分的提取,选择性强,操作时间短,溶剂耗量小,受热均匀,不会破坏果胶长链结构,得率和质量都有所提高,并且能极大限度地保留分离组分的天然活性。
21世纪初,美国发表了用微波加热技术提取果胶的专利权。
在国内,一些科研工作者,以橘皮、柚皮、向日葵盘等为原料,采用微波法提取果胶,以降低成本,节约能耗,并保证果胶成品质量为目的,作了大量的探讨[4]。
1.4.3酸法
酸提取法是一种最古老的工业果胶生产方法,其基本原理是将植物细胞中的非水溶性果胶在稀酸中转化成水溶性果胶,并萃取出来。
常用的酸有盐酸、六偏磷酸、草酸等。
经酸萃取后得到很稀的果胶水溶液,将果胶分离出来的方法有沉淀法、盐析法、电解沉淀法和胶体沉淀法等,但在工业生产中常采用醇沉淀法和盐析法。
醇沉淀法的基本原理是利用果胶不溶于醇类溶剂的特点,加人大量醇,使果胶的水溶液中形成醇一水的混合剂以使果胶沉淀出来。
醇沉淀法属于最早工业化的方法,但其生产成本高,成品质量低,且能耗大,规模化生产困难。
盐沉淀法是目前在经济上比较可行的提取果胶方法。
盐沉淀法提取果胶的基本原理是根据果胶中的游离羧基(一COOH)容易被钾、钠、铵等离子中和的这一特性,加氨水中和果胶,加盐沉淀果胶,从而会有不溶于水的果胶酸盐和少量的盐的氢氧化物沉淀以及其它杂质产生。
经分离后,用酸和醇的混合液洗沉淀,酸与金属离子发生置换反应生成果胶,而少量的盐的氢氧化物沉淀消失。
生成的果胶不溶于乙醇而沉淀下来,氯酸盐等溶于醇的水溶液中,分离得果胶。
现在主要的盐沉淀法有混合盐析法、铝盐法和铁盐法。
此外,还有铜盐法,有文献报道,以松树皮及向日葵盘为原料,利用Cu2+盐使果胶生成络合物沉淀析出,并使其溶解,然后除去Cu2+,再通过乙醇沉淀析出果胶。
在这些盐析法中铝盐法比较早,有运用铝盐法从向日葵梗和杆芯、苹果渣、佛手瓜及仙人掌等原料中提取果胶的研究报道,和醇沉淀法相比,降低了成本及能耗,且果胶的酯化度比醇沉淀法高,凝胶强度大。
混合盐析法采用铁、铝混合盐沉析果胶,通过从柑桔皮及烟末中提取果胶产品的实验中证明,混合盐析法提取出果胶较单一盐析法要好,得到的产品色泽好,产率高,所得到的沉淀性状好,易于分离,且色泽较浅,因此,混合盐析法在盐析法中是一种比较好的沉析果胶的方法。
但是铝盐法提取得到的果胶,果胶铝结合紧密,不易除去铝离子,灰分高。
科学工作者在大量的实验研究基础上,又相继提出了铁盐法和混合盐析法等。
其中铁盐法产率较高,质量稳定,凝胶强度大,并有研究表明,运用铁盐法从柑桔皮提取的果胶产品质量稳定,并省去传统乙醇法的浓缩步骤,简化了工艺,乙醇耗量可降低50%且得率高[2]。
1.5马铃薯果胶的提取
果胶作为一种食品添加剂,我国至今仍未形成规模化大生产,每年需进口大量食用果胶以满足食品行业的需求。
影响工厂规模化生产果胶的主要原因是采用常规法生产果胶时,酒精耗量大,加之酒精价格的逐年上涨,使得生产成本高。
国外对果胶的研究和商品化生产已经有了较大的发展。
我国是一个马铃薯生产大国,2001年世界马铃薯产量为2.9亿吨,其中我国年产0.6亿吨,居世界第一位。
在国内马铃薯等薯类的深加工开发利用较晚,年产量约78%被鲜食,8%烂掉,4%饲用,而用于深加工的马铃薯不足年产量的10%。
在我国北方大部分地区马铃薯加工产品主要是提取淀粉,制作粉丝、粉条等,产生大量薯渣,薯渣通常作为饲料或废渣处理,未能充分合理利用,且鲜薯渣含水量高达80%,不易储存、运输,腐败变质后产生恶臭,造成环境污染;
若烘干制成干饲料则成本过高,增加企业负担,通常作为饲料或废渣处理,利用程度较低。
随着我国马铃薯产业化发展,马铃薯淀粉加工带来的废渣处理问题越来越受到重视。
2001年8月6日在兰州、召开的“中国马铃薯学术年会”上将薯渣综合利用的问题列为今后马铃薯加工企业重点解决的问题[11]。
目前,果胶在国内外市场上销路很好,但果胶作为一种食品添加剂在我国还处在试验阶段,我国虽开始有些单位进行果胶的研制,但质和量都不理想,仍需进口,进口价高达160~200元/kg。
利用我国大量的食品工业再生资源(如柑桔皮、苹果渣、马铃薯渣)生产果胶,具有很大的经济效益和社会效益[2]。
因此本文从马铃薯渣中提取果胶不仅有极大的工业价值,而且对综合开发、利用马铃薯资源,提高原材料利用率,减少环境污染,有重要的实际意义。
马铃薯渣是以鲜薯为原料加工淀粉后的副产品,含有大量的纤维素、果胶及少量蛋白质等可利用成分,具有很高的开发利用价值。
对果胶的提取,前人曾作过不少对柑桔,香蕉,苹果等果胶含量丰富的植物进行果胶提取,但是对果胶含量同样丰富的马铃薯的果胶提取研究报道却不是很多,没有得到足够的重视,根据相关资料显示,马铃薯原料中果胶含量在15%左右[4],表明薯渣中含有丰富的果胶,是一种良好的果胶提取原料。
因此如何提高马铃薯果胶的产量,是很值得我们研究的一个重要问题。
目前广泛应用的是乙醇沉淀法提取果胶,但是乙醇消耗量太大,且需要真空浓缩,所以并不适合工艺化大生产。
对从马铃薯渣中提取果胶,已有微波法提取的相关报道,所以本文采用铁盐沉淀法提取果胶,得出铁盐沉淀法的最佳工艺条件,对从马铃薯渣中提取果胶的的工业化大生产具有一定的实际的意义。
本文就利用酸萃取铁盐沉淀法从含果胶很丰富的马铃薯中提取果胶,对提取果胶的方案进行研究,以获得提取马铃薯果胶的优化方案,对提高马铃薯的果胶产量及综合的利用具有一定的实际意义。
铁盐法实验原理,是根据果胶中的游离羧基(—COOH)容易被钾、钠、铵等离子中和的这一特性,所以本实验加入氨水中和果胶中的游离羧基(—COOH),再加入高价铁盐沉淀果胶,从而得到不溶于水的果胶酸盐和少量Fe(OH)3以及其它杂质产生。
经分离后,由酸和醇的混合液洗沉淀,酸与金属离子发生置换反应生成果胶,而少量Fe(OH)3沉淀消失,生成的果胶不溶于醇而沉淀下来[12]。
2材料及工艺
2.1材料
2.1.1原料
农院菜场购买的成熟,无虫害,无霉变的马铃薯。
2.2.2试剂
盐酸,三氯化铁,乙醇,氨水等均为分析纯。
2.1.2仪器
FA2104S型电子天平:
上海天平仪器厂;
766-1型远红外辐射干燥箱:
江苏省南通农业科学仪器厂;
SY21-Ni8电热恒温水浴锅:
北京长源实验设备厂;
FW80型万能粉碎机:
天津泰斯特仪器有限公司;
HI98128PH计:
上海第二分析仪器厂。
2.2工艺及操作要点
2.2.1工艺流程
盐酸FeCl3溶液
↓↓
马铃薯渣的制取→马铃薯的预处理→酸萃取→沉淀果胶铁盐
→过滤→成品
↑
盐酸和乙醇混合液
2.2.2操作要点
2.2.2.1马铃薯渣的制取
首先用水清洗马铃薯,待马铃薯干后,将其切碎,放入万能粉碎机中进行粉碎,将粉碎后的马铃薯渣倒入烧杯中,洗涤2~3次,然后向烧杯中加水,静置5小时,然后过滤,所的滤渣即为提取淀粉后的马铃薯渣[13]。
2.2.2.2马铃薯的预处理
称取20g提取淀粉后的马铃薯渣,加入一定量的水,把水煮沸5~8min除去马铃薯渣中的果胶酶,以防止提取的时候果胶发生分解,搅拌一定时间,静置,趁热用布过滤,将灭酶后的马铃薯渣漂洗1~2次。
2.2.2.3酸萃取
将漂洗后的马铃薯渣,置于烧杯中,加一定量的水,在搅动下慢慢的加入盐酸,调节溶液的pH值。
并加热至一定的温度,浸提一定时间。
在萃取过程中,体系的pH值会发生变化,要经常用pH计测溶液的pH值,注意使之稳定,以保证萃取的效果。
如果pH值偏高时应加适量盐酸调节pH值。
2.2.2.4沉淀果胶铁盐
萃取结束后,趁热将萃取液进行过滤,将提取液加热至70℃左右,加入1:
1的稀氨水调节溶液的pH值至2.3~4之间。
然后在搅拌下缓缓加入10%FeCl3溶液,使其逐渐形成果胶酸盐的絮状沉淀。
接着再用稀氨水调节至相同pH值,盐析后将溶液静置1h[14]~[15]。
2.2.2.5过滤
过滤分离,弃去滤液,滤渣即为粗果胶。
将粗果胶先用水冲洗掉色素和部分杂质,沥干后加入10%的盐酸∶70%乙醇=1∶1的混合液(加入量约为粗果胶的2~3倍),并加热。
搅拌1h,使果胶沉淀中的Fe(OH)3溶解[14]~[15]。
2.2.2.6成品
再将溶液过滤,将滤液用含加入10%的盐酸∶70%乙醇=1∶1洗涤2~3次。
过滤后将滤渣用红外线烘干机在50~60℃将其干燥,将其在电子天平上进行称量得果胶产量,烘干后将其粉碎即为果胶成品[14]~[15]。
2.3果胶含量检测
准确称取0.5g果胶于250mL烧杯中,加50mL水溶解,煮沸lh(煮沸过程中不断补充水,以保证其体积不变),移人250mL容量瓶,加水至刻度。
过滤,取25mL滤液于500mL烧杯中,加入100mL、0.1mol/L的NaOH溶液,静置30min,再加入50mL、1mol/L的NaOH溶液,5min后加入50mL、1mol/L的CaCl2溶液,放置1h后煮沸5min,过滤,用热水洗涤至无Cl-。
将沉淀物放人称量瓶中于105℃烘至恒重[5]。
果胶百分含量(%)=0.9235×
(W1-W2)×
100/G×
(25/250)
式中:
0.9235—果胶酸钙换算果胶的系数;
W1—果胶酸盖与干滤纸重(g);
W2—干滤纸重(g);
G—样品质量(g)。
3实验部分
3.1单因素实验分析
3.1.1水料比和果胶产量的关系
选取酸萃取时溶液pH值为2.0,浸提温度为85℃,浸提时间60min,FeCl3用量为10ml,沉淀时pH值为4,改变水料比分别为5:
1、10:
1、15:
1、20:
1、25:
1时提取果胶,所提取的果胶产量如图3.1所示。
图3.1水料比对果胶产量的影响
由图3.1可知,当水料比在5:
1和10:
1时,所得果胶产量很低分别为1.495g和2.684g,当水料比在20:
1和25:
1左右时,所得果胶的产量较高分别为3.617g和3.759g,因此,选择水和马铃薯渣的水料比在20:
1~25:
1提取果胶的的产量比较高。
3.1.2pH值与果胶产量的关系
选取水:
马铃薯的水料比为20:
1,浸提温度为85℃,浸提时间60min,FeCl3用量为10ml,沉淀时pH值为4,改变酸萃取时溶液的pH值:
分别在pH=1.0、pH=1.5、pH=2.0、pH=2.5、pH=3.0时提取果胶,所提取的果胶产量如图3.2所示。
图3.2酸萃取时pH值对果胶产量的影响
由图3.2可知,当酸萃取pH值从1.0逐渐上升到2.0时,所得果胶产量呈上升趋势,所得的果胶产量分别为2.763g、3.075g、3.617g。
酸萃取pH值从2.0~3.0变化时果胶产率产量逐渐降低分别为3.278g和3.079g。
因此,选择酸萃取pH值在2.0左右为最佳提取pH值。
3.1.3浸提温度与果胶产量的关系
选取水:
1,酸萃取时溶液pH值为2.0,浸提时间60min,FeCl3用量为10ml,沉淀时pH值为4,改变浸提温度分别为70℃、75℃、80℃、85℃、90℃、95℃时提取果胶,所提取的果胶产量如图3.3所示。
图3.3浸提温度对果胶产量的影响
由图3.3可知,当浸提温度从70℃升高时,所得果胶产量呈上升趋势,当浸提温度升高在85~90℃左右时果胶产量较高,分别为3.617g和3.872g。
当浸提温度大于90℃,由于温度果胶,导致果胶产生少量分解,果胶产量略有降低,产量为3.397g。
因此,浸提温度在85~90℃时为最佳浸提温度。
3.1.4浸提时间与果胶产量的关系
1,酸萃取时溶液pH值为2.0,浸提温度为85℃,浸提时间60min,FeCl3用量为10ml,沉淀时pH值为4,改变浸提时间分别为40min、50min、60min、70min、80min、90min时,所提取果胶产量如图3.4所示。
图3.4浸提温度对果胶产量的影响
由图3.4可知,当浸提时间由40min~60min左右时,果胶产率产量逐渐升高,当浸提时间大于60min,所得果胶产量变化不大,因此,选择浸提时间为60min即节省了时间,所提取的果胶产量也很高。
3.1.5FeCl3用量与果胶产量的关系
1,酸萃取时溶液pH值为2.0,浸提温度为85℃,浸提时间60min,沉淀pH值为4,改变FeCl3用量为10ml分别为5ml、6ml、7ml、8ml、9ml、10ml时,所萃取果胶产量分别如图3.5所示。
图3.5FeCl3用量对果胶产量的影响
由图3.5可知,当FeCl3用量从5ml增加至7ml左右时,所得果胶产量逐渐升高,FeCl3用量在7ml时,果胶产量最高为3.786g。
当FeCl3用量大于7ml时,产量有少量减少。
当FeCl3用量为7ml时,提取果胶的产量最高,相比较其他用量,生成的Fe(OH)3也最少,所以选择FeCl3用量7ml时左右时,提取果胶的效果最好。
3.1.6沉淀pH与果胶产量的关系
1,酸萃取时溶液pH为2.0,浸提温度为85℃,浸提时间60min,FeCl3用量为10ml,改变沉淀时pH值分别2.0、2.5、3.0、3.5、4.0所提取的果胶产量分别为如图3.6所示。
图3.6沉淀pH值对果胶产量的影响
由图3.6可知,当沉淀果胶铁盐时pH在3时,所提取的果胶产量最高为3.858g。
当沉淀pH值从2-3逐渐升高时,所得果胶产量逐渐增加,当沉淀pH值大于3时,所得果胶产量逐渐降低。
所以选择沉淀果胶铁盐时pH在3左右时,所提取果胶pH值的效果最好。
3.2正交实验分析
根据以上单因素实验的初步结果,酸萃取时要考虑水料比,酸萃取温度,浸提温度,浸提时间,又因为FeCl3用量,沉淀pH值是在沉淀果胶铁盐时考虑,这2组因素可以独立考虑,所以选择水料比,酸萃取温度,浸提温度,浸提时间做正交实验分析,并从单因素实验中选择提取条件比较好的几个水平做交叉实验,进行4因素3水平的正交实验分析。
表3.1因素水平表
水平
因素
水料比
酸萃取时pH值
浸提温度℃
浸提时间min
1
15:
1.5
85
60
2
20:
2.0
90
70
3
25:
2.5
95
80
表3.2L9(34)铁盐法提取马铃薯