专题08 电极反应方程式专练高三化学冲刺复习主观题一遍过原卷版Word格式文档下载.docx
《专题08 电极反应方程式专练高三化学冲刺复习主观题一遍过原卷版Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《专题08 电极反应方程式专练高三化学冲刺复习主观题一遍过原卷版Word格式文档下载.docx(12页珍藏版)》请在冰豆网上搜索。
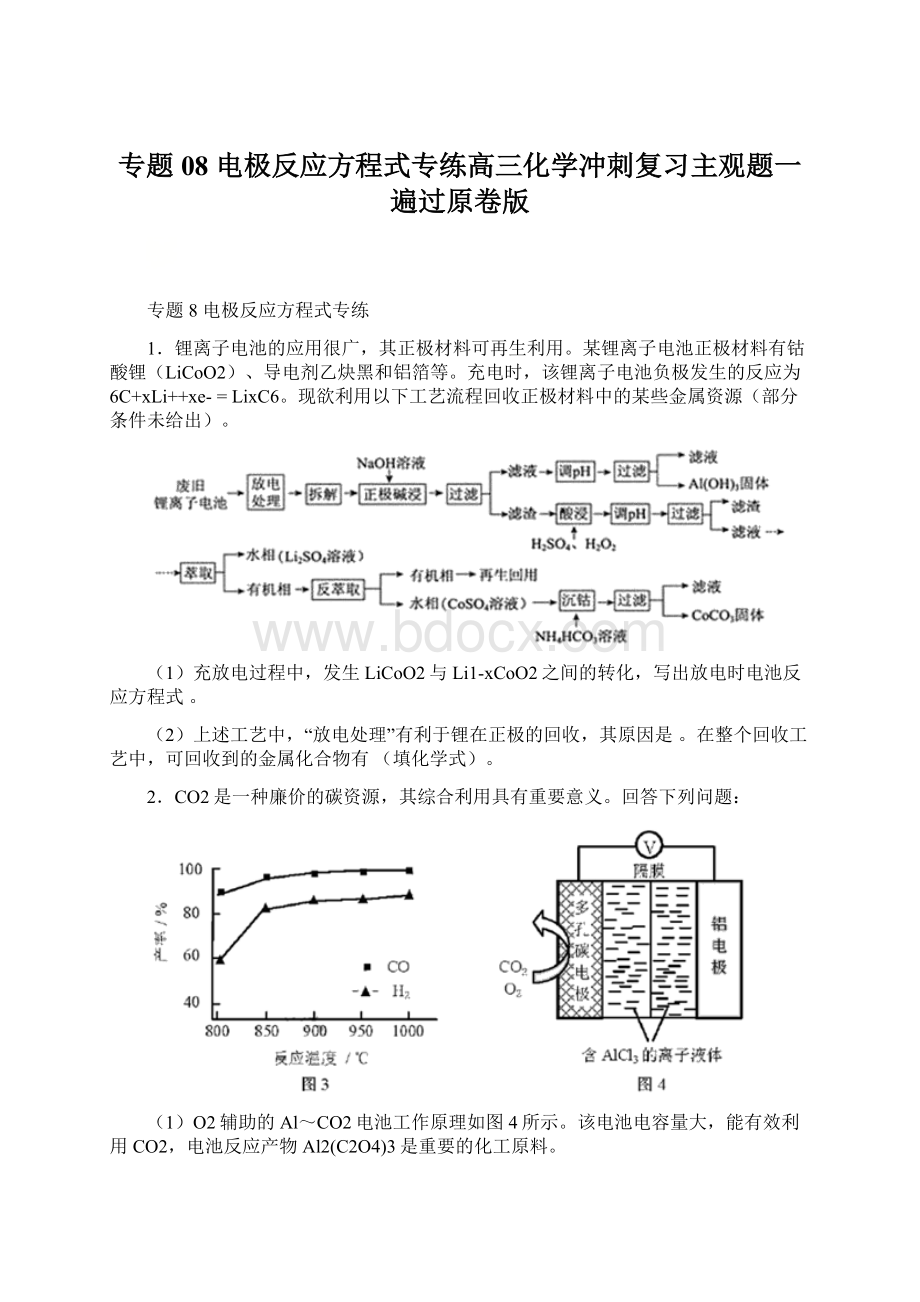
6O2−
6CO2+6O2−
3C2O42−
反应过程中O2的作用是________。
该电池的总反应式:
3.利用LiOH和钴氧化物可制备锂离子电池正极材料。
LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。
B极区电解液为________溶液(填化学式),阳极电极反应式为_________,电解过程中Li+向_____电极迁移(填“A”或“B”)。
4.石墨在材料领域有重要应用。
某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。
设计的提纯和综合应用工艺如下:
(注:
SiCl4的沸点是57.6º
C,金属氯化物的沸点均高于150º
C)
(1)石墨可用于自然水体中铜件的电化学防腐,完成下图防腐示意图,并作相应标注。
5.锂锰电池的体积小、性能优良,是常用的一次电池。
该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
回答下列问题:
(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池正极反应式为___________________________________。
(3)是否可用水代替电池中的混合有机溶剂?
________(填“是”或“否”),原因是________________________________________________________________。
6.NH3经一系列反应可以得到HNO3,如下图所示。
(1)IV中,电解NO制备NH4NO3,其工作原理如右图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是_____________,说明理由:
________________。
7.锌锰电池(俗称干电池)在生活中的用量很大。
两种锌锰电池的构造图如图(a)所示。
(1)①普通锌锰电池放电时发生的主要反应为:
Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH。
该电池中,负极材料主要是____________________,电解质的主要成分是__________,正极发生的主要反应是________________________________________________________。
②与普通锌锰电池相比,碱性锌锰电池的优点及其理由是_______。
8.化学在环境保护中起着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)电化学降解NO3-的原理如图所示。
①电源正极为(填A或B),阴极反应式为。
②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为g。
9.金属冶炼和处理常涉及氧化还原反应。
(1)下图为电解精炼银的示意图,(填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体产生,则生成该气体的电极反应式为,
(2)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为。
10.利用化石燃料开采、加工过程产生的H2S废气制取氢气,既廉价又环保。
(1)利用H2S废气制取氢气来的方法有多种
电化学法
该法制氢过程的示意图如右。
反应池中反应物的流向采用气、液逆流方式,其目的是___________;
反应池中发生反应的化学方程式为_____________________。
反应后的溶液进入电解池,电解总反应的离子方程式为_______________________。
11.KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。
(1)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:
(2)KIO3也可采用“电解法”制备,装置如图所示。
①写出电解时阴极的电极反应式_____。
②电解过程中通过阳离子交换膜的离子主要为_____,其迁移方向是_____。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有_____(写出一点)。
12.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。
从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):
编号
实验目的
碳粉/g
铁粉/g
醋酸/%
①
为以下实验作参照
0.5
2.0
90.0
②
醋酸浓度的影响
36.0
③
0.2
(2)编号①实验测得容器中压强随时间变化如图2。
t2时,容器中压强明显小于起始压强,其原因是铁发生了腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;
此时,碳粉表面发生了(“氧化”或“还原”)反应,其电极反应式是。
13.NOx(主要指NO和NO2)是大气主要污染物之一。
有效去除大气中的NOx是环境保护的重要课题。
(1)用稀硝酸吸收NOx,得到HNO3和HNO2的混合溶液,电解该混合溶液可获得较浓的硝酸。
写出电解时阳极的电极反应式:
____________________________________。
14.焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛。
(1)制备Na2S2O5也可采用三室膜电解技术,装置如图所示,其中SO2碱吸收液中含有NaHSO3和Na2SO3。
阳极的电极反应式为_____________。
电解后,__________室的NaHSO3浓度增加。
将该室溶液进行结晶脱水,可得到Na2S2O5。
15.某混合物浆液含Al(OH)3、MnO2和少量Na2CrO4。
考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图2),使浆液分离成固体混合物和含铬元素溶液,并回收利用。
回答Ⅰ和Ⅱ中的问题。
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
Ⅱ.含铬元素溶液的分离和利用
(1)用惰性电极电解时,CrO42-能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;
阴极室生成的物质为___________(写化学式)。
16.铝是应用广泛的金属。
以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:
注:
SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。
阳极的电极反应式为_____________________,阴极产生的物质A的化学式为____________。
17.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
①作负极的物质是________。
②正极的电极反应式是_________。
18.氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。
(1)化工生产的副产氢也是氢气的来源。
电解法制取有广泛用途的Na2FeO4,同时获得氢气:
Fe+2H2O+2OH−
FeO42−+3H2↑,工作原理如图1所示。
装置通电后,铁电极附近生成紫红色的FeO42−,镍电极有气泡产生。
若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。
已知:
Na2FeO4只在强碱性条件下稳定,易被H2还原。
①电解一段时间后,c(OH−)降低的区域在_______(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______。
③c(Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:
_____________。
19.(14分)研究CO2在海洋中的转移和归宿,是当今海洋科学研究的前沿领域。
(1)溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:
。
(2)利用下图所示装置从海水中提取CO2,有利于减少环境温室气体含量。
①结合方程式简述提取CO2的原理:
②用该装置产生的物质处理b室排出的海水,合格后排回大海。
处理至合格的方法是。
20.氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。
下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
(1).写出电解饱和食盐水的离子方程式。
(2).离子交换膜的作用为:
、。
(3).精制饱和食盐水从图中位置补充,氢氧化钠溶液从图中位置流出(选填“a”、“b”、“c”或“d”)。
21.C、N、O、Al、Si、Cu是常见的六种元素。
(1)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
0-t1时,原电池的负极是Al片,此时,正极的电极反应式是_____,溶液中的H+向___极移动,t1时,原电池中电子流动方向发生改变,其原因是______。
22.我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。
(1)下图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
①腐蚀过程中,负极是(填图中字母“a”或“b”或“c”);
②环境中的Cl-扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈u2(OH)3Cl,其离子方程式为;
③若生成4.29gCu2(OH)3Cl,则理论上耗氧体积为L(标准状况)。
23.次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
(1)(H3PO2)也可以通过电解的方法制备.工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过):
①写出阳极的电极反应式___________;
②分析产品室可得到H3PO2的原因___________;
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的阳膜,从而合并了阳极室与产品室,其缺点是___________杂质。
该杂质产生的原因是___________。
24.氢能是重要的新能源。
储氢作为氢能利用的关键技术,是当前关注的热点之一。
(1)一定条件下,题11图示装置可实现有机物的电化学储氢(忽略其它有机物)。
①导线中电子移动方向为____________。
②生成目标产物的电极反应式为_________。
③该储氢装置的电流效率
=_____(
=
×
100%,计算结果保留小数点后1位)
25.硫化氢的转化是资源利用和环境保护的重要研究课题。
由硫化氢获得硫单质有多种方法。
(1)将烧碱吸收H2S后的溶液加入到如题20图—1所示的电解池的阳极区进行电解。
电解过程中阳极区发生如下反应:
S2-—2e-
S(n—1)S+S2-
Sn2-
①写出电解时阴极的电极反应式:
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成。