一轮复习乙烯烯烃1Word格式.docx
《一轮复习乙烯烯烃1Word格式.docx》由会员分享,可在线阅读,更多相关《一轮复习乙烯烯烃1Word格式.docx(17页珍藏版)》请在冰豆网上搜索。
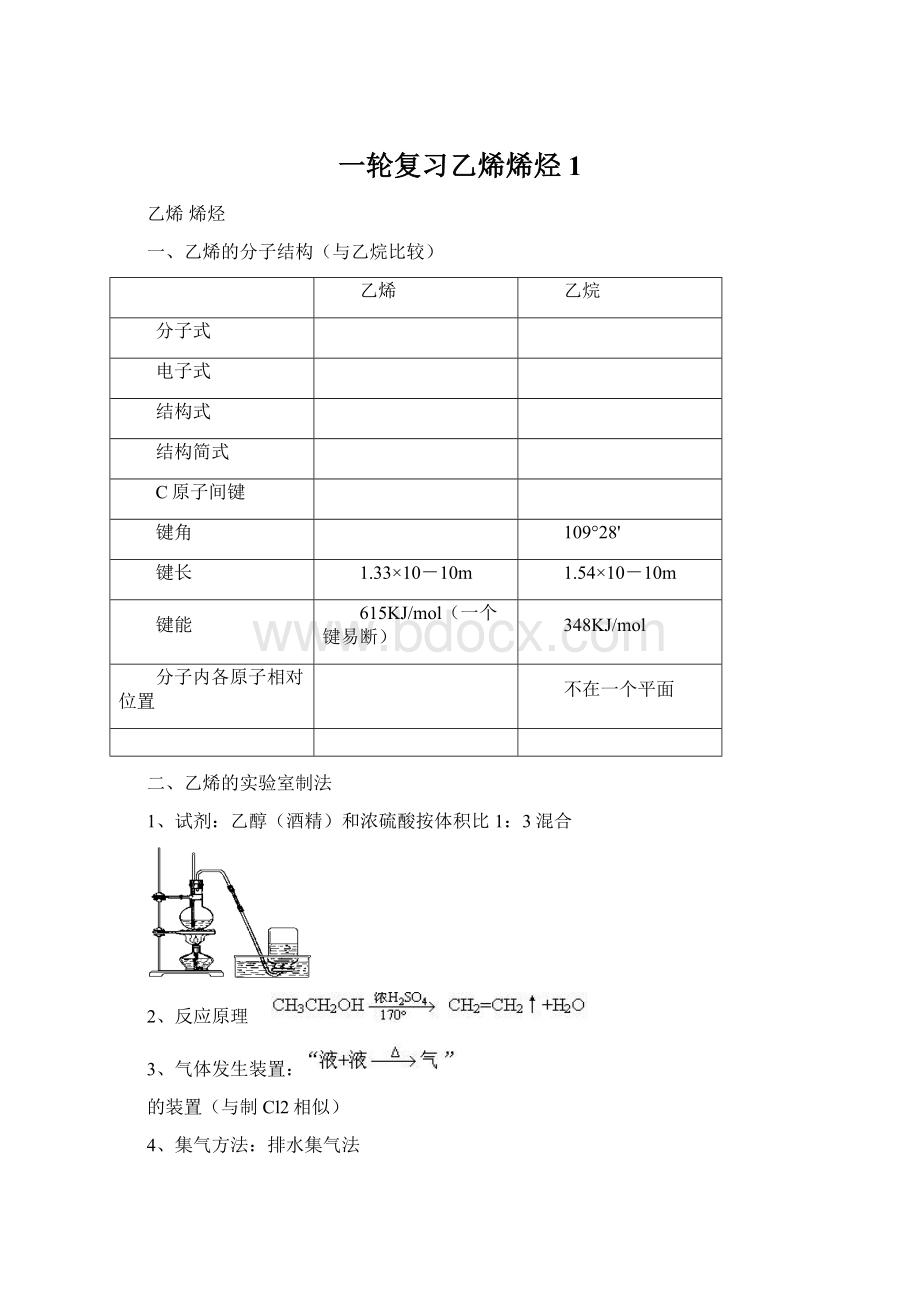
②碎瓷片的作用
防止液体剧烈跳动(防止煮沸)。
③反应温度应控制在170℃,若温度过低(140℃)将发生副反应,而生成乙醚;
若温度过高,则乙醇易被浓H2SO4氧化。
为了控制温度,应将温度计的水银球插在液面下。
以准确测定反应液体的温度。
④反应后液体易变黑,且有刺激性气味气体产生。
这是由于浓硫酸的强氧化性将乙醇氧化生成C和CO2,且硫酸被还原成SO2所致。
其反应方程式可表示为:
若要净化乙烯,可将其通过NaOH溶液除去SO2、CO2。
三、乙烯的物理性质
无色、稍有气味、难溶于水、ρ=1.25g/L
乙烯是一种典型的不饱和烃,
四、化学性质
(一)氧化反应
1、燃烧
将原先的装置中用于收集乙烯的导气管换成带玻璃尖嘴的导气管,点燃酒精灯,使反应温度迅速升至170℃,排空气,先收集一部分乙烯于试管中验纯,之后用火柴点燃纯净的乙烯。
实验现象:
乙烯气体燃烧时火焰明亮,并伴有黑烟。
熄灭燃烧的乙烯气,冷却,将乙烯通入盛有酸性KMnO4溶液的试管中,酸性KMnO4溶液的紫色很快褪去。
将乙烯气通入盛有溴的四氯化碳溶液的试管中,溴的四氯化碳溶液的红棕色很快褪去。
(先撤出导管,后熄灭酒精灯,停止反应,演示实验结束)
2、使酸性KMnO4溶液褪色(可以用于鉴别甲烷和乙烯,可以除去甲烷中乙烯杂质吗?
)
乙烯与溴反应时,乙烯分子的双键中有一个键被打开,两个溴原子分别加在两个价键不饱和的碳原子上,生成了无色的物质:
1,2—二溴乙烷。
(二)加成反应
加成反应:
有机物分子中双键(或叁键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应。
除了溴之外还可以与水、氢气、卤化氢、Cl2等在一定条件下发生加成反应,
①与卤素加成:
CH2=CH2+X2→CH2X-CH2X(使溴水褪色,可用于检验乙烯或除去乙烯)
②与氢气加成:
③与卤化氢HX加成:
(可用于制氯乙烷)
④与水加成:
(可用于工业上制酒精)
(三)加聚反应:
在适宜的温度、压强和有催化剂存在的条件下,乙烯的碳碳双键中的一个键会断裂,分子里的碳原子能互相结合成很长的链,就生成了聚乙烯。
(可用于制聚乙烯塑料)
加聚反应:
指不饱和单体通过加成反应互相结合成高分子化合物的反应。
聚乙烯的分子很大,相对分子质量可达到几万到几十万。
相对分子质量很大的化合物属于高分子化合物,简称高分子或高聚物。
那么由类似乙烯这样的相对分子质量小的化合物分子互相结合成相对分子质量大的高分子的反应叫做聚合反应。
握聚合反应的两个特点:
其一是由分子量小的化合物互相结合成分子量很大的化合物;
其二是反应属于不饱和有机物的加成反应。
像这种既聚合又加成的反应又叫加聚反应。
乙烯生成聚乙烯的反应就属于加聚反应。
四、乙烯的用途
乙烯的一个重要用途:
作植物生长调节剂可以催熟果实;
乙烯是石油化学工业最重要的基础原料,可用于制造塑料、合成纤维、有机溶剂等,乙烯的生产发展带动其他石油化工基础原料和产品的发展。
所以一个国家乙烯工业的发展水平即乙烯的产量,已成为衡量这个国家石油化学工业水平的重要标志之一。
烯烃
一、烯烃的概念:
分子里含有碳碳双键的一类链烃,乙烯是烯烃的典型,也是最简单的烯烃
二、烯烃的通式:
CnH2n(n≥2)
实际我们所说的烯烃都是指分子中只含一个碳碳双键的不饱和烃,所以也叫单烯,也还有二烯烃:
CH2==CH-CH==CH2烯烃的通式为CnH2n,但通式为CnH2n的烃不一定是烯烃,如右图中其分子式为C4H8,符合CnH2n,但不是烯烃
三、烯烃在物理性质上有何变化规律?
①随着分子里碳原子数的增加,熔沸点逐渐升高,相对密度逐渐增大;
烯烃的相对密度小于水的密度;
不溶于水等。
②烯烃常温常压下C原子数1~4为气态,C原子数5~10为液态,C原子数11以上固态,
四、烯烃化学性质
由于烯烃的分子结构相似——碳碳双键,所以它们的化学性质与乙烯相似,
(一)氧化反应 1.燃烧CnH2n+
O2nCO2+nH2O
2.使酸性KMnO4溶液褪色
(二)加成反应
R-CH==CH-R′+Br-Br
(三)加聚反应
R-CH==CH2(聚丙乙烯)
5、烯烃的系统命名法
①选主链,称某烯。
(要求含C═C的最长碳链)
②编号码,定支链,并标明双链和取代基的位置,若分子中出现二次以上的双键,则以“二烯”或“三烯”命名。
★例题精讲
例1、最近国外研究出一种高效的水果长期保鲜新技术:
在3℃潮湿条件下的水果保鲜室中用一种特制的低压水银灯照射,引起光化学反应,使水果贮存过程中缓缓释放的催熟剂转化为没有催熟作用的有机物。
试回答:
(1)可能较长期保鲜的主要原因是__________________________________________。
(2)写出主要反应的化学方程式___________________________________________。
解析:
水果能放出少量的乙烯,乙烯是催熟剂。
根据题意,这种新技术能除去乙烯,把乙烯转化为一种没有催熟作用的有机物,生成什么有机物呢?
联系题中所给出的反应条件“潮湿、光化学反应”可得出乙烯是跟水反应生成乙醇。
(1)使乙烯转化为乙醇而无催熟作用使水果在较低温度下保鲜时间长。
(2)CH2=CH2+H2O
C2H5OH。
例2、若已知某金属卡宾的结构示意为R---M=CH2(R表示有机基团、M表示金属原子),它与CH2=CHCH3的反应如下:
CH2=CHCH3+R---M=CH2
R---M=CHCH3+CH2=CH2
CH2=CHCH3+R---M=CHCH3
R---M=CH2+CH3CH=CHCH3
即2CH2=CHCH3CH2=CH2+CH3CH=CHCH3
现有金属卡宾R---M=CHCH3和烯烃分子CH2=C(CH3)2它们在一起发生反应。
请回答如下问题;
1、能否得到CH3CH2CH=CHCH2CH3(填“能”或“不能”)
2、产物中所有碳原子都在同一平面的的烯烃的结构简式是
3、生成的相对分子质量最小的烯烃的电子式为
4、若由CH2=C(CH3)2制CH2=CHCl则应选用的金属卡宾为
金属卡宾R---M=CHCH3和烯烃CH2=C(CH3)2的反应有:
CH2=C(CH3)2+R---M=CHCH3
CH3CH=C(CH3)2+R---M=CH2
CH3CH=CH2+R---M=C(CH3)2
CH3CH=C(CH3)2+R---M=CHCH3
CH3CH=CHCH3+R---M=C(CH3)2
CH2=C(CH3)2+R---M=CH2
CH2=CH2+R---M=C(CH3)2
CH2=C(CH3)2+R---M=C(CH3)2
R---M=CH2+(CH3)2C=C(CH3)2
由上述反应可知:
答案:
1、不能
2、CH2=CH2CH3CH=CH2CH3CH=CHCH3CH3CH=C(CH3)2(CH3)2C=C(CH3)2
3、
4、R---M=CHCl
例3、Grubbs催化剂,具有非常广泛的官能团实用性,且稳定、易制备。
反应产物的产率高,催化剂的用量少。
它可催化关(成)环复分解反应,它的结构如下:
已知:
环已烷的结构可用表示。
1、上述Grubbs催化剂的分子式为。
2、请用化学方程式表示以为主要原料合成
有机化合物
解析:
1、C46H64RuPN2Cl2
2
、
(先进行“烯烃复分解反应”后酯化也可以,有机物结构用箭线式或结构式都可以)
例4实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的SO2。
某同
学设计下列实验以确定上述混合气体中含有乙烯和SO2。
(1)I、II、III、IV装置可盛放的试剂是:
IIIIIIIV(请将下列有关试剂的序号填入空格内)
A、品红B、NaOH溶液C、浓硫酸D、酸性KMnO4溶液
(2)能说明SO2气体存在的现象是;
(1)使用装置II的目的是;
(2)使用装置III的目的是;
(3)确定含有乙烯的现象是。
分析:
实验室制取乙烯过程中常混有SO2。
证明SO2存在可用品红溶液,看是否褪色。
而证明乙烯存在可用酸性KMnO4溶液,但乙烯和SO2都能使酸性KMnO4溶液褪色,所以在证明乙烯存在以前应除去SO2。
利用乙烯与碱溶液不反应而SO2能与碱溶液反应的性质除去SO2。
答案为:
(1)A;
B;
A;
D。
(2)装置I中品红溶液褪色可说明混合气体中含有SO2。
(3)除去SO2气体(4)检验SO2是否除尽。
(5)装置(III)中品红溶液不褪色,装置(IV)中酸性KMnO4溶液褪色,说明混合气体中含有乙烯。
★实战演练
一、选择题(每小题5分,共45分)
1、右图可用于
A.加热无水醋酸钠和碱石灰制取CH4
B.加热乙醇与浓硫酸的混合液制C2H4
C.加热KClO3和少量MnO2,制取O2
D.加热NH4Cl和消石灰混合物制NH3
2、绿色化学提倡化工生产应提高原子利用率。
原子利用率表示目标产物的质量与生成物总质量之比。
在下列制备环氧乙烷的反应中,原子利用率最高的是
3、两种气态烃以任意比例混合,在105℃时1 L该混合烃与9L O2混合,充分燃烧后恢复到原状态,所得气体体积仍是10L,下列各组混合烃中不符合此条件的是
A.CH4、C2H4B.CH4、C3H6
C.C2H4、C3H4D.C2H2、C3H6
4、婴儿用的一次性纸尿片中有一层能吸水保水的物质。
下列高分子中有可能被采用的是
5、CH4中混有C2H4,欲除去C2H4得纯净CH4,最好依次通过盛下列哪一组试剂的洗气瓶
A.澄清石灰水,浓H2SO4B.酸性KMnO4溶液,浓H2SO4
C.Br2水,浓H2SO4D.浓H2SO4,酸性KMnO4溶液
6、下列关于反应XeF4+2CH3-CH==CH2
2CH3CH2CHF2+Xe的说法正确的是
A.XeF4被氧化B.CH3—CH==CH2是还原剂
C.CH3CH2CHF2是还原产物D.XeF4既是氧化剂,又是还原剂
7、某烃分子中含偶数个碳原子,相同条件下1mL气态烃完全燃烧时需6mL氧气,此烃分子中原子的总数为
A.8B.11C.12D.14
8、烯烃在一定条件下发生氧化反应时,C==C发生断裂。
RCH==CHR′可以氧化成RCHO和R′CHO。
在该条件下,下列烯烃分别被氧化后,产物中可能有乙醛的是
A.CH3CH==CH(CH2)2CH3B.CH2==CH(CH2)2CH3
C.CH3CH==CHCH==CHCH3D.CH3CH2CH==CHCH2CH3
9、丁腈橡胶:
具有优良的耐油、耐高温性能,合成丁腈橡胶的原料是
①CH2==CH—CH==CH2②CH3—C==C—CH3③CH2==CH—CN
④CH3—CH==CH—CN⑤CH3CH==CH2⑥CH3—CH==CH—CH3
A.③⑥B.②③C.①③D.④⑤
二、非选择题(共55分)
10.(9分)某高聚物的结构简式为
形成高聚物分子的三种单体的结构简式分别为、、
。
11.(6分)1999年合成了一种新化合物,本题用x为代号。
用现代方法测得x的相对分子质量为64。
x含碳93.8%,含氢6.2%;
x分子中有3种化学环境不同的氢原子和4种化学环境不同的碳原子;
x分子中同时存在
C—C、C==C和C==C三种键,并发现其C==C比寻常的C==C短。
(1)x的分子式是;
(2)请将x的可能结构式画在方框内。
12.(16分)实验室制取乙烯,常因温度过高而使乙醇和浓H2SO4生成少量的SO2,有人设计下列实验以确认上述混合气体中有乙烯和SO2,试回答下列问题:
(1)图中①②③④装置可盛放的试剂是:
①;
②;
③;
④(将下列有关试剂的序号填入空格内)。
A.品红溶液B.NaOH溶液C.浓硫酸
D.酸性高锰酸钾溶液
(2)装置①中的现象是。
(3)使用装置②的目的是。
(4)使用装置③的目的是。
(5)确证含有乙烯的现象是。
13.(12分)
(1)已知某混合气体由体积分数为80%CH4、15% C2H4和5% C2H6组成。
请计算0.500 mol该混合气体的质量和标准状况下的密度。
(2)CH4在一定条件下催化氧化可以生成C2H4、C2H6(水和其他反应产物忽略不计)。
取一定量CH4催化氧化后得到一种混合气体,它在标准状况下的密度为0.780 g·
L-1。
已知反应中CH4消耗了20.0%,计算混合气体中C2H4的体积分数(本题计算过程中请保留3位有效数字)。
14.(12分)(2000年上海市高考题)某烃A,相对分子质量为140,其中碳的质量分数为0.857。
A分子中有两个碳原子不与氢直接相连。
A在一定条件下氧化只生成G,G能使石蕊试液变红。
试写出:
(1)A的分子式。
(2)化合物A和G的结构简式:
A,G。
(3)与G同类的同分异构体(含G)可能有种。
通常情况下,乙烯是无色,稍有气味的气体,密度与空气相近,难溶于水。
四、化学性质
乙烯化学性较活泼,易发生如下反应:
1、加成反应:
有机物分子里不饱和碳原子跟其它原子或原子团直接结合生成别的物质的反应。
CH2=CH2+Br2→CH2Br-CH2Br(使溴水褪色,可用于检验乙烯或除去乙烯)
2、氧化反应
①燃烧:
(火焰明亮有黑烟)
②可与强氧化剂反应:
使酸性KMnO4溶液褪色(可用于检验乙烯)
3、加聚反应:
(可用于制聚乙烯塑料)加聚反应是指不饱和单体通过加成反应互相结合成高分子化合物的反应。
四、烯烃:
含有碳碳双键的一类链烃
1、烯烃的结构特点是具有碳碳双键。
烯烃的通式为CnH2n(n≥2)。
2、烯烃同系物的结构相似,化学性质与乙烯相似,易发生加成、氧化和加聚反应,其物理性质随着碳原子数增多、分子量增大,分子间作用力增大,熔点、沸点依次升高。
3、烯烃的同分异构体写法:
可依次考虑下列因素:
①碳链异构,②支链位置异构,③双键位置异构。
如C5H10:
五、二烯烃:
含有二个碳碳双键的烃。
常见的有1,3-丁二烯(CH2=CH-CH=CH2)和2-甲基-1,3-丁二烯
因有碳碳双键、性质与烯烃相似,因有二个碳碳双键、质与烯烃也有差异。
二烯烃的主要反应:
1、加成反应
2、加聚反应
天然橡胶的主要成分也是聚异戊二烯。
考点3-3乙烯
【考点整理】
一、石蜡油分解制取乙烯实验
实验现象:
①生成的气体能使酸性高锰酸钾溶液褪色;
②生成的气体能使溴的四氯化碳溶液褪色;
③点燃集气法收集到的气体,有明亮的火焰和黑烟。
研究表明,石蜡油分解的产物主要是乙烯和烷烃的混合物。
二、分子结构特点
分子式:
C2H4,结构式:
,结构简式:
CH2=CH2
乙烯的结构特点:
①乙烯是平面结构,不能旋转。
②C=C中的2个键并不完全相同,其中有一个键是不稳定的,容易断裂而被氧化或被加成;
另有一个键则较稳定。
三、性质:
无色、稍有气味的气体,难溶于水。
易氧化、易加成(加聚)
(1)氧化反应
①与酸性高锰酸钾反应(特征反应)
现象:
酸性高锰酸钾溶液褪色。
(乙烯被酸性高锰酸钾氧化成CO2)
②可燃性:
(火焰明亮,伴有黑烟)
(2)加成反应
有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应叫做加成反应。
乙烯能与Cl2、Br2、H2、HX(卤化氢)、H2O发生加成反应。
CH2=CH2+Br2
CH2Br―CH2Br(1,2—二溴乙烷)(现象:
溴水褪色)
CH2=CH2+H2
CH3CH3
CH2=CH2+HCl
CH3CH2Cl
CH2=CH2+H2O
CH3CH2OH(工业上生产酒精)
通过有机物发生加成反应时反应物之间的量关系,还可定量判断该有机物分子结构中不饱和键的情况:
是C=C键,还是C≡C键,或是苯环结构,以及它们的个数。
(3)加聚反应
①加聚反应:
在聚合反应中,由不饱和(即含碳碳双键或三键)的相对分子质量小的化合物分子通过加成聚合的形式结合成相对分子质量很大的高分子化合物的反应。
②高分子化合物:
相对分子质量很大(1万以上)的物质,简称高分子或高聚物。
聚乙烯,塑料,分子量达几万到几十万,性质坚韧,化学性质稳定,难降解。
四、用途
①乙烯的产量作为衡量石油化工水平的标志,是石油裂解的主要产品。
②乙烯是石油化学工业中生产塑料、合成纤维、洗涤剂、乙醇等的最重要基础原料。
③乙烯还用作植物生长调节剂、水果催熟剂、杀虫剂等。
附参考答案
一、1.AC2.C3.BD4.B5.C6.B7.C8.AC9.C
12.
(1)ABAD
(2)品红溶液褪色
(3)除去SO2,以免干扰乙烯的性质实验
(4)检验SO2是否除尽
(5)装置③中的品红溶液不褪色,装置④中的酸性KMnO4溶液褪色
13.
(1)9.25g0.826g·
L-1
(2)4.44%
14.解析:
(1)由0.857可求出A的分子式C10H20;
(3)实际考丁基的4种异构体
答案:
(1)C10H20
(2)CH3—C(CH3)2—CH==CH—C(CH3)2—CH3CH3—C(CH3)2—COOH
(3)4