有机化学课后答案文档格式.docx
《有机化学课后答案文档格式.docx》由会员分享,可在线阅读,更多相关《有机化学课后答案文档格式.docx(41页珍藏版)》请在冰豆网上搜索。
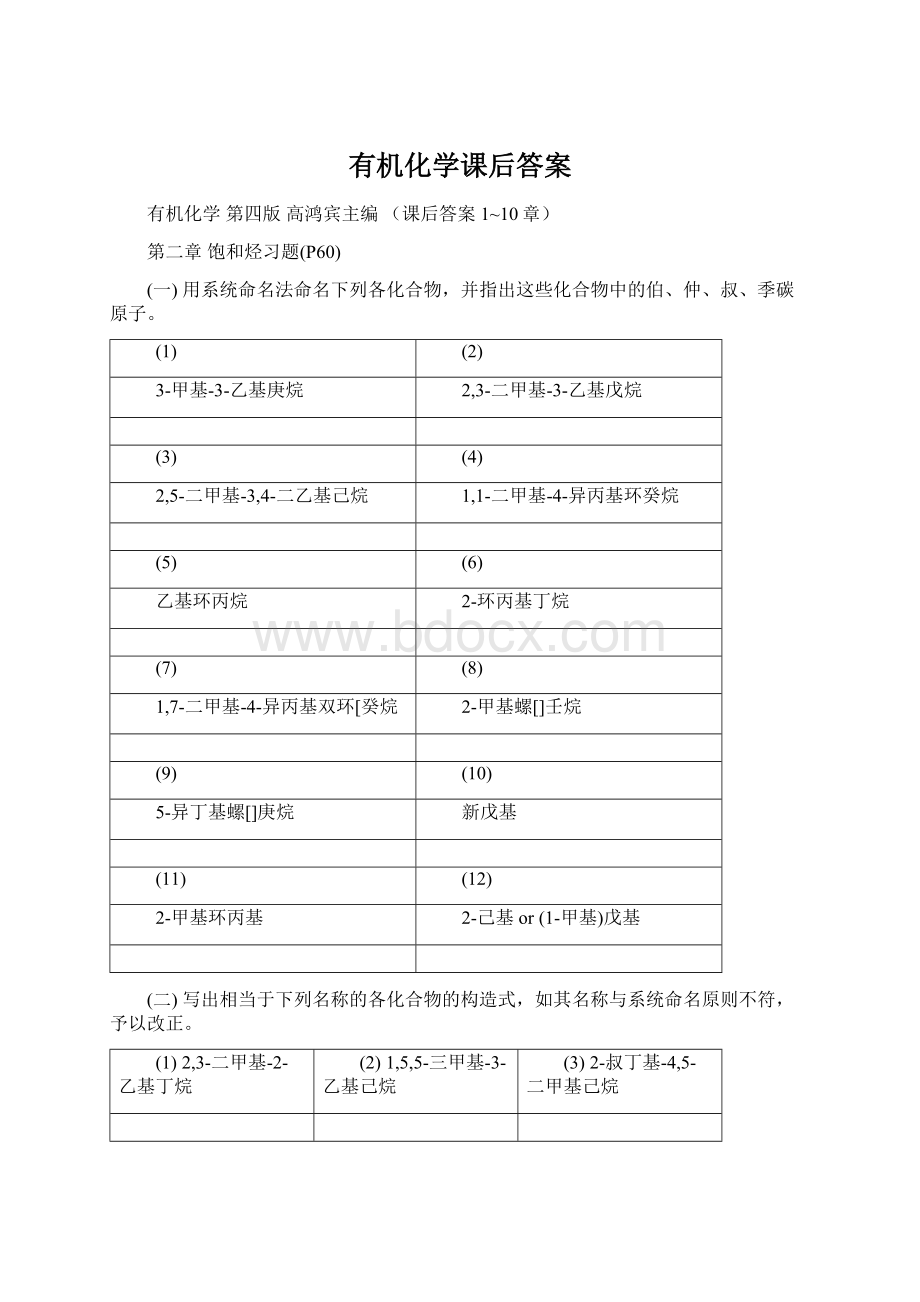
1-环丙基丁烷
1-甲基-3-丁基环己烷
(三)以C2与C3的σ键为旋转轴,试分别画出2,3-二甲基丁烷和2,2,3,3-四甲基丁烷的典型构象式,并指出哪一个为其最稳定的构象式。
解:
2,3-二甲基丁烷的典型构象式共有四种:
2,2,3,3-四甲基丁烷的典型构象式共有两种:
(四)将下列的投影式改为透视式,透视式改为投影式。
(五)用透视式可以画出三种CH3-CFCl2的交叉式构象:
它们是不是CH3-CFCl2的三种不同的构象式用Newman投影式表示并验证所得结论是否正确。
它们是CH3-CFCl2的同一种构象——交叉式构象!
从下列Newman投影式可以看出:
将(I)整体按顺时针方向旋转60º
可得到(II),旋转120º
可得到(III)。
同理,将(II)整体旋转也可得到(I)、(III),将(III)整体旋转也可得到(I)、(II)。
(六)试指出下列化合物中,哪些所代表的是相同的化合物而只是构象表示式之不同,哪些是不同的化合物。
(1)
(2)(3)
(4)(5)(6)
⑴、⑵、⑶、⑷、⑸是同一化合物:
2,3-二甲基-2-氯丁烷;
⑹是另一种化合物:
2,2-二甲基-3-氯丁烷。
(七)如果将船型和椅型均考虑在环己烷的构象中,试问甲基环己烷有几个构象异构体其中哪一个最稳定哪一个最不稳定为什么
按照题意,甲基环己烷共有6个构象异构体:
(A)
(B)
(C)
(D)
(E)
(F)
其中最稳定的是(A)。
因为(A)为椅式构象,且甲基在e键取代,使所有原子或原子团都处于交叉式构象;
最不稳定的是(C)。
除了船底碳之间具有重叠式构象外,两个船头碳上的甲基与氢也具有较大的非键张力。
(八)不参阅物理常数表,试推测下列化合物沸点高低的一般顺序。
(1)(A)正庚烷(B)正己烷(C)2-甲基戊烷(D)2,2-二甲基丁烷(E)正癸烷
沸点由高到低的顺序是:
正癸烷>正庚烷>正己烷>2-甲基戊烷>2,2-二甲基丁烷
(2)(A)丙烷(B)环丙烷(C)正丁烷(D)环丁烷(E)环戊烷(F)环己烷
(G)正己烷(H)正戊烷
F>G>E>H>D>C>B>A
(3)(A)甲基环戊烷(B)甲基环己烷(C)环己烷(D)环庚烷
D>B>C>A
(九)已知烷烃的分子式为C5H12,根据氯化反应产物的不同,试推测各烷烃的构造,并写出其构造式。
(1)一元氯代产物只能有一种
(2)一元氯代产物可以有三种
(3)一元氯代产物可以有四种(4)二元氯代产物只可能有两种
(1)
(2)
(3)(4)
(十)已知环烷烃的分子式为C5H10,根据氯化反应产物的不同,试推测各环烷烃的构造式。
(1)一元氯代产物只有一种
(2)一元氯代产物可以有三种
(1)
(2)
(十一)等物质的量的乙烷和新戊烷的混合物与少量的氯反应,得到的乙基氯和新戊基氯的摩尔比是1∶。
试比较乙烷和新戊烷中伯氢的相当活性。
设乙烷中伯氢的活性为1,新戊烷中伯氢的活性为x,则有:
∴新戊烷中伯氢的活性是乙烷中伯氢活性的倍。
(十二)在光照下,2,2,4-三甲基戊烷分别与氯和溴进行一取代反应,其最多的一取代物分别是哪一种通过这一结果说明什么问题并根据这一结果预测异丁烷一氟代的主要产物。
2,2,4-三甲基戊烷的构造式为:
氯代时最多的一氯代物为;
溴代时最多的一溴代物为
这一结果说明自由基溴代的选择性高于氯代。
即溴代时,产物主要取决于氢原子的活性;
而氯代时,既与氢原子的活性有关,也与各种氢原子的个数有关。
根据这一结果预测,异丁烷一氟代的主要产物为:
FCH2CH2CH3
(十三)将下列的自由基按稳定性大小排列成序。
⑴⑵⑶⑷
自由基的稳定性顺序为:
⑶>⑷>⑵>⑴
(十四)在光照下,甲基环戊烷与溴发生一溴化反应,写出一溴代的主要产物及其反应机理。
反应机理:
引发:
增长:
……
终止:
(十五)在光照下,烷烃与二氧化硫和氯气反应,烷烃分子中的氢原子被氯磺酰基取代,生成烷基磺酰氯:
此反应称为氯磺酰化反应,亦称Reed反应。
工业上常用此反应由高级烷烃生产烷基磺酰氯和烷基磺酸钠(R-SO2ONa)(它们都是合成洗涤剂的原料)。
此反应与烷烃氯化反应相似,也是按自由基取代机理进行的。
试参考烷烃卤化的反应机理,写出烷烃(用R-H表示)氯磺酰化的反应机理。
第三章不饱和烃习题(P112)
(一)用系统命名法命名下列各化合物:
(2)对称甲基异丙基乙烯
3-甲基-2-乙基-1-丁烯
4-甲基-2-戊烯
2,2,5-三甲基-3-己炔
3-异丁基-4-己烯-1-炔
(二)用Z,E-标记法命名下列各化合物:
(1)↓↑
(2)↑↑
(E)-2,3-二氯-2-丁烯
(Z)-2-甲基-1-氟-1-氯-1-丁烯
(3)↑↑
(4)↑↑
(Z)-1-氟-1-氯-2-溴-2-碘乙烯
(Z)-3-异基-2-己烯
(三)写出下列化合物的构造式,检查其命名是否正确,如有错误予以改正,并写出正确的系统名称。
(1)顺-2-甲基-3-戊烯
(2)反-1-丁烯
顺-4-甲基-3-戊烯
1-丁烯(无顺反异构)
(3)1-溴异丁烯
(4)(E)-3-乙基-3-戊烯
2-甲基-1-溴丙烯
3-乙基-2-戊烯(无顺反异构)
(四)完成下列反应式:
红色括号中为各小题所要求填充的内容。
(硼氢化反应的特点:
顺加、反马、不重排)
(13)
(14)
(五)用简便的化学方法鉴别下列各组化合物:
(六)在下列各组化合物中,哪一个比较稳定为什么
(1)(A),(B)
(B)中甲基与异丙基的空间拥挤程度较小,更加稳定。
(2)(A),(B)
(A)中甲基与碳-碳双键有较好的σ-π超共轭,故(A)比较稳定。
(3)(A),(B),(C)
(C)的环张力较小,较稳定。
(4)(A),(B)
(A)的环张力较小,较稳定。
(5)(A),(B),(C)
(C)最稳定。
(6)(A),(B)
(A)的环张力很大,所以(B)较稳定。
(七)将下列各组活性中间体按稳定性由大到小排列成序:
(1)C>A>B
(2)B>C>A
(八)下列第一个碳正离子均倾向于重排成更稳定的碳正离子,试写出其重排后碳正离子的结构。
题给碳正离子可经重排形成下列碳正离子:
(九)在聚丙烯生产中,常用己烷或庚烷作溶剂,但要求溶剂中不能有不饱和烃。
如何检验溶剂中有无不饱和烃杂质若有,如何除去
可用Br2/CCl4或者KMnO4/H2O检验溶剂中有无不饱和烃杂质。
若有,可用浓硫酸洗去不饱和烃。
(十)写出下列各反应的机理:
(1)
(2)
(3)
该反应为自由基加成反应:
略。
(箭头所指方向为电子云的流动方向!
)
(十一)预测下列反应的主要产物,并说明理由。
双键中的碳原子采取sp2杂化,其电子云的s成分小于采取sp杂化的叁键碳,离核更远,流动性更大,更容易做为一个电子源。
所以,亲电加成反应活性:
>
解释:
在进行催化加氢时,首先是H2及不饱和键被吸附在催化剂的活性中心上,而且,叁键的吸附速度大于双键。
所以,催化加氢的反应活性:
叁键>双键。
叁键碳采取sp杂化,其电子云中的s成分更大,离核更近,导致其可以发生亲核加成。
而双键碳采取sp2杂化,其电子云离核更远,不能发生亲核加成。
解释:
双键上电子云密度更大,更有利于氧化反应的发生。
氧化反应总是在电子云密度较大处。
解释:
C+稳定性:
3°
C+>2°
C+
(十二)写出下列反应物的构造式:
(十三)根据下列反应中各化合物的酸碱性,试判断每个反应能否发生(pKa的近似值:
ROH为16,NH3为34,RC≡CH为25,H2O为
所以,该反应能够发生。
所以,该反应不能发生。
(十四)给出下列反应的试剂和反应条件:
(1)1-戊炔→戊烷
(2)3-己炔→顺-3-己烯
(3)2–戊炔→反-2-戊烯
(十五)完成下列转变(不限一步):
(十六)由指定原料合成下列各化合物(常用试剂任选):
(1)由1-丁烯合成2-丁醇
(2)由1-己烯合成1-己醇
(4)由乙炔合成3-己炔
(5)由1-己炔合成正己醛
(6)由乙炔和丙炔合成丙基乙烯基醚
(十七)解释下列事实:
(1)1-丁炔、1-丁烯、丁烷的偶极矩依次减小,为什么
电负性:
>>
键的极性:
分子的极性:
1-丁炔>1-丁烯>丁烷(即:
1-丁炔、1-丁烯、丁烷的偶极矩依次减小)
(2)普通烯烃的顺式和反式异构体的能量差为•mol-1,但4,4-二甲基-2-戊烯顺式和反式的能量差为kJ•mol-1,为什么
顺-4,4-二甲基-2-戊烯反-4,4-二甲基-2-戊烯
由于叔丁基的体积大,空间效应强,导致在顺-4,4-二甲基-2-戊烯中,叔丁基与甲基处于双键同侧,空间障碍特别大,能量更高。
(3)乙炔中的键比相应乙烯、乙烷中的键键能增大、键长缩短,但酸性却增强了,为什么
炔烃分子中的叁键碳采取sp杂化。
与sp2、sp3杂化碳相比,sp杂化s成分更多,电子云离核更近,受核的束缚更强,电负性更大。
由于sp杂化碳的电子云离核更近,使乙炔中的键键能增大、键长缩短;
由于sp杂化碳的电负性更大,使中的电子云更偏向碳原子一边,导致乙炔分子中氢原子更容易以H+的形式掉下来,酸性增强。
(4)炔烃不但可以加一分子卤素,而且可以加两分子卤素,但却比烯烃加卤素困难,反应速率也小,为什么
烯烃、炔烃与卤素的加成反应是亲电加成,不饱和键上的电子云密度越大,越有利于亲电加成。
由于炔烃中的叁键碳采取sp杂化,电负性较大。
所以,炔烃与卤素加成时,比烯烃加卤素困难,反应速率也小于烯烃。
(5)与亲电试剂Br2、Cl2、HCl的加成反应,烯烃比炔烃活泼。
然而当炔烃用这些试剂处理时,反应却很容易停止在烯烃阶段,生成卤代烯烃,需要更强烈的条件才能进行第二步加成。
这是否相互矛盾,为什么
不矛盾。
烯烃与Br2、Cl2、HCl的加成反应都是亲电加成。
由于双键碳的电负性小于叁键碳,导致双键上的π电子受核的束缚程度更小,流动性更大,更有利于亲电加成反应。
所以,与亲电试剂Br2、Cl2、HCl的加成反应,烯烃比炔烃活泼
而、都是吸电子基,它们的引入,导致双键上电子云密度降低,不利于亲电加成反应的进行。
所以,当炔烃用亲电试剂Br2、Cl2、HCl处理时,反应却很容易停止在烯烃阶段,生成卤代烯烃,需要更强烈的条件才能进行第二步加成
(6)在硝酸钠的水溶液中,溴对乙烯的加成,不仅生成1,2-二溴乙烷,而且还产生硝酸-β-溴代乙酯(BrCH2CH2ONO2),怎样解释这样的反应结果试写出各步反应式。
溴与乙烯的加成是亲电加成反应,首先生成活性中间体——环状溴翁正离子。
后者可与硝酸根负离子结合得到硝酸-β-溴代乙酯(BrCH2CH2ONO2):
(7)(CH3)3CCH=CH2在酸催化下加水,不仅生成产物(A),而且生成(B),但不生成(C)。
试解释为什么。
该实验现象与烯烃酸催化下的水合反应机理有关:
(2°
C+)(3°
C+)
与(C)相关的C+为(1°
C+),能量高,不稳定,因此产物(C)不易生成。
(8)丙烯聚合反应,无论是酸催化还是自由基引发聚合,都是按头尾相接的方式,生成甲基交替排列的整齐聚合物,为什么
以自由基聚合为例。
若按头尾相接的方式,生成甲基交替排列的整齐聚合物,则与之相关的自由基都是二级自由基:
二级自由基二级自由基
二级自由基
头尾相接、甲基交替排列的整齐聚合物
反之,则会生成稳定性较差的一级自由基:
二级自由基一级自由基
丙烯在酸催化下进行聚合反应,其活性中间体为碳正离子,其稳定性顺序同样为:
三级>二级>一级碳正离子。
(十八)化合物(A)的分子式为C4H8,它能使溴溶液褪色,但不能使稀的高锰酸钾溶液褪色。
1mol(A)与1molHBr作用生成(B),(B)也可以从(A)的同分异构体(C)与HBr作用得到。
(C)能使溴溶液褪色,也能使稀和酸性高锰酸钾溶液褪色。
试推测(A)、(B)和(C)的构造式。
并写出各步反应式。
(A)(B)
(C)或
反应式略。
(十九)分子式为C4H6的三个异构体(A)、(B)、(C),可以发生如下的化学反应:
(1)三个异构体都能与溴反应,但在常温下对等物质的量的试样,与(B)和(C)反应的溴量是(A)的2倍;
(2)三者都能HCl发生反应,而(B)和(C)在Hg2+催化下与HCl作用得到的是同一产物;
(3)(B)和(C)能迅速地与含HgSO4的硫酸溶液作用,得到分子式为C4H8O的化合物;
(4)(B)能与硝酸银的溶液反应生成白色沉淀。
试写出化合物(A)、(B)和(C)的构造式,并写出有关的反应式。
(A)(B)(C)
有关的反应式略。
(二十)某化合物(A)的分子式为C7H14,经酸性高锰酸钾溶液氧化后生成两个化合物(B)和(C)。
(A)经臭氧化而后还原水解也得相同产物(B)和(C)。
试写出(A)的构造式。
(二十一)卤代烃C5H11Br(A)与氢氧化钠的乙醇溶液作用,生成分子式为C5H10的化合物(B)。
(B)用高锰酸钾的酸性水溶液氧化可得到一个酮(C)和一个羧酸(D)。
而(B)与溴化氢作用得到的产物是(A)的异构体(E)。
试写出(A)、(B)、(C)、(D)和(E)的构造式及各步反应式。
各步反应式:
(二十二)化合物C7H15Br经强碱处理后,得到三种烯烃(C7H14)的混合物(A)、(B)和(C)。
这三种烯烃经催化加氢后均生成2-甲基己烷。
(A)与B2H6作用并经碱性过氧化氢处理后生成醇(D)。
(B)和(C)经同样反应,得到(D)和另一异构醇(E)。
写出(A)~(E)的结构式。
再用什么方法可以确证你的推断
C7H15Br的结构为:
(A)~(E)的结构式:
将(A)、(B)、(C)分别经臭氧化-还原水解后,测定氧化产物的结构,也可推断(A)、(B)、(C)的结构:
(二十三)有(A)和(B)两个化合物,它们互为构造异构体,都能使溴的四氯化碳溶液褪色。
(A)与Ag(NH3)2NO3反应生成白色沉淀,用KMnO4溶液氧化生成丙酸(CH3CH2COOH)和二氧化碳;
(B)不与Ag(NH3)2NO3反应,而用KMnO4溶液氧化只生成一种羧酸。
试写出(A)和(B)的构造式及各步反应式。
(二十四)某化合物的分子式为C6H10。
能与两分子溴加成而不能与氧化亚铜的氨溶液起反应。
在汞盐的硫酸溶液存在下,能与水反应得到4-甲基-2-戊酮和2-甲基-3-戊酮的混合物。
试写出C6H10的构造式。
(二十五)某化合物(A),分子式为C5H8,在液氨中与金属钠作用后,再与1-溴丙烷作用,生成分子式为C8H14的化合物(B)。
用高锰酸钾氧化(B)得到分子式C4H8O2为的两种不同的羧酸(C)和(D)。
(A)在硫酸汞存在下与稀硫酸作用,可得到分子式为C5H10O的酮(E)。
试写出(A)~(E)的构造式及各步反应式。
第四章二烯烃和共轭体系习题(P147)
(一)用系统命名法命名下列化合物:
4-甲基-1,3-戊二烯
2-甲基-2,3-戊二烯
2-甲基-1,3,5-己三烯
(3Z)-1,3-戊二烯
(二)下列化合物有无顺反异构现象:
若有,写出其顺反异构体并用Z,E-命名法命名。
(1)无;
(2)有;
(3E)-1,3-戊二烯,(3Z)-1,3-戊二烯;
(3)有;
(3Z,5Z)-3,5-辛二烯,(3Z,5E)-3,5-辛二烯,(3E,5E)-3,5-辛二烯;
(4)有;
(3E)-1,3,5-己三烯,(3Z)-1,3,5-己三烯;
(5)无
(三)完成下列反应式:
(四)给出下列化合物或离子的极限结构式,并指出哪个贡献最大
(2)(3)
(4)(5)(6)
(1)
贡献最大(非电荷分离)
结构相似,二者贡献一样大
(3)
结构相似,二者贡献一样大
各共振结构式结构相似,能量相同,对真实结构的贡献相同。
贡献最大(与电负性预计相同)
贡献最大(共价键最多)
(五)化合物和同相比,前者C=C双键的电子云密度降低,而后者C=C双键的电子云密度升高。
试用共振论解之。
的真实结构可用共振论表示如下:
其中(II)对真实结构的贡献就是使C=C双键带部分正电荷,电子云密度降低。
其中(II)对真实结构的贡献就是使C=C双键带部分负电荷,电子云密度升高。
(六)解释下列反应:
(七)某二烯烃与一分子溴反应生成2,5-二溴-3-己烯,该二烯烃若经臭氧化再还原分解则生成两分子乙醛和一分子乙二醛(O=CH-CH=O)。
试写出该二烯烃的构造式及各步反应式。
该二烯烃的构造式为:
2,4-己二烯
各步反应式略。
(八)3-甲基-1,3-丁二烯与一分子氯化氢加成,只生成3-甲基-3-氯-1-丁烯和3-甲基-1-氯-2-丁烯,而没有2-甲基-3-氯-1-丁烯和3-甲基-1-氯-2-丁烯。
试简单解释之,并写出可能的反应机理。
由于C+稳定性:
所以,只有与相关的产物生成:
(九)分子式为C7H10的某开链烃(A),可发生下列反应:
(A)经催化加氢可生成3-乙基戊烷;
(A)与硝酸银氨溶液反应可产生白色沉淀;
(A)在Pd/BaSO4催化下吸收1molH2生成化合物(B),(B)能与顺丁烯二酸酐反应生成化合物(C)。
试写出(A)、(B)、(C)的构造式。
(十)下列各组化合物分别与HBr进行亲电加成反应,哪个更容易试按反应活性大小排列顺序。
,,
1,3-丁二烯,2-丁烯,2-丁炔
(1)反应活性顺序:
>>>
(考虑C+稳定性!
(2)反应活性顺序为:
1,3-丁二烯>2-丁烯>2-丁炔(考虑C+稳定性!
(十一)下列两组化合物分别与1,3-丁二烯[
(1)组]或顺丁烯二酸酐[
(2)组]进行Diels-Alder反应,试将其按反应活性由大到小排列成序。
(A)(B)(C)
反应活性:
(1)B>C>A;
(2)A>B>C(C难以形成s-顺式构型,不反应)
(十二)试用简单的化学方法鉴别下列各组化合物:
(1)己烷,1-己烯,1-己炔,2,4-己二烯
(2)庚烷,1-庚炔,1,3-庚二烯,1,5-庚二烯
(十三)选用适当原料,通过Diels-Alder反应合成下列化合物。
(3)
(十四)三个化合物(A)、(B)和(C),其分子式均为C5H8,都可以使溴的四氯化碳溶液褪色,在催化下加氢都得到戊烷。
(A)与氯化亚铜碱性氨溶液作用生成棕红色沉淀,(B)和(C)则不反应。
(C)可以顺丁烯二酸酐反应生成固体沉淀物,(A)和(B)则不能。
试写出(A)、(B)和(C)可能的构造式。
(A)(B)or
(C)
(十五)1,2-丁二烯聚合时,除生成高分子聚合物外,还有一种二聚体生成。
该二聚体可以发生如下的反应:
(1)还原后可以生成乙基环己烷;
(2)溴化时可以加上两分子溴;
(3)氧化时可以生成β-羧基己二酸
根据以上事实,试推测该二聚体的构造式,并写出各步反应式。
该二聚体的构造式为:
第五章芳烃芳香性
(一)写出分子式为C9H12的单环芳烃的所有同分异构体并命名。
(二)命名下列化合物:
(1)
(2)(3)
(7)(8)(9)
(1