第31课时 水和溶液Word格式.docx
《第31课时 水和溶液Word格式.docx》由会员分享,可在线阅读,更多相关《第31课时 水和溶液Word格式.docx(14页珍藏版)》请在冰豆网上搜索。
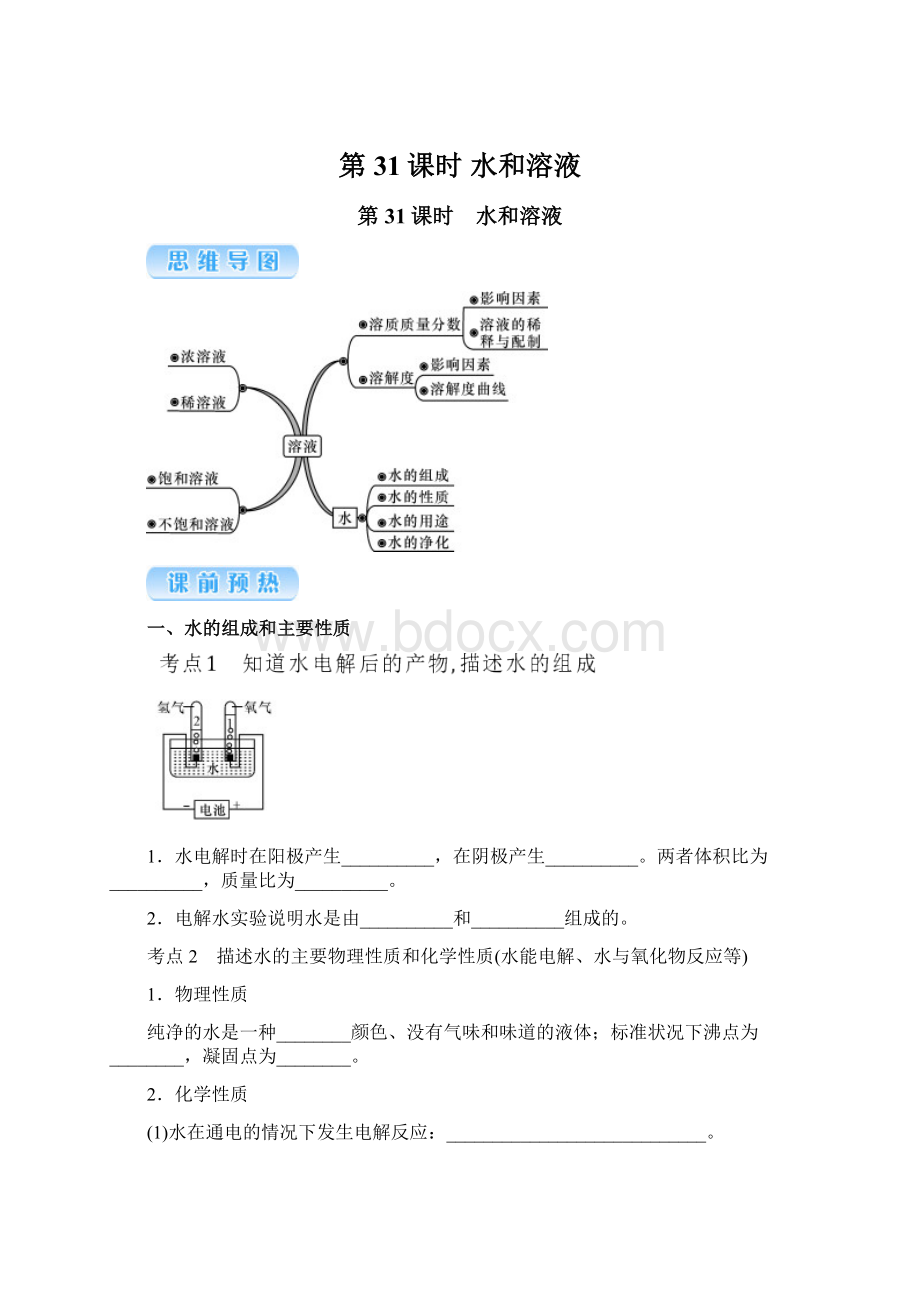
溶液
浊液
悬浊液
乳浊液
不
同
点
组成
由溶质和溶剂组成(水是最常见的溶剂)
不溶性固体和液体组成
不溶性液体和液体组成
分散
微粒
分子或离子直径小于10-9米
大量分子的集合体,乳浊液的颗粒大约为1~50微米
均一性
_______、透明
不均一、不透明(浑浊)
稳定性
稳定
不稳定、久置后分层
相同点
都是________物
3.(2019·
兰州)下列有关溶液的叙述正确的是( )
A.食盐水倒出一半后浓度降低
B.果粒橙属于溶液
C.升温会降低二氧化碳在水中的溶解度
D.蔗糖可以无限溶解在一定量的水中
4.概念图能清晰地反映概念之间的联系,如图表示溶液中部分概念的相互联系。
请回答:
(1)图中“?
”是指_______。
(2)将5克食盐固体放入盛有20克蒸馏水的烧杯中,充分搅拌后完全溶解。
你是如何确定食盐固体“完全溶解”的?
_________。
三、饱和溶液与不饱和溶液、
溶解度
1.饱和溶液与不饱和溶液
在一定温度下,在一定量的溶剂里,________某种溶质的溶液称为这种溶质的_________,还能继续溶解某种溶质的溶液称为这种溶质的_______________。
2.饱和溶液和不饱和溶液一般情况下可相互转化。
饱和溶液
不饱和溶液
影响溶解性的因素有:
①溶质、溶剂自身的性质;
②_________;
③气体的溶解度还受__________的影响。
考点8 说出物质的溶解度的含义(不要求溶解度的计算)
溶解度:
在一定温度中,溶质在_________水中达到_________状态时所溶解的克数,就称作为该温度下某物质的__________。
5.(2019·
金华、义乌、丽水)甲是60℃的蔗糖溶液,按如图所示进行操作。
以下分析错误的是( )
A.甲一定是不饱和溶液
B.丙和丁一定是饱和溶液
C.乙的溶质质量分数一定比甲大
D.甲和丙的溶质质量分数一定不相等
6.(2018·
宁波)20℃时,四个实验小组分别取不同质量的NaCl,逐渐加入到各盛有50g水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余NaCl的质量。
记录数据如下表:
实验小组
第一组
第二组
第三组
第四组
水的质量/g
50
所取NaCl的质量/g
15
20
25
30
剩余NaCl的质量/g
2
7
12
A.20℃时,50gNaCl饱和溶液中含有18gNaCl
B.用蒸发的方法可以使不饱和溶液变成饱和溶液
C.第二组所得溶液的溶质与溶剂的质量比为9∶25
D.相同温度下,NaCl在水里的溶解度与水的质量无关
四、溶质的质量分数
1.溶液中溶质质量分数:
溶质质量与_________质量之比。
2.意义:
能定量表示溶液的组成,可用小数或百分数表示。
考点10 应用“溶质的质量分数=(溶质质量/溶液质量)”进行简单计算
计算:
溶液中溶质的质量分数=
×
100%=
100%
考点11 按要求配制一定溶质质量分数的溶液,说明有关配制方案、步骤与操作方法
1.实验仪器:
天平、玻璃棒、量筒、药匙、烧杯、胶头滴管。
2.实验步骤:
______________________。
7.硫酸镁在工农业以及医疗上有广泛应用,其溶解度如下表所示。
则下列说法正确的是( )
温度/℃
10
70
90
溶解度/g
27.7
39.3
49.0
54.1
51.1
A.硫酸镁的溶解度随温度升高而增大
B.10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液
C.50℃时,100g硫酸镁饱和溶液中溶质和溶剂的质量比为49∶100
D.70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大
8.(2019·
宁波)图甲是一种稀释瓶,用户可以根据需求用它以一定体积比对原液进行稀释,图乙是它的7种不同比例的稀释方式。
小科用该稀释瓶按1∶2的比例稀释原液,原液是密度为1.5g/mL、溶质质量分数为50%的NaOH溶液。
稀释过程中,不考虑温度变化和混合前后的体积变化。
(1)当水加到1∶1的刻度线时,水对稀释瓶底的压强为p1,当水加到1∶2的刻度线时,水对稀释瓶底的压强为p2,则p1________p2。
(填“>”、“<”或“=”)
(2)稀释得到的NaOH溶液的密度为________g/mL,溶质质量分数为________。
(计算结果分别精确到0.1g/mL和0.1%)
五、水污染
水污染的主要来源:
工业生产中的“三废”;
生活污水的任意排放;
农业生产中的农药、化肥的流失。
考点13 列举吸附、沉淀、过滤、蒸馏等水净化的方法
水的净化方法:
沉淀法、_________、蒸馏法。
考点14 树立水是生命之源的观点,树立节约用水的意识,增强防止水污染的责任感
水污染的防治;
加强对水质的监测;
工业“三废”经过处理后再排放;
农业生产中要合理使用化肥和农药等。
9.(2018·
台州)如图为自来水生产过程示意图。
下列说法正确的是( )
A.清水池中的水是溶液
B.过滤池中主要发生化学变化
C.消毒用的液氯是化合物
D.供水系统流出的水是纯净物
(2019·
眉山)下列有关溶液的说法正确的是( )
A.长期放置不分层的液体一定是溶液
B.溶质可以是固体,也可以是液体或气体
C.降低饱和溶液的温度,一定有晶体析出
D.配制好的6%的NaCl溶液,装入试剂瓶中时不慎洒漏一部分,浓度减小
葫芦岛)把少量下列物质分别放入足量的水中充分搅拌,可以得到溶液的是( )
A.白糖B.泥沙
C.牛奶D.花生油
20℃时氯化钾的溶解度为34g。
下列是四位同学在20℃时配制的氯化钾溶液,其中一定达到饱和的是( )
温州)如图,将红砂糖倒入一杯开水中,充分溶解。
能作为判断砂糖水是饱和溶液的依据是( )
A.砂糖水颜色很深B.砂糖水味道很甜
C.砂糖溶解得很快D.砂糖固体有剩余
(2018·
滨州)小芳在配制一定溶质质量分数的氯化钠溶液时,没有按照正确的操作规程进行称量氯化钠、量取水的操作(如图为小芳操作时的读数,其他操作都正确)。
小芳实际配制的氯化钠溶液的溶质质量分数(水的密度为1g/cm3)约为( )
A.12.4%B.17.2%
C.16.9%D.12.5%
绍兴)下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
40
溶解度/克
13.3
20.9
31.6
45.8
63.9
(1)10℃时,100克水中最多可溶解硝酸钾的质量为________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为________。
(3)如图是硝酸钾溶液的变化情况,请写出一种可行的操作方法。
(写出计算过程)
【提醒】解答本题关键是知道酒精具有挥发性,氧化钙能与水反应,饱和溶液析出晶体的过程。
许多化学反应都是在溶液中进行的,关于溶液理解正确的是( )
A.通过加热蒸发的方法提高75%酒精的浓度
B.将氧化钙溶于水,可以形成氧化钙溶液
C.5gCuSO4·
5H2O溶于95g水中配制CuSO4溶液,此溶液溶质的质量分数小于5%
D.将50℃下的饱和KNO3溶液冷却至室温,硝酸钾固体析出,过滤后可得纯水和硝酸钾固体
【提醒】此题是对溶质质量分数的扩展与延伸,使学生明确溶质的质量分数是溶质与溶液的比值,而与其他因素无关的道理。
30℃时将等质量的两份饱和石灰水,一份冷却到20℃,另一份加入少量生石灰,温度仍保持在30℃。
则两种情况下均不改变的是( )
A.溶剂的质量B.溶质的质量
C.溶质的溶解度D.溶液中溶质的质量分数
金华、义乌、丽水)为研究“不同物质在敞口容器久置后的质量变化”,某科学兴趣小组将10.00克下列物质分别盛放于相同的烧杯中,将它们敞口放置在恒温实验室。
一段时间后,测得烧杯中物质减少的质量情况如下表。
放置时间
(小时)
烧杯中物质减少的质量(克)
水
饱和氯化钠溶液
饱和硝酸钾溶液
7.3%的稀盐酸
24
1.85
0.61
0.72
1.35
48
3.70
?
1.44
2.80
(1)表格中“?
”的值是________克。
(2)与原饱和硝酸钾溶液相比较,敞口放置24小时的硝酸钾溶液溶质质量分数________(填“变大”、“变小”或“不变”)。
(3)分析上表中水、饱和硝酸钾溶液和稀盐酸敞口放置后质量减少程度随时间变化不一样,为进一步研究稀盐酸在敞口容器中久置后的溶质质量分数变化,小丽进行了下列操作:
取敞口放置时间48小时的稀盐酸5.00克于锥形瓶中,滴入两滴指示剂,用溶质质量分数为8%的氢氧化钠溶液逐滴滴入稀盐酸中,至恰好完全反应,共消耗5.50克氢氧化钠溶液。
通过计算,确定敞口放置48小时的稀盐酸溶质质量分数是“变大”、“变小”还是“不变”?
并对变化的原因作出解释。
(友情提示:
本栏目建议午休时间完成)
遵义)实验室配制一定溶质质量分数的氢氧化钠溶液,下列操作正确的是( )
嘉兴、舟山)20℃时,把36克氯化钠放入64克水中,使其充分溶解(20℃时氯化钠的溶解度为36克)。
对所得溶液的有关说法错误的是( )
A.该溶液是饱和溶液
B.溶液中Na+和Cl-个数一定相等
C.溶液质量为100克
D.溶质与溶剂质量比为9∶25
河北)常温下,对100mL氯化钠饱和溶液进行如图所示实验。
下列分析错误的是( )
第3题图
A.实验1后,甲、乙中溶液的溶质质量分数相等
B.实验2后,乙中比甲中氯化钠的溶解度大
C.实验2后,甲中溶液为氯化钠的不饱和溶液
D.实验2后,甲、乙中溶液所含溶质质量相等
4.(2019·
滨州)某同学选用氢氧化钠固体与水配制20g溶质质量分数为10%的氢氧化钠溶液,下列说法错误的是( )
①需称取氢氧化钠固体2.0g
②称量前托盘天平应先检查游码是否归零,并调节平衡
③用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
④选用250mL量筒量取18mL的水
⑤存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A.①④B.③④⑤C.④⑤D.②③⑤
第5题图
黄石)在蒸馏水中加入NaOH颗粒,不断搅拌,用温度传感器记录溶解过程的温度变化如图,a、c两点观察到溶液中有固体存在,b点固体完全消失。
下列说法不正确的是( )
A.NaOH固体溶于水是放热过程
B.a、c两点时,NaOH的溶解度相同
C.b点时,该溶液一定是饱和溶液
D.c点时的溶剂质量等于a点时的溶剂质量
(2018·
衡阳)实验室配制100g溶质质量分数为8%的氯化钠溶液,下列说法中错误的是( )
A.若在量取水时俯视凹液面的最低处,则配制溶液的质量分数小于8%
B.溶解过程中玻璃棒搅拌的作用是加快氯化钠的溶解速率
C.实验的步骤为计算、称量、量取、溶解、装瓶贴标签
D.量取水时,用规格为100mL的量筒
7.(2019·
贵港)已知甲物质的溶解度与温度的关系如下表所示:
10.0
18.0
36.0
56.0
按如图步骤进行操作:
第7题图
(1)甲属于________(填“易”或“可”)溶性物质,它的溶解度随温度的升高而________。
(2)在A-E的溶液中,属于不饱和溶液的是________(填序号,下同),与B溶液的溶质质量分数相同的是________。
(3)要使E中未溶的甲物质全部溶解,至少需要加入30℃的水________g。
8.(2018·
长春)在实验室里配制100g溶质的质量分数为10%的NaCl溶液。
(1)用NaCl固体和蒸馏水配制溶液时,用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和__量筒__。
(2)用浓溶液配制稀溶液时,计算的依据是稀释前后__溶质__的质量保持不变。
(3)下列配制方法可以达到上述实验目的的是________。
A.将10gNaCl固体与100g水混合溶解
B.向50g溶质的质量分数为20%的NaCl溶液中加入50g水
9.下表是不同温度下KNO3的溶解度表。
温度(℃)
溶解度(g/100g水)
(1)称取30gKNO3固体时,在加一定量的KNO3固体后,发现托盘天平指针偏右,接下来的操作是___________________,直到天平平衡。
(2)20℃时,将30gKNO3固体加入到盛有100g水的烧杯中,所得溶液是否饱和?
______________。
(3)要使20℃的KNO3不饱和溶液变成饱和溶液,可采用____________________的方法。
(写出一种即可)
工业上常用红锌矿(主要含ZnO)和18%~25%的稀硫酸为原料制取硫酸锌。
(1)硫酸锌中硫元素和氧元素的质量比是________。
(2)100g溶质质量分数为98%的浓硫酸配制成溶质质量分数为20%的稀硫酸,需要水的质量是________g。
参考答案
课前预热
考点1 1.氧气 氢气 1∶2 8∶1 2.氢元素 氧元素
考点2 1.没有 100℃ 0℃ 2.
(1)2H2O
2H2↑+O2↑
(2)CO2+H2O===H2CO3,SO3+H2O===H2SO4 (3)CaO+H2O===Ca(OH)2,Na2O+H2O===2NaOH
【考点真题】1.B 2.B
考点3 溶质 溶剂
考点4 溶剂 汽油、酒精
考点5 均一 混合
【考点真题】3.C 4.
(1)溶剂
(2)烧杯底部观察不到食盐固体颗粒
考点6 1.不能继续溶解 饱和溶液 不饱和溶液
考点7 ②温度 ③压强
考点8 100g 饱和 溶解度
【考点真题】5.D 6.A
考点9 1.溶液
考点11 2.计算、称量、溶解
【考点真题】7.C 8.
(1)<
(2)1.2 21.4%
考点13 过滤法
【考点真题】9.A
课堂突破
例1 B 例2 B 例3 A 例4 C 例5 D 例6
(1)1.22
(2)不变 (3)设敞口放置48小时的稀盐酸溶质质量分数为x,
NaOH+HCl===NaCl+H2O
4036.5
5.5克×
8% 5克×
x
40∶36.5=5.5克×
8%∶5克×
x,
解得:
x=8.03%>7.3%(其他解法也可)
故放置48小时的稀盐酸溶质质量分数变大。
解释:
蒸发的水和挥发的HCl的质量比大于927∶73(或蒸发的水占水总质量的百分比大于挥发的HCl占HCl总质量的百分比)。
【变式拓展】
1.A 2.D 3.
(1)20.9
(2)20% (3)方法一:
设要加入硝酸钾的质量为x。
100克×
10%+x=(100克+x)×
25% x=20克
答:
可向烧杯中加入20克硝酸钾。
方法二:
设蒸发水的质量为y。
10%=(100克-y)×
25% y=60克
可蒸发60克水。
校内作业
1.D 2.C 3.B 4.B 5.C 6.A
7.
(1)易 增大
(2)C、D A (3)50
8.
(1)量筒
(2)溶质 (3)B
9.
(1)继续加入KNO3固体
(2)不饱和 (3)降低温度(或蒸发水或加KNO3固体)
10.
(1)1∶2
(2)390