中考化学专题复习练习 溶解度曲线专题练习卷Word文档格式.docx
《中考化学专题复习练习 溶解度曲线专题练习卷Word文档格式.docx》由会员分享,可在线阅读,更多相关《中考化学专题复习练习 溶解度曲线专题练习卷Word文档格式.docx(25页珍藏版)》请在冰豆网上搜索。
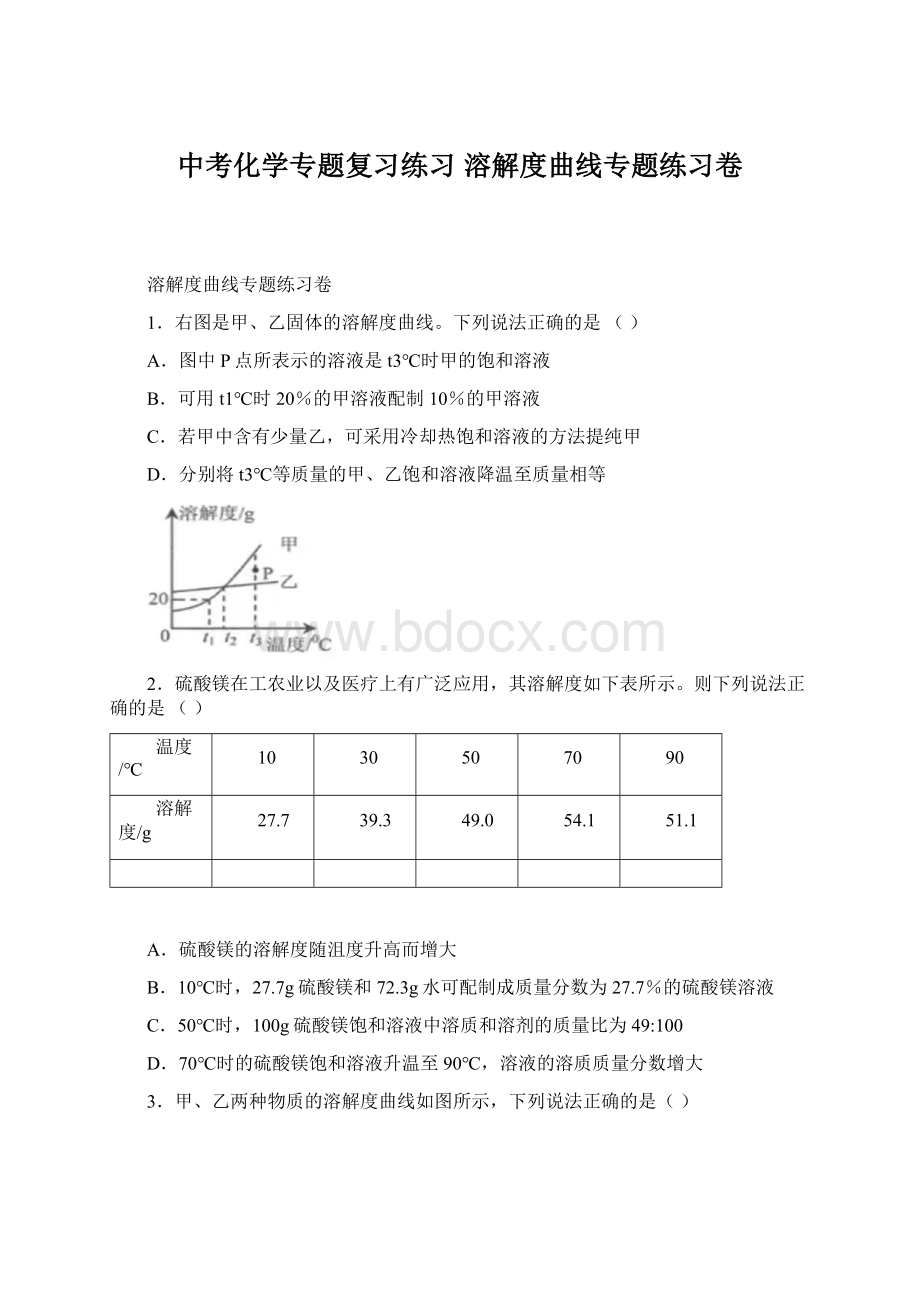
B.10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液
C.50℃时,100g硫酸镁饱和溶液中溶质和溶剂的质量比为49:
100
D.70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大
3.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是()
A.将甲、乙的饱和溶液从t2℃分别降温到t1℃,
析出晶体的质量甲一定大于乙
B.t1℃时甲、乙的饱和溶液中溶质质量分数相等
C.t2℃时将40g甲溶于100g水中,形成饱和溶液
D.将M点的甲溶液变成饱和溶液常采取的方法是__________________________。
4.t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氣化钾的溶解度曲线如图2所示。
A.烧杯①的溶液一定是不饱和溶液
B.烧杯①的溶液是硝酸钾溶液
C.烧杯②的溶液升温到t2℃时,烧杯底部还有部分物质不溶解
D.若烧杯①和烧杯②的溶液都升温到t2℃时,溶质的质量分数相等
5、NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。
20
40
60
溶解度
S/g
NH4Cl
33.3
37.2
41.4
45.8
50.4
60.2
Na2SO4
9.6
20.2
40.8
48.4
47.5
47.0
A.甲为NH4Cl
B.t2℃应介于30℃~50℃
C.甲、乙饱和溶液从t3降温到t2,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1升温到t3,为使其溶液恰好饱和,加入的甲、乙固体质量相等
6.MgSO4和Na2CO3的溶解度表及溶解度曲线如下.下列说法正确的是( )
温度/℃
20
30
40
50
60
70
80
溶解度S/g
MgSO4
25.1
28.2
30.8
32.9
34.3
35.0
34.9
Na2CO3
21.5
39.7
49.0
48.5
46.0
45.2
43.9
A.甲为Na2CO3
B.乙的饱和溶液从t1升温到t4,溶质质量分数增大
C.等质量甲、乙饱和溶液从t3降温到t1,析出晶体的质量(不带结晶水):
乙>甲
D.b、c点乙的饱和溶液溶质质量分数相等,且大于a点甲的饱和溶液溶质质量分数
7.如图所示为X、Y、Z三种固体物质(不含结晶水)的溶解度曲线,请回答下列问题:
(1)X中含有少量Y,应采用的方法提纯X。
(2)t2℃时,三种物质的溶解度的大小关系是。
(3)t3℃时,溶质质量分数为25%的X溶液降温到t1℃,所得溶液中溶质质量分数是。
(4)t3℃时,等质量X、Y、Z的饱和溶液分别降温到t1℃,溶液质量没有变化的是。
8、图表法是一种常用的数据处理方法。
结合所给图表回答下列问题:
(氢氧化钠、碳酸钠分别在水、酒精中的溶解度如下表所示)
氢氧化钠
碳酸钠
20℃
40℃
水
109g
129g
21.8g
49g
酒精
17.3g
40g
不溶
(1)上述图像表示________(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
(2)20℃时,氢氧化钠的溶解度_______(填“大于”或“小于”)碳酸钠。
(3)40℃时,若将50gNaOH分别投入到100g水和100g酒精中,能形成饱和溶液的是_______,再将CO2通入所得NaOH的酒精溶液中,观察到的现象为_______。
9.根据右图溶解度曲线判断下列问题,若错误请改正.
A.t2温度时abc三物质的溶解度大小关系是:
a>
b>
c
B.t1温度时a和c两物质的溶解度相等
C.t1温度时a和c两物质的溶液溶质质量分数相等
D.t1温度时,a、b饱和溶液中含有相同质量的溶质
E当温度大于t2温度,a溶液一定比b溶液浓
F.b中含有少量a时,用溶解、蒸发浓缩、降温结晶的方法除去b中的a
G.将t2温度时abc三物质的的饱和溶液降温到t1温度时三物质的溶质质量分数大小关系是:
a=c
H.将t2温度时a、b饱和溶液恒温蒸发等质量的水,析出晶体的质量a>
b
I.将t2温度时a、b两物质的的饱和溶液降温到t1温度时,析出晶体的质量大小关系是a>
J.将t2温度时将120克a物质放入200克水中得到溶液质量320克,溶质质量分数约33.3%
K将t1温度时abc三物质的的饱和溶液升温到t2温度时溶质质量分数a>
2020年中考化学模拟试卷
一、选择题
1.右表是元素周期表的一部分,下列判断正确的是()
6C
碳
12.01
甲
乙
丙
14Si
硅
28.09
丁
A.施用含甲元素的化肥可防植株倒伏
B.铁丝能在乙的单质中剧烈燃烧,火星四射,生成红棕色固体
C.丙合金具有较强的抗腐蚀性能,但其硬度较小
D.丁燃烧后的产物可用NaOH溶液吸收
2.对下列各组物质鉴别方案的描述,正确的是
A.NaOH、CuSO4、NaCl三种固体,只用水不能将其鉴别出来
B.N2、CO2、O2三种气体,只用燃着的木条就能将其鉴别出来
C.棉纤维、羊毛纤维、涤纶三种纤维,通过灼烧闻气味的方法不能将其鉴别出来
D.MgCl2、NaOH、Fe2(SO4)3三种溶液,不加其他试剂就能将其鉴别出来
3.有一种有机物(C15H26O),因分子形似“阿波罗”号飞船,被称为“阿波罗烷”。
下列说法正确的是
A.该物质属于有机高分子化合物
B.该物质中氢元素质量分数最大
C.该物质由15个碳原子、26个氢原子和1个氧原子构成
D.该物质中碳元素、氢元素和氧元素的质量比为90:
13:
8
4.锂矿是重要的国家战略资源,有着21世纪改变世界格局的“白色石油”和“绿色能源金属”之称。
如图是锂原子结构示意图和锂元素在元素周期表中的相关信息。
下列说法正确的是()
A.锂元素属于非金属元素
B.锂原子在化学反应中易失电子
C.锂原子的相对原子质量是6.941g
D.锂原子核内有3个中子
5.逻辑推理是一种重要的化学思维方法,下列推理合理的是()。
A.铁在潮湿空气中易缓慢氧化生成Fe2O3,则铁丝在氧气中燃烧也生成Fe2O3
B.NaOH溶液能使无色酚酞试液变红,则Cu(OH)2也能使无色酚酞试液变红
C.一氧化碳和氢气都能夺取氧化铁中的氧元素,所以它们都具有还原性
D.根据电解水的实验现象,可推知水是由氢气和氧气组成的
6.含碳元素物质之间发生转化:
C→CO2→CO→CO2→CaCO3其中不包括的化学反应类型有()
A.氧化反应B.化合反应C.置换反应D.复分解反应
7.下列有关实验操作的叙述正确的是
①用广泛pH试纸测定某溶液的pH值为5.6
②用10mL量筒量取8.8mL水
③蒸发结束用玻璃棒将食盐转移到指定容器中
④稀释浓硫酸时将水沿着烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌
A.①②③B.②③④C.①④D.②③
8.下列两种物质的溶液混合后、能发生反应、且溶液的总质量不会发生改变的是
A.氯化钠溶液和稀硫酸B.碳酸钠溶液和稀盐酸
C.氢氧化钠溶液和稀盐酸D.碳酸钠溶液和氯化钙溶液
9.下列关于碳和碳的化合物说法,错误的是
A.张校的墨宝在办公室摆放数年不褪色,是由于碳常温下化学性质不活泼
B.一个C60分子是由60个碳原子构成的,形似足球
C.一氧化碳和二氧化碳都属于非金属氧化物,所以都能与氢氧化钠溶液反应
D.人们把石墨放在高温、高压和有催化剂的反应釜中制得人造金刚石,虽然它们都是只由碳原子构成的物质,但这个变化属于化学变化
10.下列实验操作正确的是()
A.
滴加液体B.
验满二氧化碳
C.
稀释浓硫酸D.
给液体加热
11.“雾霾”中的“霾”是指烟、尘等小颗粒悬浮而形成的浑浊现象。
下列物质在空气中充分燃烧,能生成类似于“霾”的物质的是
A.CB.SC.PD.H2
12.下图是硫元素在元素周期表的信息及原子结构示意图。
下列说法错误的是()
A.n等于6B.S属于非金属元素
C.S的相对原子质量是32.06D.S在反应中易失去两个电子
13.将两种金属有X和Y分别放入硫酸铜溶液中,X表面无现象,Y的表面有红色固体析出,则三种金属活动性由强到弱的顺序是()
A.Y、Cu、XB.X、Y、CuC.X、Cu、YD.Y、X、Cu
14.将大蒜切成片,放置于空气中15分钟后会产生大蒜素(C6H10S2O),是抗癌之王。
大蒜本身不含大蒜素,只有在空气中氧化后才能获得大蒜素。
A.大蒜素中C、H元素的质量比为
B.大蒜素的相对分子质量为162
C.大蒜素中含有2个硫原子D.大蒜素属于氧化物
15.甲、乙两种固体物质溶解度曲线如右图所示,下列说法错误的是
A.15℃时,甲的溶解度小于乙的溶解度
B.40℃时,等质量的甲、乙饱和溶液中,溶剂质量:
甲<乙
C.将40℃时150g甲的饱和溶液降温到20℃,溶质质量分数为23.1%
D.20℃时,甲、乙溶液的溶质质量分数相同
二、填空题
16.早在诗经时代,艾草已经是很重要的民生植物,艾草有浓烈芳香的气味,我国民间有端午节挂艾草辟邪的习俗,艾草含有丰富的黄酮素(化学式为:
C15H10O2),有很高的药用价值,可以抗菌、平喘、止血等,艾草可作“艾叶茶”、“艾叶汤”、“艾叶粥”等食谱,以增强人体对疾病的抵抗能力.
请回答:
(1)黄酮素属于_____(填“混合物”“有机物”之一)
(2)黄酮素碳、氢元素的质量比是_____(填最简整数比)
(3)11.1g黄酮素中含氢元素质量是_____g
(4)黄酮素的功效是多方面的,它是一种很强的抗氧化剂,可有效清除体内的氧自由基,这种抗氧化作用可以阻止细胞的退化、衰老,也可阻止癌症的发生.对于黄酮素和艾草,下列相关说法中正确的是_____(填序号)
①黄酮素是碳、氢、氧原子构成②黄酮素有很高的利用价值③艾草浓烈芳香的气味,可用来驱蚊,说明分子不断运动.
17.根据表中信息,填写化学符号或符号意义:
化学符号
2O2
(2)___
(3)____
符号的意义
(1)___
水银
SO3中S的化合价为+6价
18.溶液与人们的生产、生活密切相关。
(1)将少量下列物质分