广东高中化学专题十四化学与技术选考讲义Word文档格式.docx
《广东高中化学专题十四化学与技术选考讲义Word文档格式.docx》由会员分享,可在线阅读,更多相关《广东高中化学专题十四化学与技术选考讲义Word文档格式.docx(19页珍藏版)》请在冰豆网上搜索。
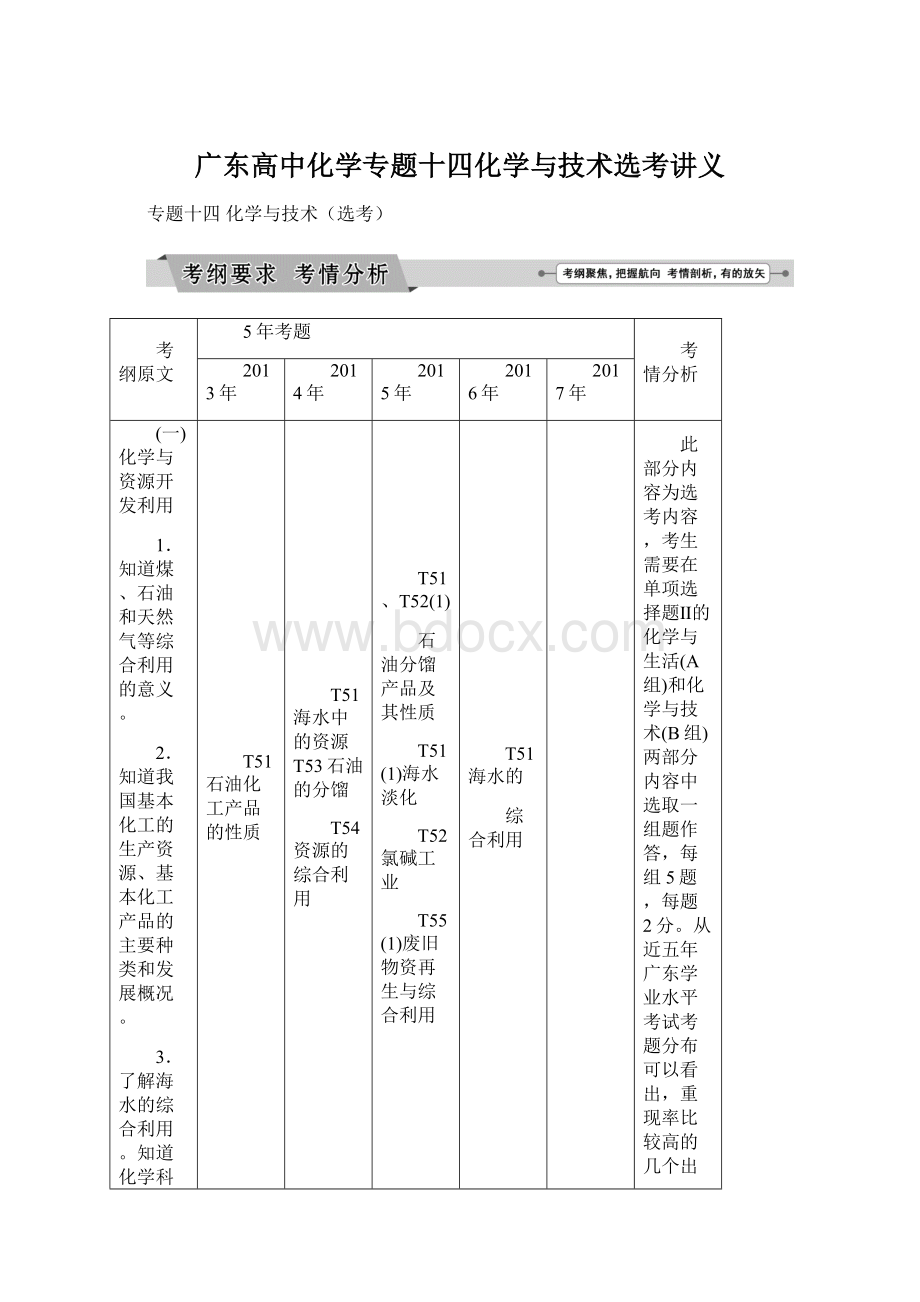
T51海水的
综合利用
此部分内容为选考内容,考生需要在单项选择题Ⅱ的化学与生活(A组)和化学与技术(B组)两部分内容中选取一组题作答,每组5题,每题2分。
从近五年广东学业水平考试考题分布可以看出,重现率比较高的几个出题热点有:
煤和石油化工涉及到的变化、污水处理方法、农药化肥的使用及对环境的影响等。
(二)化学与材料的制造、应用
1.了解社会发展和科技进步对材料的要求。
知道化学对材料科学发展的促进作用。
2.了解金属材料、无机非金属材料、高分子合成材料、复合材料和其他新材料的特点。
3.了解用化学方法进行金属材料表面处理的原理。
4.知道我国现代材料研究和材料工业的发展情况。
知道新材料的发展方向。
T53工业制玻璃
T55复合材料的性质
T55材料的性质
T53常见材料的主要成分
T52铝土矿处理的综合考查
T54缩合聚合反应的概念
T55复合材料的概念
(三)化学与工农业生产
1.了解化学在水处理中的应用。
2.了解合成氨的主要原理、原料、重要设备、流程和意义,认识催化剂的研制对促进化学工业发展的重大意义。
3.了解精细化工产品的生产特点、精细化工在社会发展中的作用。
4.了解化学肥料、农药等在农业生产中的作用。
T52侯氏制碱法
T54污水处理
T55农药、化肥的使用
T52化肥的分类
T53污水处理
T54农药、化肥的使用
T54
(1)工业合成氨
T52废水治理
T54氮肥的综合考查
T55侯氏制碱法
T51制备硫酸的综合考查
T53废水处理
注:
(1)表示1月学业水平考题。
考点1 化学与资源开发利用
1.(2016·
广东学业水平测试T51)海水蕴藏着丰富的资源。
下列有关海水综合利用的说法中,不正确的是( )
A.从海水中可提取食盐B.海水蒸馏可得淡水
C.直接电解海水可得镁D.从海水中可提取溴
2.(2015·
广东学业水平测试T51)下列石油的分馏产品中,沸点最低的是( )
A.汽油B.煤油
C.柴油D.石油气
3.(2015·
广东1月学业水平测试T52)下列物质不能通过石油分馏得到的是( )
A.汽油B.柴油
C.煤油D.水煤气
4.(2014·
广东学业水平测试T51)海洋中蕴藏着巨大的化学资源。
下列有关海水综合利用的说法正确的是( )
A.蒸发海水可以生产单质碘
B.蒸馏海水可以得到淡水
C.电解海水可以得到单质镁
D.电解海水可以制得金属钠
5.(2013·
广东学业水平测试T51)石油被誉为“工业的血液”,其分馏产品中沸点最高的是( )
A.汽油B.重油
1.煤、石油和天然气的综合利用
(1)煤的综合利用
主要是通过煤的干馏、煤的液化和气化,获得洁净的燃料和多种化工原料(如水煤气)。
从煤干馏得到的煤焦油中可获得苯等有机化工原料。
(2)石油的综合利用
石油的综合利用主要是通过石油的分馏获得汽油、煤油、柴油等轻质油,通过石油的催化裂化和裂解获得乙烯、丙烯等重要化工原料。
(3)天然气的综合利用
天然气既是一种清洁的化石燃料,也是合成氨和生产甲醇的重要化工原料。
天然气化工以含一个碳原子的甲烷为原料,通过化学变化形成含两个或多个碳原子的其他有机化合物。
2.海水的综合利用
(1)海水中盐的开发和利用
①海水制盐
由海水制盐的方法仍以蒸发法为主,它的原理很简单,即在太阳照射后,海水受热使水分蒸发,当各种盐分别达到其饱和浓度时,依次以固态形式析出。
②食盐资源的利用
氯碱工业就是通过电解饱和食盐水的方法得到NaOH、Cl2、H2,反应的化学方程式为2NaCl+2H2O2NaOH+H2↑+Cl2↑。
(2)海水提溴
从海水中提取的溴约占世界溴产量的1/3。
常用的一种海水提溴技术叫作吹出法,即用氯气氧化海水中的Br-,使其变成Br2,然后用空气或水蒸气吹出。
(3)海水提镁
海水中镁的总储量约为2.1×
1015t,目前世界生产的镁60%来自海水。
[温馨提示]
(1)煤和石油的加工方法中,只有石油的分馏是物理变化,其他都是化学变化。
(2)煤的气化主要是指高温下煤和水蒸气反应生成水煤气(CO和H2),是化学变化;
煤的液化是指将煤加工成液态燃料,也是化学变化。
海水中含有氯化镁,是镁的重要来源之一。
从海水中制取镁,可按如下步骤进行:
①把贝壳制成石灰乳 ②在引入的海水中加石灰乳,沉降、过滤、洗涤沉淀物 ③将沉淀物与盐酸反应,结晶、过滤、干燥产物 ④将得到的产物熔融后电解。
关于从海水中提取镁,下列有关说法不正确的是( )
A.此法的优点之一是原料来源丰富
B.进行①②③步骤的目的是从海水中提取氯化镁
C.第④步电解制镁是由于镁是很活泼的金属
D.以上制取镁的过程中涉及的反应有分解反应、化合反应和置换反应
[解析] 镁是活泼金属,用电解法制取,整个流程并没有涉及置换反应。
[答案] D
考点2 化学与材料的制造、应用
1.(2017·
广东学业水平测试T54)缩合聚合是合成高分子材料的一种重要反应。
下列属于缩合聚合反应的是( )
A.乙烯生成聚乙烯
B.四氟乙烯生成聚四氟乙烯
C.乙烯和氯气生成二氯乙烷
D.对苯二甲酸和乙二醇生成聚酯和水
2.(2016·
广东学业水平测试T53)喀斯特地貌地区蕴藏了大量石灰石。
下列材料与石灰石主要成分相同的是( )
A.玻璃B.水泥
C.陶瓷D.大理石
广东学业水平测试T55)新型柴油发动机的受热面由耐高温且不易传热的材料制造。
这种材料最可能是( )
A.陶瓷B.不锈钢
C.纯铁D.铝合金
广东学业水平测试T55)航天飞船高速进入大气层后,温度会迅速升高,其表层的复合材料可保护飞船不受破坏。
这体现了该复合材料具有的特点是( )
A.耐酸性B.耐热性
C.耐腐蚀D.耐碱性
1.无机非金属材料(见专题十三考点4)
2.金属材料
(1)从铁矿石中获得金属
①铁的冶炼:
生铁的冶炼原理是在高温下用还原剂将铁从其氧化物中还原出来,工业上一般是以铁矿石、石灰石和空气等为原料在高炉中炼制生铁。
用CO还原赤铁矿的化学方程式为Fe2O3+3CO2Fe+3CO2。
②铝的冶炼:
电解制铝的化学方程式为
2Al2O34Al+3O2↑。
(2)金属的腐蚀和防护(见专题十三考点4)
3.高分子材料
(1)加聚反应
①加聚反应的概念
由不饱和的单体加成聚合成高分子化合物的反应为加聚反应。
反应通过单体的自聚或共聚完成。
②加聚反应的特点
高分子链节与单体的化学组成相同,生成物只有高分子,一般形成线形结构。
(2)缩聚反应
指单体之间的相互作用生成高分子,同时还生成小分子(如水、氨、卤化氢等)的聚合反应,是缩合聚合反应的简称。
[温馨提示]
(1)铝制品的利用比铁制品晚是因为铝比铁活泼,更难冶炼。
(2)乙烯中含有碳碳双键,但加聚生成的聚乙烯中没有碳碳双键。
在航天飞机返回地球大气层时,为防止其与空气剧烈摩擦而被烧毁,需在航天飞机外表面安装保护层。
该保护层的材料可能为( )
A.铝合金B.合金钢
C.塑料D.新型陶瓷
[解析] 新型陶瓷具有抗高温的性能。
下列对制取水泥和玻璃的共同特点的叙述中错误的是( )
A.生产所用设备相同
B.反应都在高温的条件下进行
C.原料中均有石灰石
D.都发生复杂的物理、化学变化
[解析] 水泥和玻璃是传统的硅酸盐产品,因硅酸盐产品的熔点较高,故反应都是在高温条件下进行的,制取过程中都发生复杂的物理、化学变化且反应过程中都用到了石灰石为原料。
生产水泥的主要设备是水泥回转窑,制玻璃主要设备是玻璃熔炉。
[答案] A
考点3 化学与工农业生产
广东学业水平测试T53)保护水资源刻不容缓。
下列属于物理方法处理废水的是( )
A.用生石灰处理酸性废水
B.用沉淀剂处理含重金属离子废水
C.用稀盐酸处理碱性废水
D.用沉降法处理废水中的固体颗粒
广东学业水平测试T55)侯氏制碱法是将CO2通入含NH3的饱和NaCl溶液中,结晶,析出NaHCO3,过滤,将NaHCO3加热分解制得Na2CO3。
母液加入NaCl,通入NH3,降温,结晶析出NH4Cl,使母液又成为含NH3的饱和NaCl溶液。
下列说法错误的是( )
A.侯氏制碱法的主要原料是NaCl、CO2和NH3
B.Na2CO3的热稳定性低于NaHCO3
C.该方法的副产物是NH4Cl
D.母液可循环利用
3.(2016·
广东学业水平测试T52)生石灰常用于治理酸性废水,下列说法合理的是( )
A.生石灰主要成分是碱性化合物
B.该过程只发生了物理变化
C.生石灰主要成分是酸性化合物
D.该过程同时实现了水软化
4.(2015·
广东学业水平测试T54)下列关于农药和肥料的说法正确的是( )
A.氮肥只能通过人工合成而得到
B.含磷化合物都可以作为磷肥直接使用
C.草木灰含有K2CO3,可作为钾肥使用
D.农药都对人体无害,可以大量使用农药
5.(2014·
广东学业水平测试T52)化肥的合理利用显示了化学在促进农业现代化进程中的重要作用。
下列化肥既属于氮肥又属于钾肥的是( )
A.草木灰B.尿素
C.硝酸钾D.氨水
1.水的净化和处理
(1)净化原理
①混凝剂一般用铝盐或铁盐,如明矾等。
其净化原理是铝离子在水中生成胶状沉淀Al(OH)3,Al(OH)3具有强吸附性,能吸附悬浮的物质。
②消毒剂有氯气、漂白精、臭氧和二氧化氯等。
③活性炭表面积大,吸附能力强,可以除去水中的异味。
(2)硬水和软水
①概念:
硬水是含较多钙、镁离子的水;
软水是不含或少含钙、镁离子的水。
②硬水的软化方法有加热法、药剂法和离子交换法等。
(3)水污染处理的方法(见专题十三考点5)
2.化工生产
(1)氨的工业合成
原理:
N2+3H22NH3
工业上,采用铁为主的催化剂,在400~500℃和10~30MPa的条件下合成氨。
(2)氨氧化法制硝酸
4NH3+5O24NO+6H2O(常用铂作催化剂),2NO+O2===2NO2,3NO2+H2O===2HNO3+NO。
尾气净化:
用Na2CO3溶液吸收氮的氧化物得到亚硝酸钠和硝酸钠。
(3)接触法制硫酸
原料:
主要用硫铁矿、硫黄、有色金属冶炼烟气、石膏。
以硫铁矿为原料生产硫酸经过三个阶段:
4FeS2+11O22Fe2O3+8SO2;
2SO2+O22SO3;
SO3+H2O===H2SO4。
(4)纯碱工业(以联合制碱法为例)
氨气、二氧化碳和食盐。
反应原理:
NH3+CO2+H2O+NaCl===NH4Cl+NaHCO3↓。
3.农药和化肥
(1)化肥为农作物补充必要的营养元素
①农业生产中,大量使用的化肥主要有氮肥、磷肥、钾肥。
②常用的钾肥主要有氯化钾、硫酸钾、硝酸