实验报告及评价表参考模板Word格式文档下载.docx
《实验报告及评价表参考模板Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《实验报告及评价表参考模板Word格式文档下载.docx(11页珍藏版)》请在冰豆网上搜索。
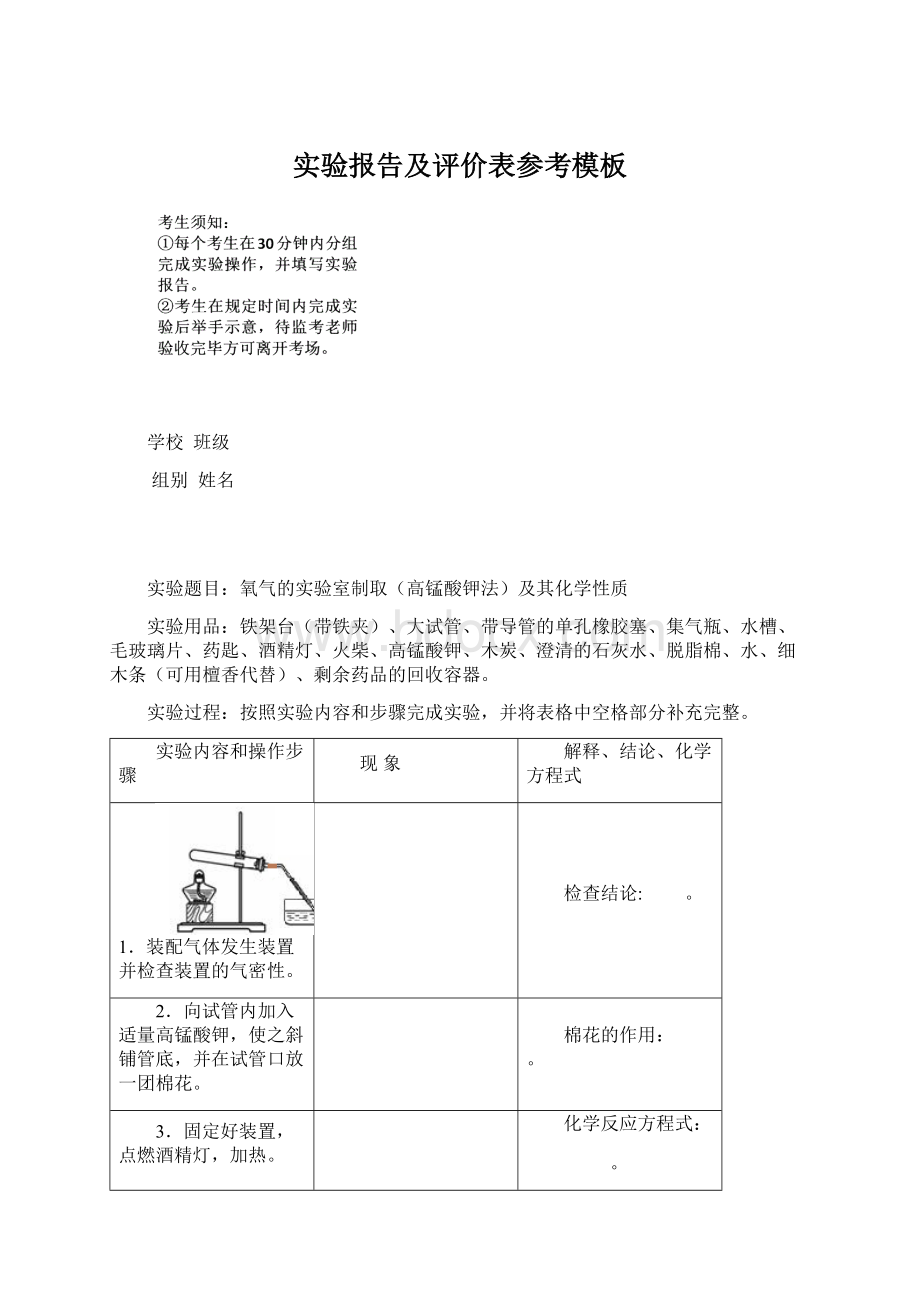
棉花的作用:
3.固定好装置,点燃酒精灯,加热。
化学反应方程式:
。
4.用排水集气法收集2集气瓶氧气。
气体呈色。
收集氧气能用排水集气法,是因为
。
5.检验收集的氧气。
6.木炭在氧气中燃烧。
将点燃的木炭移入盛满氧气的集气瓶中。
移出木炭后向集气瓶内加入澄清的石灰水。
木炭在空气中燃烧的现象
;
木炭在氧气中燃烧的现象
倒入石灰水后可看
到。
木炭燃烧的化学反应方程式:
。
7.终止实验。
8.问题研究
1)你认为用高锰酸钾制取氧气的实验操作步骤中应该注意哪些操作要点?
请分析原因。
2)为什么用带火星的木条,而不是燃着的木条检验是否有氧气生成?
3)比较木炭在空气中和在氧气中燃烧现象的不同,试分析产生不同现象的原因?
成绩评定
学校班级
组别姓名
燃烧的条件
酒精灯、蜡烛(两支大小相同)、玻璃棒、玻璃片、火柴、纸盒、小木条(直径与玻璃棒基本相同)、水、坩埚钳、剩余药品的回收容器。
实验内容和操作步骤
研究的变量
现象
解释、结论、化学方程式
1.将两支大小相同的蜡烛固定在玻璃片上,分别点燃,待燃烧片刻后,将一支蜡烛用小烧杯倒扣起来,观察。
实验结论:
2.点燃酒精灯,将一支玻璃棒和一支小木条同时在酒精灯火焰上加热一段时间,观察。
3.将小纸盒中加入少量水,用坩埚钳夹取并在酒精灯火焰上加热一段时间,观察。
另取一个相同材质的纸盒,在酒精灯火焰上加热。
4.终止实验。
5.问题研究
1)可燃物燃烧的必要条件是什么?
2)实验探究的一般步骤是什么?
3)在本实验中为什么要控制变量?
以前的实验中,有哪些实验是控制变量的?
4)结合实验步骤3要研究的变量,利用所给实验用品,请你再设计一个实验,写出实验的步骤、现象和结论。
成绩评定
质量守恒定律
托盘天平、砝码、烧杯、镊子、CuSO4溶液、铁钉、砂纸、剩余药品的回收容器。
1.实验准备。
1)调试托盘天平。
2)用砂纸将铁钉打磨光亮。
3)向100ml烧杯中加入大约30ml的硫酸铜溶液。
打磨后的铁钉的颜色为。
硫酸铜溶液的颜色是。
用砂纸将铁钉打磨光亮的原因
是。
2.反应前称量。
将盛有硫酸铜溶液的烧杯和铁钉同时放在托盘天平上称量,记录所称量的质量m1。
m1=g
反应物为。
3.发生化学反应。
取下烧杯和铁钉,将铁钉浸到硫酸铜溶液中,观察。
铁钉的变化
溶液的变化
生成物为,
反应的化学反应方程式为
4.反应后称量。
待充分反应后,再将烧杯放到托盘天平上称量,记录所称得的质量m2
m2=g
m1和m2的关系是。
5.终止实验。
6.问题研究
1)以铁钉和硫酸铜溶液的反应为例试分析,反应前后称量体系的质量m1和m2分别都包含哪些物质的质量?
由以上数据的分析得到什么结论?
2)为什么参加化学反应的物质的质量总和与生成的物质的质量总和相等?
实验编号:
4
学校班级
考生须知:
①每个考生在30分钟内分组完成实验操作,并填写实验报告。
②考生在规定时间内完成实验后举手示意,待监考老师验收完毕方可离开考场。
组别姓名
二氧化碳的实验室制取及其性质
锥形瓶(或平底烧瓶)、试管、带导管的单孔塞、集气瓶、毛玻璃片、镊子、药匙、胶头滴管、试管夹、火柴、酒精灯、细木条、蒸馏水、大理石或石灰石、稀盐酸、紫色石蕊溶液、剩余药品的回收容器。
1.装配气体制备装置并检查发生装置的气密性。
2.向容器内加入适量石灰石,然后再向其中加入适量稀盐酸。
可看到
。
3.迅速按要求固定好装置。
4.用排空气集气法收集1瓶二氧化碳。
用向上排空气集气法收集,是因
为。
5.验满收集的二氧化碳。
这是利用了二氧化碳的
的性质
6.二氧化碳与水的反应。
①向两支试管中分别加入约2ml的蒸馏水,然后分别各滴入1-2滴紫色石蕊试剂,观察。
试管中液体的颜色为色
②将其中一支试管静置,向另一支试管中通入二氧化碳气体,观察,并与静置的试管进行对比。
通入二氧化碳气体的试管中液体的颜色为
色
该反应的化学方程式为:
③将上述通入二氧化碳的试管放在酒精灯火焰上加热,并与静置的试管中溶液的颜色进行对比。
加热后,试管中的液体为色。
1.检验二氧化碳与验满二氧化碳的操作有何区别?
2.若只有大理石和稀硫酸两种药品,能否制得一瓶二氧化碳气体?
5
配制室温下含有8g溶质的质量分数为16%的氯化钠溶液
氯化钠固体、蒸馏水、托盘天平、烧杯(100ml)、量筒(10ml、
100ml)、玻璃棒、药匙、空的细口试剂瓶、空白的标签、剩余药品的回收容器。
1.计算溶质和溶剂的质量(或体积)。
氯化钠的质量=g;
蒸馏水的质量=g;
蒸馏水的体积=mL(水的密度近似看做1g/cm3)。
2.分别称取溶质、量取溶剂。
1)用托盘天平称量所需氯化钠的质量,倒入烧杯中。
2)用量筒量取所需体积的蒸馏水,倒入盛有氯化钠的烧杯中。
氯化钠是色的固体物质。
选用的量筒为
ml的。
称量氯化钠固体时,应先将放在天平的盘上。
用量筒量取蒸馏水时,若采取了俯视读数的方法,将会使配制的溶液溶质质量分数。
(填“偏大”“偏小”“不变”)
3.搅拌溶解。
用玻璃棒搅拌烧杯里的混合物,直至氯化钠全部溶解。
若要使加入的氯化钠固体快速溶液可采取的操作是。
4.装瓶、贴标签。
把配制好的溶液装入试剂瓶,盖好瓶塞并贴上标签(注意标签的规范书写)。
为了保护试剂瓶上的标签,在倾倒溶液时应将标签,倾倒结束时要注意。
5.终止实验
1)若室温下氯化钠的溶解度为36g;
经过简单计算,判断室温条件下溶质的质量分数为16%的氯化钠溶液是属于饱和溶液还是不饱和溶液?
2)本次实验如果出现配制的溶液中溶质的质量分数小于16%,你认为可能是哪些实验操作导致的实验误差?
化学实验一:
氧气的制取及性质
学校组别
评价要点及具体要求
总分
得分
(1)认真核对实验药品及仪器
(2)正确装配氧气的发生装置。
顺序
3
位置
操作
(3)正确检查装置的气密性。
(4)装入固体药品。
(5)固定仪器。
(6)加热药品。
(7)排水法收集氧气方法正确
准备
收集
结束
(8)检验氧气。
(9)木炭燃烧实验
点燃
移入
倾倒
(10)实验结束。
剩余物
仪器清洗
桌面
(11)问题研究
10
(10)及时记录实验现象,正确填写实验报告。
20
教师(签名)
2013年月日
友情提示:
范文可能无法思考和涵盖全面,供参考!
最好找专业人士起草或审核后使用,感谢您的下载!