高中化学常见离子的检验和物质的鉴别Word文件下载.doc
《高中化学常见离子的检验和物质的鉴别Word文件下载.doc》由会员分享,可在线阅读,更多相关《高中化学常见离子的检验和物质的鉴别Word文件下载.doc(4页珍藏版)》请在冰豆网上搜索。
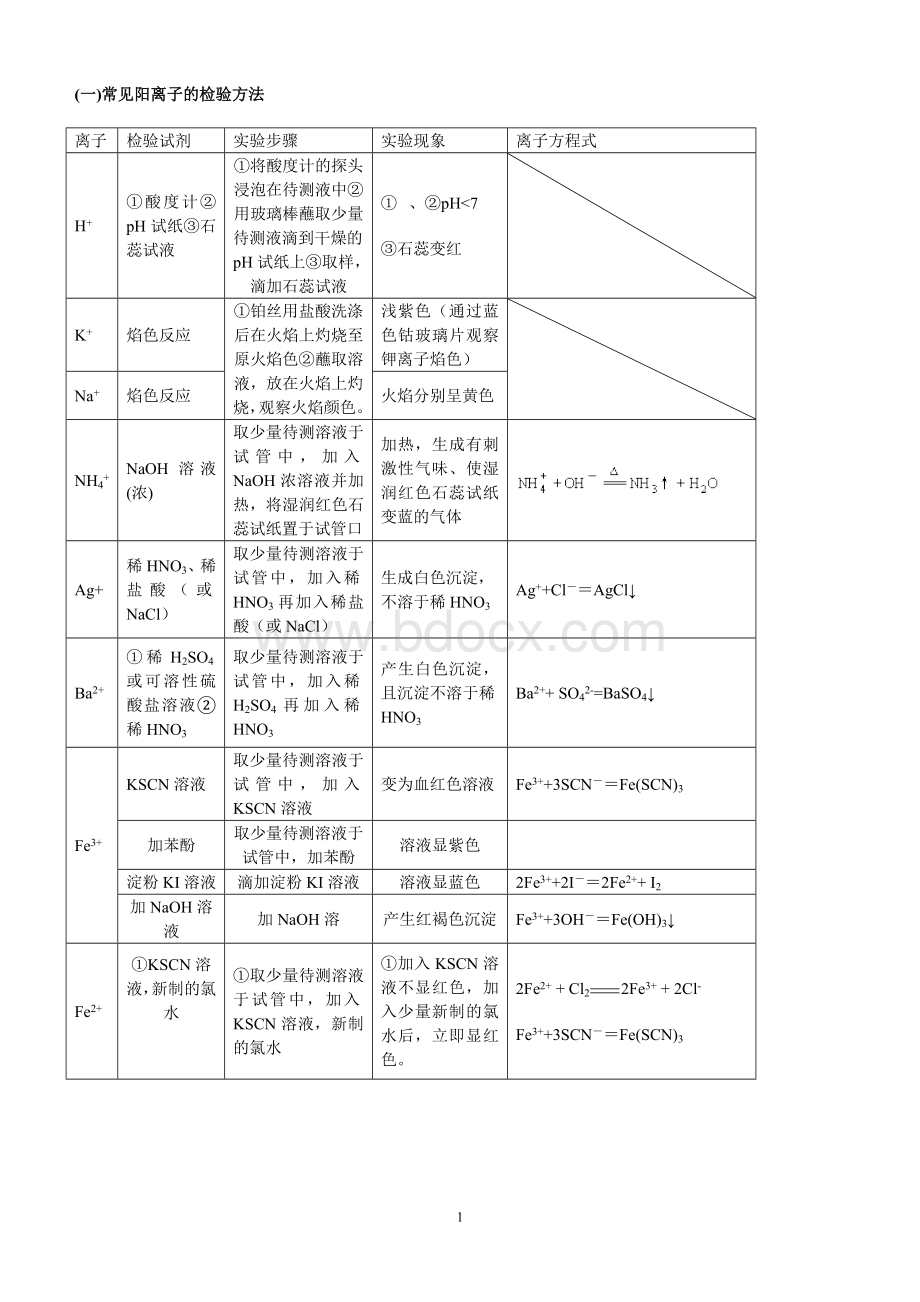
火焰分别呈黄色
NH4+
NaOH溶液(浓)
取少量待测溶液于试管中,加入NaOH浓溶液并加热,将湿润红色石蕊试纸置于试管口
加热,生成有刺激性气味、使湿润红色石蕊试纸变蓝的气体
Ag+
稀HNO3、稀盐酸(或NaCl)
取少量待测溶液于试管中,加入稀HNO3再加入稀盐酸(或NaCl)
生成白色沉淀,不溶于稀HNO3
Ag++Cl-=AgCl↓
Ba2+
①稀H2SO4或可溶性硫酸盐溶液②稀HNO3
取少量待测溶液于试管中,加入稀H2SO4再加入稀HNO3
产生白色沉淀,且沉淀不溶于稀HNO3
Ba2++SO42-=BaSO4↓
Fe3+
KSCN溶液
取少量待测溶液于试管中,加入KSCN溶液
变为血红色溶液
Fe3++3SCN-=Fe(SCN)3
加苯酚
取少量待测溶液于试管中,加苯酚
溶液显紫色
淀粉KI溶液
滴加淀粉KI溶液
溶液显蓝色
2Fe3++2I-=2Fe2++I2
加NaOH溶液
加NaOH溶
产生红褐色沉淀
Fe3++3OH-=Fe(OH)3↓
Fe2+
①KSCN溶液,新制的氯水
①取少量待测溶液于试管中,加入KSCN溶液,新制的氯水
①加入KSCN溶液不显红色,加入少量新制的氯水后,立即显红色。
2Fe2++Cl22Fe3++2Cl-
Fe3++3SCN-=Fe(SCN)3
②加NaOH溶液
②取少量待测溶液于试管中,加入NaOH溶液并露置在空气中
②开始时生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀。
Fe2++2OH—=Fe(OH)2↓
4Fe(OH)2十O2+2H2O=4Fe(OH)3
②加K3[Fe(CN)6]
取少量待测溶液于试管中,加入铁氰化钾
特征性蓝色沉淀
Al3+
NaOH溶液
取少量待测溶液于试管中,逐滴加入NaOH溶液至过量
加入适量NaOH溶液后生成白色沉淀,该沉淀溶于过量NaOH溶液中
Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-=AlO2-+2H2O
Cu2+
取少量待测溶液于试管中,加入NaOH溶液
加入适量NaOH溶液后生成蓝色沉淀
Cu++2OH-=Cu(OH)2↓
(二)常见阴离子的检验方法
OH-
①酸度计②pH试纸③酚酞或石蕊试液
③②pH>
③酚酞变红或石蕊变蓝
CO32-
①BaCl2溶液、稀盐酸
取少量待测溶液于试管中,加入BaCl2溶液再向沉淀中加入稀盐酸。
1.加入BaCl2溶液后生成白色沉淀,沉淀溶于稀盐酸,并放出无色无味气体
Ba2++CO32-=BaCO3↓
BaCO3+2H+=Ba2++CO2↑+H2O
②稀盐酸、Ca(OH)2溶液
取少量待测溶液于试管中,加入稀盐酸后放出的气体通入使澄清的Ca(OH)2溶液
2.加入稀盐酸后放出无色无味气体,通入澄清的Ca(OH)2溶液变浑浊
CO32-+2H+=H2O+CO2↑
Ca2++2OH-+CO2=CaCO3↓+H2O
SO42-
BaCl2溶液、稀硝酸或稀盐酸
生成不溶于稀硝酸或稀盐酸的白色沉淀
SO32-
①稀盐酸、品红溶液
取少量待测溶液于试管中,加入稀盐酸后放出的气体通入品红溶液
加入稀盐酸后放出的气体使品红溶液褪色
SO32-+2H+=H2O+SO2↑
②BaCl2溶液、稀盐酸
加入BaCl2溶液后生成白色沉淀,沉淀溶于稀盐酸,并放出刺激性气味的气体
Cl-
AgNO3溶液、稀硝酸或稀盐酸
取少量待测溶液于试管中,加入AgNO3溶液,再向沉淀中加入稀盐酸。
Br-
生成不溶于稀硝酸或稀盐酸的浅黄色沉淀
Ag++Br-=AgBr↓
I-
①AgNO3溶液、稀硝酸
①生成不溶于稀硝酸的黄色沉淀
Ag++I-=AgI↓
②新制氯水,淀粉溶液
取少量待测溶液于试管中,加入新制氯水,再加入淀粉溶液
②滴入新制Cl2,振荡后再滴入淀粉溶液,变蓝
2I-+Cl2=I2+2Cl-
I2遇淀粉变蓝
ClO-
HCl、淀粉-KI
取少量待测溶液于试管中,加入HCl溶液,然后加入淀粉-KI溶液
淀粉-KI溶液变蓝
HCl、石蕊
取少量待测溶液于试管中,加入HCl溶液,然后加入石蕊试液
石蕊先变红后褪色
注意:
1.若SO42-与Cl-同时检验,需注意检验顺序。
应先用Ba(NO3)2溶液将SO42-检出,并滤去BaSO4,然后再用AgNO3检验Cl-。
2.检验SO32-的试剂中,只能用盐酸,不能用稀硝酸。
因为稀硝酸能把SO32-氧化成SO42-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
4.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出
5.若CO32-和HCO3-同时检验,应先用足量的BaCl2溶液将CO32-检出,静置,取上层清夜用Ba(OH)2或Ca(OH)2检出HCO3-
(三).常见气体的检验
常见气体
检验方法
氢气
纯净的氢气在空气中燃烧呈淡蓝色火焰,混合空气点燃有爆鸣声,生成物只有水。
不是只有氢气才产生爆鸣声;
可点燃的气体不一定是氢气
氧气
可使带火星的木条复燃
氯气
黄绿色,能使湿润的碘化钾淀粉试纸变蓝(O3、NO2也能使湿润的碘化钾淀粉试纸变蓝)
氯化氢
无色有刺激性气味的气体。
在潮湿的空气中形成白雾,能使湿润的蓝色石蓝试纸变红;
用蘸有浓氨水的玻璃棒靠近时冒白烟;
将气体通入AgNO3溶液时有白色沉淀生成。
二氧化硫
能使品红溶液褪色,加热后又显红色。
能使酸性高锰酸钾溶液褪色。
硫化氢
无色有具鸡蛋气味的气体。
能使Pb(NO3)2或CuSO4溶液产生黑色沉淀,或使湿润的醋酸铅试纸变黑。
氨气
无色有刺激性气味,能使湿润的红色石蕊试纸变蓝,用蘸有浓盐酸的玻璃棒靠近时能生成白烟。
二氧化氮
红棕色气体,通入水中生成无色的溶液并产生无色气体,水溶液显酸性。
一氧化氮
无色气体,在空气中立即变成红棕色
二氧化碳
能使澄清石灰水变浑浊;
能使燃着的木条熄灭。
SO2气体也能使澄清的石灰水变混浊,N2等气体也能使燃着的木条熄灭。
一氧化碳
可燃烧,火焰呈淡蓝色,燃烧后只生成CO2;
能使灼热的CuO由黑色变成红色。
甲烷
无色气体,可燃,淡蓝色火焰,生成水和CO2;
不能使高锰酸钾溶液、溴水褪色。
乙烯
无色气体、可燃,燃烧时有明亮的火焰和黑烟,生成水和CO2。
能使高锰酸钾溶液、溴水褪色。
乙炔
无色无臭气体,可燃,燃烧时有明亮的火焰和浓烟,生成水和CO2,能使高锰酸钾溶液、溴水褪色。
(四).几种重要有机物的检验
(1)苯能与纯溴、铁屑反应,产生HBr白雾。
能与浓硫酸、浓硝酸的混合物反应,生成黄色的苦杏仁气味的油状(密度大于1)难溶于水的硝基苯。
(2)乙醇能够与灼热的螺旋状铜丝反应,使其表面上黑色CuO变为光亮的铜,并产生有刺激性气味的乙醛。
乙醇与乙酸、浓硫酸混合物加热反应,将生成的气体通入饱和Na2CO3溶液,有透明油状、水果香味的乙酸乙酯液体浮在水面上。
(3)苯酚能与浓溴水反应生成白色的三溴苯酚沉淀。
能与FeCl3溶液反应,生成紫色溶液。
(4)乙醛能发生银镜反应,或能与新制的蓝色Cu(OH)2加热反应,生成红色的Cu2O沉淀。
4