初中常见化学式及化学方程式 1Word格式文档下载.docx
《初中常见化学式及化学方程式 1Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《初中常见化学式及化学方程式 1Word格式文档下载.docx(10页珍藏版)》请在冰豆网上搜索。
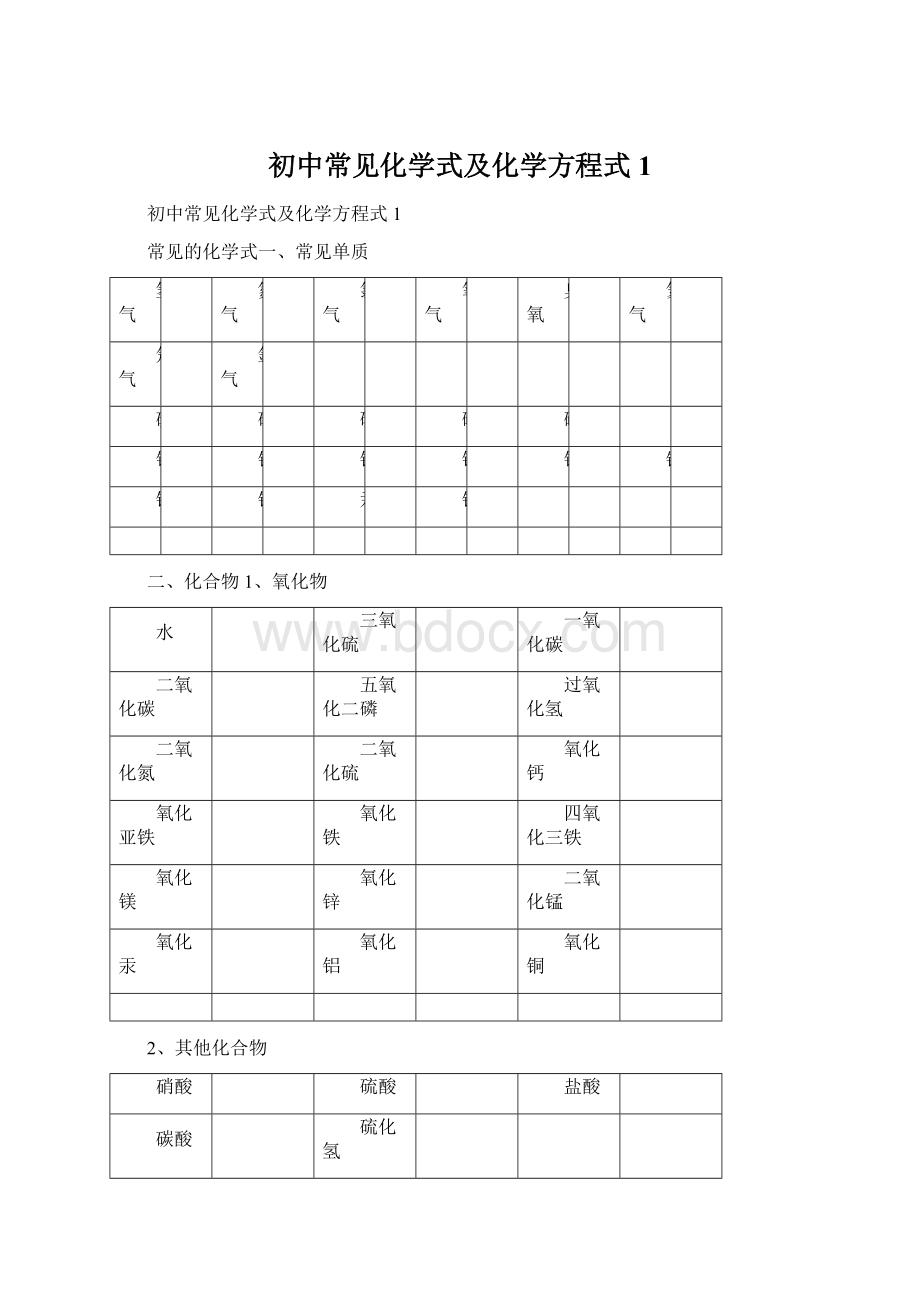
二氧化氮
二氧化硫
氧化钙
氧化亚铁
氧化铁
四氧化三铁
氧化镁
氧化锌
二氧化锰
氧化汞
氧化铝
氧化铜
2、其他化合物
硝酸
硫酸
盐酸
碳酸
硫化氢
氢氧化钠
氢氧化钾
氢氧化钙
氢氧化镁
氢氧化铝
氢氧化锌
氢氧化铁
氢氧化亚铁
氢氧化铜
氢氧化钡
氨水
氯化钠
氯化铜
氯化铝
氯化钾
氯化亚铁
氯化铁
氯化银
氯化钙
氯化镁
氯化钡
氯化锌
硫酸铜
高锰酸钾
锰酸钾
氯酸钾
碳酸钙
硝酸钾
硝酸钠
硝酸铁
硝酸亚铁
硝酸铝
碳酸钠
碳酸铵
碳酸氢钠
硫酸铁
硫酸亚铁
硝酸银
硝酸钡
硝酸铵
硫酸钡
3、常见有机化合物
甲烷
乙醇
葡萄糖
初中化学方程式全(已配平).
一、化合反应
1、镁在空气中燃烧:
2、铁在氧气中燃烧:
3、铝在空气中燃烧:
4、氢气在空气中燃烧:
5、红磷在空气中燃烧:
6、硫粉在空气中燃烧:
7、碳在氧气中充分燃烧:
8、碳在氧气中不充分燃烧
9、二氧化碳通过灼热碳层:
10、一氧化碳在氧气中燃烧:
11、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):
12.生石灰溶于水:
13、无水硫酸铜作干燥剂:
14、钠在氯气中燃烧:
12、二、分解反应
15、实验室用双氧水制氧气:
16、加热高锰酸钾:
17、水在直流电的作用下分解:
18、碳酸化学物理学报不稳定而分解:
19、高温煅烧石灰石(二氧化碳工业制法):
三、置换反应
20、铁和硫酸铜溶液反应:
21、锌和稀硫酸反应(实验室制氢气):
22、镁和稀盐酸反应:
23、氢气还原氧化铜:
24、木炭还原氧化铜:
25、甲烷在空气中燃烧:
26、水蒸气通过灼热碳层:
27、焦炭还原氧化铁:
其他
28、氢氧化钠溶液与硫酸铜溶液反应:
29、甲烷在空气中燃烧:
30、酒精在空气中燃烧:
31、一氧化碳还原氧化铜:
32、一氧化碳还原氧化铁:
33、二氧化碳通过澄清石灰水(检验二氧化碳):
34、氢氧化钠和二氧化碳反应(除去二氧化碳):
35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):
36、碳酸钠与浓盐酸反应(泡沫灭火器的原理):
一.物质与氧气的反应:
(1)单质与氧气的反应:
1.镁在空气中燃烧:
2.铁在氧气中燃烧:
3.铜在空气中受热:
4.铝在空气中燃烧:
5.氢气中空气中燃烧:
6.红磷在空气中燃烧:
7.硫粉在空气中燃烧:
8.碳在氧气中充分燃烧:
9.碳在氧气中不充分燃烧:
(2)化合物与氧气的反应:
10.一氧化碳在氧气中燃烧:
11.甲烷在空气中燃烧:
12.酒精在空气中燃烧:
二.几个分解反应:
13.水在直流电的作用下分新概念英语第一册解:
14.加热碱式碳酸铜:
15.加热氯酸钾(有少量的二氧化锰):
16.加热高锰酸钾:
17.碳酸不稳定而分解:
18.高温煅烧石灰石:
三.几个氧化还原反应:
19.氢气还原氧化铜:
20.木炭还原氧化铜:
2初三化学方程式大合集
21.焦炭还原氧化铁:
22.焦炭还原四氧化三铁:
23.一氧化碳还原氧化铜:
24.一氧化碳还原氧化铁:
25.一氧化碳还原四氧化三铁:
四.单质、氧化物、酸、碱、盐的相互关系
(1)金属单质+酸--------盐+氢气(置换反应)
26.锌和稀硫酸
27.铁和稀硫酸
28.镁和稀硫酸
29.铝和稀硫酸
30.锌和稀盐酸
31.铁和稀盐酸
32.镁和语文教案格式稀盐酸Mg
33.铝和稀盐酸
(2)金属单质+盐(溶液)-------另一种金属+另一种盐
34.铁和硫酸铜溶液反应:
35.锌和硫酸铜溶液反应:
36.铜和硝酸汞溶液反应:
(3)碱性氧化物+酸--------盐+水
37.氧化铁和稀盐酸反应:
38.氧化铁和稀硫酸反应:
39.氧化铜和稀盐酸反应:
40.氧化铜和稀硫酸反应:
41.氧化镁和稀硫酸反应:
42.氧化钙和稀盐酸反应:
(4)酸性氧化物+碱--------盐+水
43.苛性钠暴露在空气中变质:
44.苛性钠吸收二氧化硫气体:
45.苛性钠吸收三氧化硫气体:
46.消石灰放在空气中变质:
47.消石灰吸收二氧化硫:
(5)酸+碱--------盐+水
48.盐酸和烧碱起反应:
49.盐酸和氢氧化钾反应:
50.盐酸和氢氧化初中家长会课件铜反应:
51.盐酸和氢氧化钙反应:
52.盐酸和氢氧化铁反应:
53.氢氧化铝药物治疗胃酸过多:
54.硫酸和烧碱反应:
55.硫酸和氢氧化钾反应:
56.硫酸和氢氧化铜反应:
57.硫酸和氢氧化铁反应:
58.硝酸和烧碱反应:
(6)酸+盐--------另一种酸+另一种盐
59.大理石与稀盐酸反应:
60.碳酸钠与稀盐酸反应:
61.碳酸镁与稀盐酸反应:
62.盐酸和硝酸银溶液反应:
63.硫酸和碳酸钠反应:
64.硫酸和氯化钡溶液反应:
(7)碱+盐--------另一种碱+另一种盐
65.氢氧化钠与硫酸铜:
66.氢氧化钠与氯化铁:
67.氢氧化钠与氯化镁:
68.氢氧化钠与氯化铜:
69.氢氧化钙与碳酸钠:
(8)盐+盐-----两种新盐
70.氯化钠溶液新概念英语第二册和硝酸银溶液:
71.硫酸钠和氯化钡:
五.其它反应:
72.二氧化碳溶解于水:
73.生石灰溶于水:
74.氧化钠溶于水:
75.三氧化硫溶于水:
76.硫酸铜晶体受热分解:
77.无水硫酸铜作干燥剂:
化学方程式反应现象应用删后面的中文
2Mg+O2点燃或Δ2MgO
2Hg+O2点燃或Δ2HgO
2Cu+O2点燃或Δ2CuO
4Al+3O2点燃或Δ2Al2O3
3Fe+2O2点燃Fe3O4
C+O2点燃CO2
S+O2点燃SO2
2H2O2点燃2H2O
4P+5O2点燃2P2O5
CH4+2O2点燃2H2O+CO2
2C2H2+5O2点燃2H2O+4CO2
2KClO3MnO2、Δ2KCl+3O2↑
2KMnO4ΔK2MnO4MnO2+O2↑
2HgOΔ2Hg+O2↑
2H2O通电2H2↑+O2↑
Cu2(OH)2CO3Δ2CuO+H2O+CO2↑
NH4HCO3ΔNH3↑+H2O+CO2↑
Zn+H2SO4=ZnSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
Mg+H2SO4=MgSO4+H2↑
2Al+3H2SO4=Al2(SO4)3+3H2↑
Fe2O3+3H2Δ2Fe+3H2O
Fe3O4+4H2Δ3Fe+4H2O
WO3+3H2ΔW+3H2O
MoO3+3H2ΔMo+3H2O
2Na+Cl2Δ或点燃2NaCl
H2+Cl2点燃或光照2HCl
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
2C+O2点燃2CO
2CO+O2点燃2CO2
C+CuO高温2Cu+CO2↑
2Fe2O3+3C高温4Fe+3CO2↑
Fe3O4+2C高温3Fe+2CO2↑
C+CO2高温2CO
CO2+H2O=H2CO3
H2CO3ΔCO2↑+H2O
Ca(OH)2+CO2=CaCO3↓+H2O
CaCO3+H2O+CO2=Ca(HCO3)2
Ca(HCO3)2ΔCaCO3↓+H2O+CO2↑
2NaHCO3ΔNa2CO3+H2O+CO2↑
CaCO3高温CaO+CO2↑
CaCO3+2HCl=CaCl2+H2O+CO2↑
初中化学方程式汇总
一、氧气的性质:
(化合反应)
6.红磷在空气中燃烧(研究空气组成的实验):
(3)氧气的来源:
13.玻义耳研究空气的成分实验
14.加热高锰酸钾:
(实验室制氧气原理1)
15.过氧化氢在二氧化锰作催化剂条件下分解反应:
(实验室制氧气原理2)
二、自然界中的水:
16.水在直流电的作用下分解(研究水的组成实验):
17.生石灰溶于水英语六级作文:
18.二氧化碳可溶于水:
3、质量守恒定律:
19.镁在空气中燃烧:
20.铁和硫酸铜溶液反应:
21.氢气还原氧化铜:
22.镁还原氧化铜:
四、碳和碳的氧化物:
(1)碳的化学性质
23.碳在氧气中充分燃烧:
24.木炭还原氧化铜:
25.焦炭还原氧化铁:
(2)煤炉中发生的三个反应:
(几个化合反应)
26.煤炉的底层:
27.煤炉的中层:
28.煤炉的上部蓝色火焰的产生:
(3)二氧化碳的制法与性质:
29.大理石与稀盐酸反应(实验室制二氧化碳):
30.碳酸不稳定而分解:
31.二氧化碳可溶于水:
32.高温煅烧石灰石(工业制二氧化碳):
33.石灰水与中学历史教学园地二氧化碳反应(鉴别二氧化碳):
(4)一氧化碳的性质:
34.一氧化碳还原氧化铜:
35.一氧化碳的可燃性:
其它反应:
36.碳酸钠与稀盐酸反应(灭火器的原理):
五、燃料及其利用:
37.甲烷在空气中燃烧:
38.酒精在空气中燃烧:
39.氢气中空气中燃烧:
六、金属
(1)金属与氧气反应:
40.镁在空气中燃烧:
41.铁在氧气中燃烧:
42.铜在空气中受热:
43.铝在空气中形成氧化膜:
(2)金属单质酸--------盐氢气(置换反应)
44.锌和稀硫酸
45.铁和稀硫