元素周期律元素周期表 学生文档格式.docx
《元素周期律元素周期表 学生文档格式.docx》由会员分享,可在线阅读,更多相关《元素周期律元素周期表 学生文档格式.docx(19页珍藏版)》请在冰豆网上搜索。
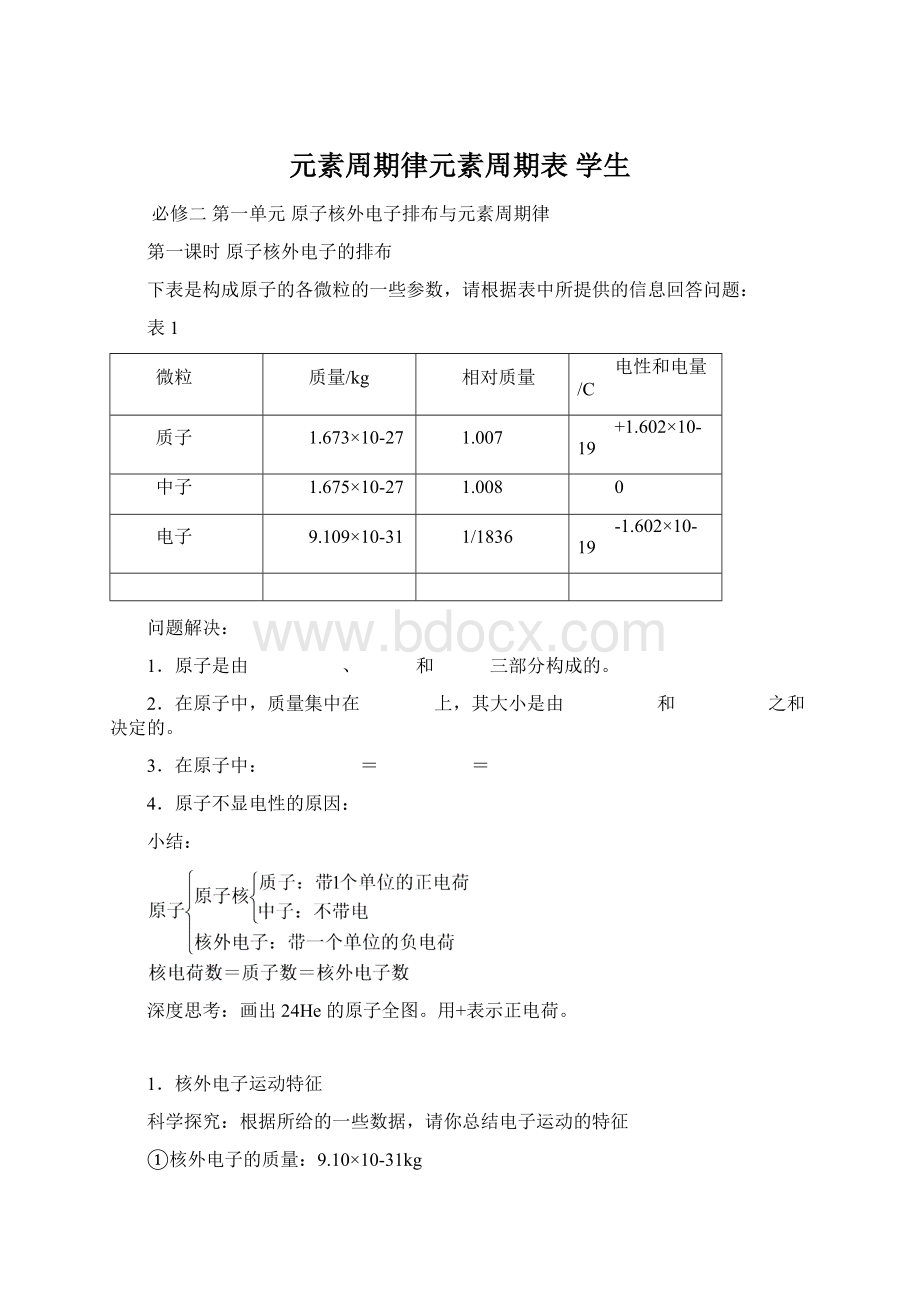
3.在原子中:
= =
4.原子不显电性的原因:
小结:
深度思考:
画出24He的原子全图。
用+表示正电荷。
1.核外电子运动特征
科学探究:
根据所给的一些数据,请你总结电子运动的特征
①核外电子的质量:
9.10×
10-31kg
②炮弹的速度2km/s,人造卫星7.8km/s,宇宙飞船11km/s;
氢核外电子2.2×
108m/s
③乒乓球半径:
4×
10-2m;
原子半径:
n×
10-10m
结论:
电子运动的特征是:
电子质量 ,运动速度 ,运动空间范围 。
核外电子的运动特点
(1)电子的质量很小,带负电荷。
(2)电子运动的空间范围小。
(3)电子做高速运动,接近光速。
一、核外电子的分层排布
含多个核外电子的原子中,电子运动的主要区域离核 ,在离核较近的区域运动的电子能量 ,在离核较远的区域运动的电子能量 ,即电子在原子核外是
排布的。
电子层序号
1
2
3
4
5
6
7
电子层符号
电子离核远近与能量大小
电子离核由 到 ,电子能量由 到 。
例题1:
同一个原子的下列电子层中,能量最低的是( )
A、K层 B、L层 C、M层 D、N层
二、核外电子排布的一般规律
1、能量最低原理:
电子在原子核外排布时,总是尽量先排在能量 的电子层里,即最先排布 层,当 层排满后,再排 层等;
2、原子核外各电子层最多能容纳的电子数为 (n表示电子层数);
3、最外电子层最多只能容纳 个电子(K层为最外层时最多只能容纳 个电子);
4、次外层(由外向里数第二层)电子数目不超过 个,倒数第三层电子数目不超过
个。
例题2:
依据核外电子排布的一般规律解释下列现象。
(1)Na的原子结构示意图为什么是 ,而不是 ,原因为
;
(2)Xe的原子结构示意图为 ,为什么不是 或
,原因分别为 和
。
三、核外电子排布的表示方法
核外电子排布通常用 表示,包括 结构示意图和 结构示意图。
例题3:
分别画出下列微粒的结构示意图。
Na+Mg2+Al3+NeF—O2—
四、元素性质与核外电子排布的关系
1、由于稀有气体元素的原子最外层电子数 ,所以稀有气体的性质比较稳定;
2、元素原子的最外层电子数≥4,易 电子,体现 性;
3、元素原子的最外层电子数<4,易 电子,体现 性。
例题4:
填写下列空白。
(1) ,质子数为 ,质量数为 ,中子数为 ,电子数为 ,核电荷数为 ;
(2) ,质子数为 ,质量数为 ,中子数为 ,电子数为 ,核电荷数为 ,X原子的最外层电子数为 ;
(3) n+,质子数为 ,质量数为 ,中子数为 ,电子数为 ,核电荷数为 ,X原子的最外层电子数为 。
〔巩固练习〕——(要求:
标出关键词,写出解题过程。
)
1、下列有关电子运动的说法中,错误的是 ( )
A、电子绕原子核不停地作高速运动
B、电子在原子核外是分层排布的
C、核外电子运动的区域被称为电子层
D、离核近的电子能量高,离核远的电子能量低
2、下列所画原子结构示意图正确的是 ( )
A、B、C、D、
3、某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该元素的核电荷数可能为( )
A、11B、15C、17D、10
4、人类探测月亮发现,在月球的土壤中含有较丰富的质量数为3的氦,它可以作为未来核聚变的重要原料之一。
氦的该种原子应表示为 ( )
5.和氖原子有相同的电子层的微粒是()
A.HeB.K+C.Cl-D.
6、从1~18号元素原子中选择合适的化学式填空
(1)最外层有1个电子的原子_________________
(2)最外层有2个电子的原子_________________
(3)最外层电子数等于次外层电子数的原子_________________
(4)最外层电子数是次外层电子数2倍的原子_________________
最外层电子数是次外层电子数3倍的原子_________________
最外层电子数是次外层电子数4倍的原子_________________
(5)电子层数与最外层电子数相等的原子_________________
(6)次外层电子数是最外层电子数2倍的原子_________________
(7)内层电子总数是最外层电子数2倍的原子_________________
7、画出下列各微粒的结构示意图
(1)与Ne原子电子层结构相同的-2价阴离子_______________
(2)最外层电子数为次外层电子数2倍的原子_______________
(3)L层电子数为K层、M层电子数之和的原子_______________
8、下列指定微粒的个数比等于2:
1的是()
A.H原子的中子数和质子数B.Ar原子中的质量数和中子数
C.Be2+离子中的电子数和质子数D.Mg2+离子中的中子数和电子数
9.今有A、B两种原子,已知A原子的核外电子总数是B原子核外电子总数的1/2倍,B原子的L层电子数为A原子L层电子数的2倍,A和B分别是()
A.硼和氦B.碳和镁C.氯和碳D.铍和氧
10.在第n电子层中,当它作为原子的最外电子层时,能容纳的最多电子数与n-1层相同,当它作为原子的次外层时。
其电子数比n+1层最多能多10个,则此电子层是()
A.K层B.L层C.M层D.N层
11.178O和168O原子核外电子数(判断前后两者的关系)()
A.大于B.小于C.等于D.不能肯定
第二课时元素周期律
这是门捷列夫手稿中的一个片断:
他把元素按照原子量由小到大的顺序排列起来:
H
Li
B
C
Be
N
O
F
Na
Mg
Al
Si
P
S
Cl
K
Ca
原子量
11
12
13.5
14
16
19
23
24
27
28
31
32
35.5
39
40
化合价
+1
+3
+4
+2
+5
-2
-1
+6
+7
思考下列问题:
①门捷列夫在“看”什么?
②他是如何“看”出Be的位置不正确的?
③如何“试”着矫正Be的位置?
④为什么门捷列夫依据原子量而不是化合价或者是物质的颜色等性质作为元素分类的依据呢?
1、写出1~18号元素的元素符号并画出相应的原子结构示意图。
元素符号
He
原子结构示意图
2、仔细观察上述元素原子结构示意图,填写下表。
原子序数
电子层数
最外层电子数
达到稳定结构时最外层电子数
1~2
3~10
11~18
随着核电荷数的递增,元素原子的核外电子排布呈现 变化。
除H、He外,最外层电子数重复出现从 → 递增的变化。
二、原子半径
原子半径的变化情况
3~9
11~17
随着核电荷数的递增,元素原子的半径呈现 变化。
在3~9号元素或11~17号元素随着核电荷数的递增,原子半径逐渐 。
原子或者离子半径比较的一般规律
例1:
下列元素中,原子半径最大的是()
A、锂 B、钠 C、氟 D、氯
三、元素的主要化合价
最高正价或最低负价的变化
最高或最低化合价与最外层电子数的关系
最高正价:
由 到
最低负价:
最高化合价=
最低化合价=
某一元素最高正价与最低负价的绝对值之和为 。
随着原子序数的递增,元素主要化合价呈现 变化。
例23、下列各组元素中,按原子序数逐渐增加,原子半径依次增大的是()
A、NaMgAlSiB、ClSPSiC、FClBrID、HFClNa
4444444444444444444:
M元素原子核外有两个电子层,L层有5个电子,该元素的最高正价为 ,其最高价氧化物对应的水化物为 ;
最低负价为 ,其氢化物的化学式为 。
例3:
某元素最高价氧化物对应水化物的化学式是H2XO4,其气态氢化物的化学式()
A、HX B、H2X C、XH3 D、XH4
4、元素的金属性与非金属性
1、元素的金属性强弱的判断依据:
2、元素的非金属性强弱的判断依据:
①;
①;
②;
②;
③。
③。
随着元素核电荷数的递增,元素的金属性和非金属性呈现 变化。
3-9、11-17号元素的金属性逐渐 ,非金属性逐渐 。
例4:
下列气态氢化物中,最稳定的是 ()
A、PH3 B、H2S C、SiH4 D、HCl
例5:
下列叙述中,肯定A金属比B金属活泼性强的是()
A、A原子的最外层电子数比B原子的最外层电子数少
B、A原子电子层数比B原子的电子层数多
C、1molA从酸中置换H+生成的H2比1molB从酸中置换H+生成的H2多
D、常温时,A能从水中置换出氢气,而B不能
五、元素周期律
随着元素的递增,元素的(除稀有气体元素外)、元素的性和性、元素的(最高化合价与最低化合价)都呈现周期性变化。
元素的性质随着元素 的递增而呈周期性变化的规律叫做元素周期律。
元素周期律是元素原子 发生周期性变化的必然结果。
例题6:
元素性质呈现周期性变化的本质原因是()