襄阳市中考化学三模试题及答案Word文档下载推荐.docx
《襄阳市中考化学三模试题及答案Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《襄阳市中考化学三模试题及答案Word文档下载推荐.docx(27页珍藏版)》请在冰豆网上搜索。
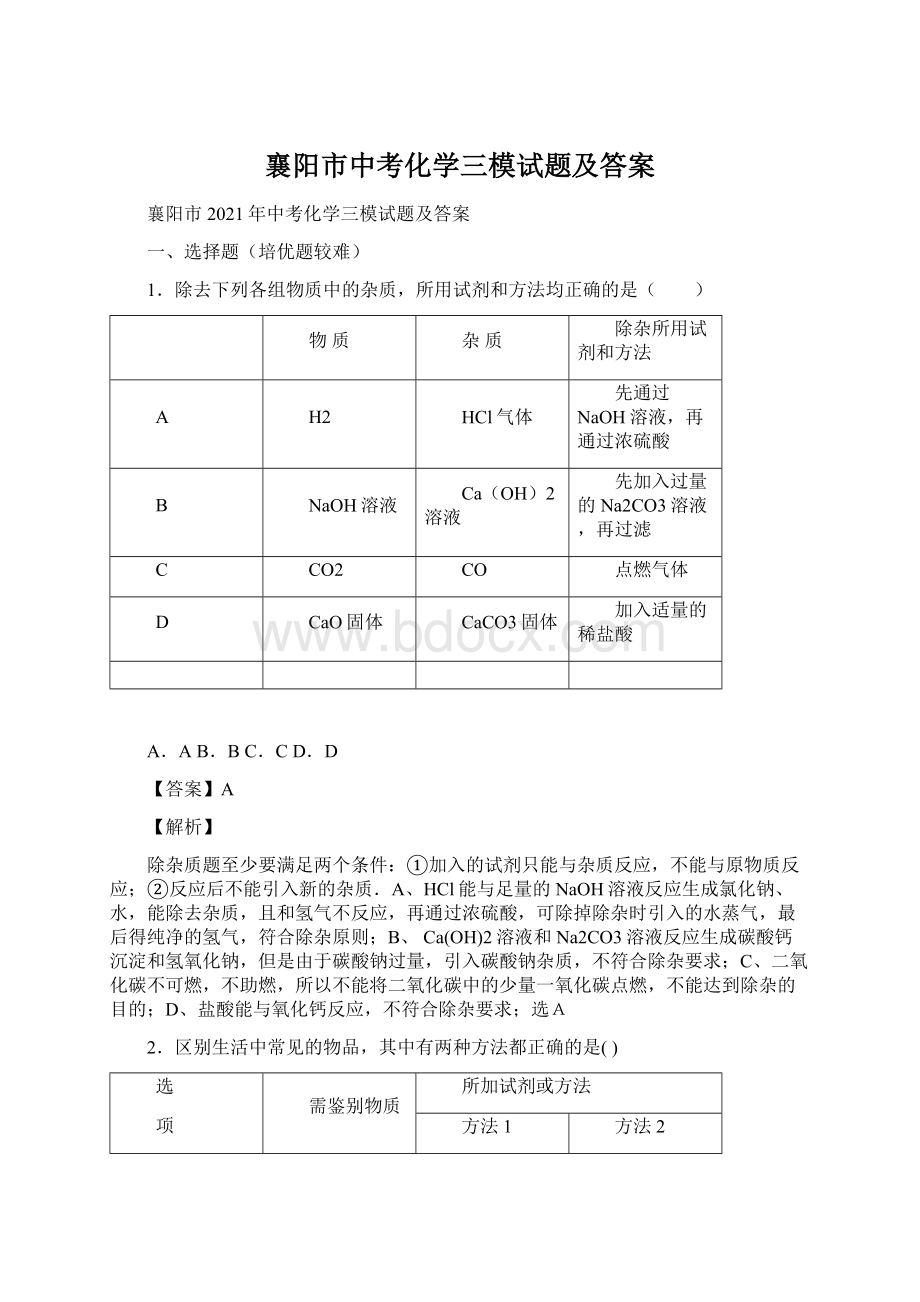
点燃气体
D
CaO固体
CaCO3固体
加入适量的稀盐酸
A.AB.BC.CD.D
【答案】A
【解析】
除杂质题至少要满足两个条件:
①加入的试剂只能与杂质反应,不能与原物质反应;
②反应后不能引入新的杂质.A、HCl能与足量的NaOH溶液反应生成氯化钠、水,能除去杂质,且和氢气不反应,再通过浓硫酸,可除掉除杂时引入的水蒸气,最后得纯净的氢气,符合除杂原则;
B、Ca(OH)2溶液和Na2CO3溶液反应生成碳酸钙沉淀和氢氧化钠,但是由于碳酸钠过量,引入碳酸钠杂质,不符合除杂要求;
C、二氧化碳不可燃,不助燃,所以不能将二氧化碳中的少量一氧化碳点燃,不能达到除杂的目的;
D、盐酸能与氧化钙反应,不符合除杂要求;
选A
2.区别生活中常见的物品,其中有两种方法都正确的是()
选
项
需鉴别物质
所加试剂或方法
方法1
方法2
厕所清洁剂与厨房洗涤剂
加入石灰石
加水看是否放热
NH4NO3氮肥和K2SO4钾肥
加Ca(OH)2研磨并闻气味
加水触摸烧杯
苏打和小苏打
加水,观察能否溶解
加入稀HCl
羊毛织品和尼龙织品
触摸纺织品
抽丝灼烧观察
【答案】B
A、厕所清洁剂显酸性,能与石灰石的主要成分碳酸钙反应生成二氧化碳,产生冒气泡的现象;
厨房洗涤剂显碱性,与石灰石不反应;
两种物质溶于水都无明显的放热现象;
B、NH4NO3氮肥和K2SO4钾肥,加Ca(OH)2研磨,硝酸铵会生成氨气,能闻到刺激性气味,硫酸钾不能;
硝酸铵溶于水,溶液温度降低,硫酸钾无明显现象;
C、苏打是碳酸钠和小苏打是碳酸氢钠,加水,都能溶解;
加入稀HCl都能生成二氧化碳气体;
D羊毛织品和尼龙织品,触摸纺织品无明显差异,抽丝灼烧,羊毛会有烧焦羽毛的气味。
选B
点睛:
鉴别题要做到同一操作下或与同一物质反应时,现象要不同。
3.在AlCl3溶液中逐滴加入NaOH溶液至过量,发生如下反应:
3NaOH+AlCl3=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O。
已知NaAlO2易溶于水,则下列图像不正确的是()
A.B.C.D.
【分析】
【详解】
A、图中所示,随着氢氧化钠溶液的滴加,溶液中水的质量逐渐增大,当加入一定量时会出现滴加氢氧化钠溶液,而水的质量不增加的阶段而后继续增加;
而反应的事实却是溶液中水会随着氢氧化钠溶液的滴加而不断增加,选项A错误;
B、图中所示,随着氢氧化钠的滴加,溶液中的氯化铝不断形成氢氧化铝沉淀,沉淀质量逐渐增加。
至完全反应后,随着氢氧化钠的滴加沉淀逐渐减少。
符合氯化铝先与氢氧化钠生成氢氧化铝沉淀,然后沉淀氢氧化铝又和滴加的氢氧化钠生成可溶的NaAlO2的反应事实,选项B正确;
C、图中所示,溶液的pH逐渐变大,符合氯化铝先与氢氧化钠生成氢氧化铝沉淀,溶液渐呈中性,然后沉淀氢氧化铝又和滴加的氢氧化钠生成可溶的NaAlO2而使溶液逐渐呈碱性的反应事实,选项C正确;
D、图中所示,随着氢氧化钠溶液的滴加,溶液中铝元素质量减少至完全消失,之后随着氢氧化钠溶液滴加溶液中铝元素质量又逐渐增加,符合氯化铝先与氢氧化钠生成氢氧化铝沉淀,然后沉淀氢氧化铝又和滴加的氢氧化钠生成可溶的NaAlO2的反应事实,选项D正确。
故选A。
【点睛】
根据反应进程,分析反应对溶液组成的影响,结合图示该因素变化的曲线,判断曲线与反应事实是否相符。
4.向盛有一定质量MgO和MgCO3混合物的烧杯中加入142g稀盐酸,恰好完全反应,一定温度下,得到150g不饱和溶液。
下列数据中,与该溶液的溶质质量分数最接近的是
A.5.3%
B.5.6%
C.12.7%
D.13.4%
【答案】C
氧化镁和稀盐酸反应生成氯化镁和水,碳酸镁和稀盐酸反应生成氯化镁、水和二氧化碳;
可见生成的氯化镁相同时造成的溶液质量增加是相等的,与是氧化镁还是碳酸镁反应无关;
设生成的氯化镁的质量为x,则
解得x=19g;
该溶液的溶质质量分数为:
。
故选:
C。
差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解。
5.部分变质的烧碱样品18.6g,能与7.3%的稀盐酸200g恰好完全反应,则此样品中变质的烧碱与原烧碱的质量比为()
A.3:
2B.2:
3C.1:
2D.1:
1
氢氧化钠容易与空气中的二氧化碳反应生成碳酸钠,设此样品中生成碳酸钠的质量为x,与碳酸钠反应的盐酸的质量为m
x=106m/73
设未变质的氢氧化钠的质量为y
y=40(14.6g-m)/36.5
x+y=(106m/73)+40(14.6g-m)/36.5=18.6g,m=7.3g
x=10.6gy=8g
设变质的氢氧化钠的质量为z
z=8g
则此样品中变质的烧碱与原烧碱的质量比为:
8g:
(8g+8g)=1:
2。
故选C。
6.一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、硝酸钙、氯化铜、碳酸钠中的一种或几种。
为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取14.9g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钙、氯化铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
【答案】D
A、氯化钾、氯化钠和硝酸银反应的化学方程式及其质量关系为:
KCl+AgNO3═AgCl↓+KNO3,
74.5
143.5
14.9g
28.7g
NaCl+AgNO3═AgCl↓+NaNO3,
58.5
11.7g
取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成,是因为碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠,因此杂质中含有碳酸钠,由计算可知,14.9g氯化钾和硝酸银反应生成28.7g氯化银,11.7g氯化钠和硝酸银反应生成28.7g氯化银,杂质中含有碳酸钠,氯化钾质量小于14.9g,和硝酸银反应生成氯化银质量小于28.7g,因此杂质中一定含有氯化钠,错误;
B、取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成,是因为碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠,因此杂质中含有碳酸钠,则杂质中不含有硝酸钙,加蒸馏水,充分搅拌,得无色澄清溶液,说明杂质中不含有氯化铜,错误;
C、由A知,杂质中肯定含有碳酸钠、氯化钠,错误;
D、杂质中肯定含有氯化钠、碳酸钠,由于硝酸钾是否存在不影响实验结果,因此可能含有硝酸钾,也可能不含有硝酸钾,正确。
故选D。
7.下列图像不能正确反映其对应变化关系的是
ABCD
A.用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
B.一定质量的红磷在密闭容器中燃烧
C.向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
D.向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液
试题分析:
A选项用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气能正确反应对应关系;
B选项一定质量的红磷在密闭容器中燃烧,根据质量守恒定律可知能正确反应对应关系;
C选项向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉不能说明对应关系,因为没有具体说明金属的量;
D选项向一定质量的氯化铜和稀盐酸的混合溶液中逐滴加入氢氧化钠溶液能正确反应对应关系,酸碱盐反应时先发生酸碱中和,然后碱盐反应产生沉淀,故答案选择C
考点:
酸碱盐、金属的性质、催化剂
8.将铝和镁组成的混合物10g加入到200g稀盐酸中恰好完全反应后得到溶液209g,再向溶液中加入足量的氢氧化钠溶液,最终生成沉淀的质量为( )
A.12gB.14.25gC.17.25gD.27g
铝和稀盐酸反应生成氯化铝和氢气,镁和稀盐酸反应生成氯化镁和氢气,氯化铝和氢氧化钠反应生成氢氧化铝和氯化钠,氯化镁和氢氧化钠反应生成氢氧化镁和氯化钠。
铝和镁组成的混合物10g加入到200g稀盐酸中恰好完全反应后得到溶液209g,则生成氢气的质量为
设参加反应的铝的质量为x,生成氢气的质量为y
由和得,,
生成氢氧化铝的质量为,生成氢氧化镁的质量为,最终生成沉淀的质量为
9.图中“→”表示甲在一定条件下可以转化成乙,“—”表示相连的物质在一定条件下可以发生反应,甲、乙、丙、丁分别表示一氧化碳、碳、氧气、二氧化碳中的某一物质,下列说法正确的是
A.甲一定是一氧化碳B.乙一定不是二氧化碳
C.丙可能是碳或氧气D.丁可能是碳或二氧化碳
根据各组内四种物质的性质及变化规律,利用物质间发生反应需要满足的条件,判断物质间反应与转化关系图中所示的物质间关系相符合的选项;
丙与丁均能和其它的两种物质反应,所以可判断它们是氧气与碳,推断结论是否正确可采用依据选项分析判断转化是否完成即可得到答案。
A、甲是一氧化碳时则乙是二氧化碳,丙是氧气,丁是碳,符合该转化过程;
但当甲是二氧化碳,乙是一氧化碳,丁是氧气,丙是碳时,该转化也能完成,故该说法错误;
B、当乙是二氧化碳时,丁是碳,丙是氧气,甲是一氧化碳该转化也能完成,故说法错误;
C、当丙是碳时,乙是一氧化碳,丁是氧气,甲是二氧化碳可完成该转化;
丙是氧气时,乙是二氧化碳,丁是一氧化碳,甲是碳可完成该转化,故选项说法正确;
D、当丁是二氧化碳时,二氧化碳无法与其它的两种物质反应,该转化无法完成,故该选项说法错误。
10.将乙酸(CH3COOH)和葡萄糖(C6H12O6)溶于水得到混合溶液,测得溶液中氢元素的质量分数为a,则溶液中碳元素的质量分数为( )
A.1﹣9aB.1﹣8aC.12aD.8a
根据乙酸(CH3COOH)、葡萄糖(C6H12O6)、水中,氢原子和氧原子的个数比均为2:
1,进行分析解答。
乙酸(CH3COOH)、葡萄糖(C6H12O6)、水中,氢原子和氧原子的个数比均为2:
1,则将乙酸(CH3COOH)和葡萄糖(C6H12O6)溶于水得到混合溶液中氢元素和氧元素的质量比为(1×
2):
(16×
1)=1:
8;
测得溶液中氢元素的质量分数为a,氧元素的质量分数为8a,则溶液中碳元素的质量分数为1−a−8a=1−9a。
11.某铁粉样品中可能混有C粉、CuO粉末中的一种或两种。
将该样品加入到一定量的稀硫酸中,充分反应后过滤,再向滤液中加入铁粉,铁粉表面只有气泡产生;
将滤渣在氧气中充分灼烧,产生能使澄清石灰水变浑浊的气体,并