海南省海口十四中学年九年级上学期期中化学试题Word文档格式.docx
《海南省海口十四中学年九年级上学期期中化学试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《海南省海口十四中学年九年级上学期期中化学试题Word文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
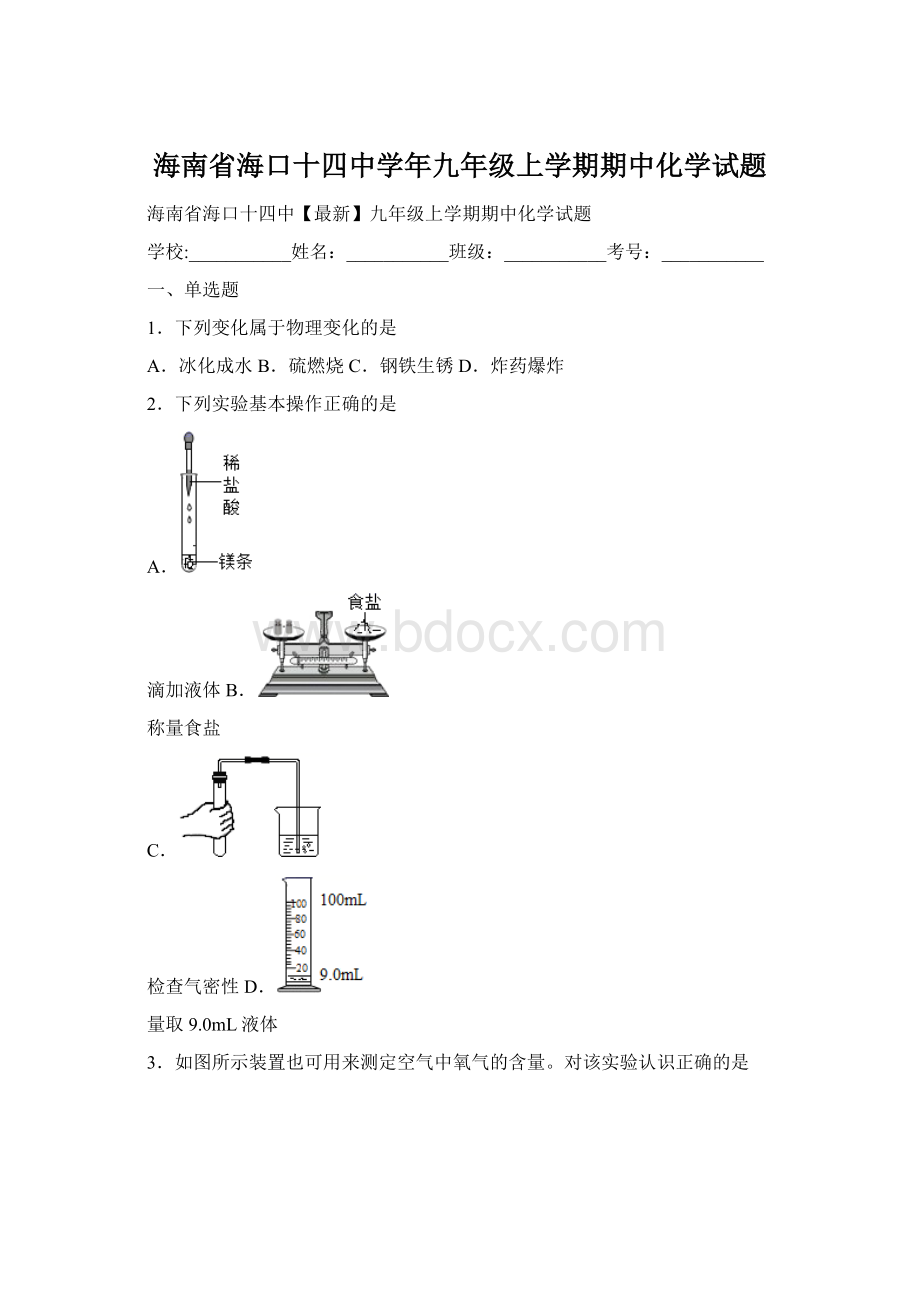
D.本实验还可以证明空气含有CO2和稀有气体
4.下列化学符号正确的是
A.1个一氧化碳分子:
CoB.2个硫酸根离子:
2SO42-
C.3个钠离子:
Na3+D.4个氢原子:
H4
5.如图是钙元素在元素周期表中的信息,从中获取的信息错误的是
A.该元素的原子序数为20
B.该元素属于非金属元素
C.该元素的原子核外有20个电子
D.该元素的相对原子质量为40.08
6.卟啉铁(C34H32ClFeN4O4)对人体缺铁性贫血有显著疗效。
以下说法正确的是( )
A.卟啉铁中含有5种元素
B.“缺铁性贫血”中的“铁”指单质铁
C.人体补铁的唯一方法是服用卟啉铁
D.1个卟啉铁分子中含有34个碳原子
7.在课堂上老师演示额如图所示实验,容器A中溶液变红,B中溶液不变色,该现象说明( )
A.分子可以再分
B.分子在不断地运动
C.分子由原子构成
D.分子是保持物质化学性质的最小粒子
8.据报道,俄罗斯科学家最近合成了一种新的原子,经测定该原子的核电荷数为114,相对原子质量为289,其中电子数为
A.175B.289C.61D.114
9.如图是表示物质分子的示意图,图中“●”和“○”分别表示两种含有不同质子数的原子,则图中表示单质的是( )
B.
C.
D.
10.某温泉的水质为硬水,下列说法正确的是
A.硬水放一段时间就变成软水B.凡是含有杂质的水就是硬水
C.硬水是一种纯净物D.硬水中含较多的可溶性钙和镁的化合物
11.下列粒子在人体中起着重要的作用,其中属于阴离子的是( )
D.
12.下列各种物质中,由离子构成的是
A.SB.NO2C.NaClD.CO2
13.在10-9m~10-10m范围内,对分子、原子进行操纵的纳米技术往往能实现意想不到的变化。
如纳米铜粉、纳米铁粉等一遇到空气,不必点燃就会急剧燃烧,甚至发生爆炸。
下列关于纳米铜粉的说法不正确的是
A.纳米铜属于金属单质
B.纳米铜比普通铜的化学性质更活泼
C.保存纳米铜时应该隔绝空气
D.纳米铜与普通铜所含元素不同
14.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是
A.KClB.KClOC.Cl2D.CCl4
二、填空题
15.用元素符号或化学式等化学符号填空:
①铁_____________;
②氢分子_____________;
③二氧化锰___________;
④3个氢氧根离子______________;
⑤H2O氧元素显-2价_____________
16.空气中含量最多的物质是__________,地壳中含量最多的元素是__________。
17.科学研究发现,用氯气作自来水消毒剂易产生致癌物。
新型高效安全的杀菌剂二氧化氯已经研制成功。
二氧化氯的化学式是______________,其中氯元素的化合价是_______。
18.如图表示电解水实验,a管中产生20mL的气体时,b管中同时产生气体_______mL。
电解水的实验说明水是由____________元素组成,每个水分子是由________________构成。
19.下表是部分元素的原子结构示意图、主要化合价等信息,请完成以下填空
(1)铝原子的最外层电子数是_______。
(2)原子序数为8和15的元素组成化合物的化学式_______。
三、简答题
20.某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
(1)图中还缺少的一种仪器是___________。
(2)过滤后观察发现,滤液仍然浑浊。
可能的原因之一_________。
21.请观察如右标志徽记:
你认为它是什么徽记?
请提出你在生活中两条节约用水的行为或措施。
22.国际卫生组织把苯定为强烈致癌物质。
苯是一种没有颜色带有特殊气味的液体,密度比水小,不溶于水,在一定条件下,苯分别能跟氢气、溴、浓硝酸、浓硫酸等物质发生化学反应。
请写出苯的性质:
(1)物理性质:
(2)化学性质:
四、实验题
23.现有下列A、B、C、D、E五种实验装置,根据题意,完成下列填空。
(1)指出仪器a的名称:
a_____________。
(2)用高锰酸钾制取并收集氧气,气体发生装置可选用:
__________(填序号,下同)。
(3)写出该反应的文字表达式______________________________;
若要收集较为纯净的氧气最好选用________装置。
五、计算题
24.硝酸铵(NH4NO3)是农村常用的一种化肥,因其含氮量较高而深受农民的喜爱,其市场价为810元/吨,请计算{其中
(2)至(5)要写出计算过程}:
(1)硝酸铵(NH4NO3)是由____种元素组成;
(2)硝酸铵(NH4NO3)的相对分子质量_______;
(3)硝酸铵(NH4NO3)中各元素的质量比_______;
(4)硝酸铵(NH4NO3)中氮元素的质量分数;
(5)现用1000元买硝酸铵,请问所购买到的化肥中含氮元素的质量是多少吨?
(精确至0.01吨)
参考答案
1.A
【解析】
【分析】
物理变化是没有生成其他物质的变化,而化学变化生成了其他的物质。
化学变化的基本特征是有其他物质生成,这是判断化学变化的依据。
【详解】
A、冰化成水,只是水的状态发生变化,无新物质生成是物理变化,符合题意;
B、硫燃烧生成二氧化硫,有新物质生成,属于化学变化,不符合题意;
C、钢铁生锈,铁与空气中的氧气和水分发生反应生成铁锈,有新物质生成,属于化学变化,不符合题意;
D、炸药爆炸有二氧化硫等物质生成,属于化学变化,不符合题意。
故选:
A。
2.C
滴加液体时滴管不能深入试管内,要悬空滴加,所以A错误;
称量物质的时候要按照左物右码的原则,所以B错误;
量取9.0mL液体应该选择10mL的量筒,不能用100mL的。
故选C。
考点:
实验操作及其仪器的选择
3.A
A、选用红磷是因为反应可以耗尽氧气,生成固态的五氧化二磷,选项A正确;
B、如果把红磷换成硫或木炭,硫或木炭燃烧生成的二氧化硫气体或二氧化碳气体会占据氧气的空间,导致水不能进入集气瓶,从而导致不能测定空气中氧气的含量,选项B不正确;
C、集气瓶中的氧气的量是一定的,反应需要的红磷的量也是一定的,最终进入集气瓶中的水也是一定的,并不是燃烧匙中的红磷越多,水位上升越高,选项C不正确;
D、本实验可以测定空气中氧气的含量,但是不能证明空气中含有氮气、二氧化碳和稀有气体等,选项D不正确。
故选A。
4.B
A、一氧化碳的化学式为CO,两个字母都大写,Co表示钴元素,选项A错误;
B、表示多个离子,就在其离子符号前加上相应的数字,故2个硫酸根离子表示为2SO42-,选项B正确;
C、钠离子带一个单位的正电荷,表示离子个数的数字标在离子符号的前面,3个钠离子表示为:
3Na
+,选项C错误;
D、原子的表示方法就是在其元素符号前加上相应的数字,4个氢原子表示为4H,选项D错误。
故选B。
5.B
试题分析:
从图示看:
该元素的原子序数为20;
该元素属于金属元素;
该元素的原子核外有20个电子;
该元素的相对原子质量为40.08。
故选B.
元素周期表
6.D
A、由卟啉铁的化学式可知,卟啉铁是由碳、氢、氯、铁、氮、氧六种元素组成的,故A不正确;
B、“缺铁性贫血”中的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关,故B不正确;
C、人体补铁的方法很多,不只是服用卟啉铁,如使用铁锅等,故C不正确;
D、1个卟啉铁分子中含有34个碳原子,故D正确。
故选D。
7.B
浓氨水具有挥发性,挥发出来的氨气分子不断运动,扩散到容器A中,氨气溶于水呈碱性,能使酚酞试液变红,因此容器A中溶液变红,该现象说明氨气分子不断运动,符合题意。
8.D
在原子内部,核电荷数等于质子数等于核外电子数,故该原子的电子数为114。
故本题选D。
9.A
A、示意图中只有两个相同原子构成的分子,因此图中表示的物质为单质,符合题意;
B、示意图中有两种不同的原子构成的分子,因此图中表示的为混合物,不符合题意;
C、示意图中表示两种不同的原子构成的分子,因此图中表示的物质为化合物,不符合题意;
D、示意图中表示两种不同的原子构成的分子,因此图中表示的物质为化合物,不符合题意。
10.D
硬水是指含有很多可溶性的杂质的水;
硬水一般通过煮沸措施才能软化;
所以硬水属于混合物。
故选D.
水的净化
11.C
A、质子数和核外电子数都为8,为原子,错误;
B、质子数为12,核外电子数为12,质子数=核外电子数,为原子,错误;
C、质子数为17,核外电子数为18,质子数<核外电子数,为阴离子,正确;
D、质子数为11,核外电子数都为10,为阳离子,错误;
12.C
A、S属于固态非金属单质,是由硫原子直接构成的,选项A错误;
B、二氧化氮是由非金属元素组成的化合物,是由二氧化氮分子构成的,选项B错误;
C、氯化钠是由钠离子和氯离子构成的,选项C正确;
D、二氧化碳是由二氧化碳分子构成的,选项D错误。
【点睛】
金属、大多数固态非金属单质、稀有气体等由原子构成;
有些物质是由分子构成的,气态的非金属单质和一般由非金属元素组成的化合物,如氢气、水等;
有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠。
13.D
纳米铜粉属于金属单质;
纳米铜比普通铜的化学性质更活泼;
保存纳米铜时应该隔绝空气,防止氧化;
纳米铜与普通铜所含元素相同。
基本概念和原理
14.C
根据在化合物中正负化合价代数和为零,可知:
HCl中Cl的化合价为:
(+1)+a=0,则a=-1,
HClO中Cl的化合价为:
(+1)+b+(-2)=0,则b=+1,
KClO3中Cl的化合价为:
(+1)+c+(-2)×
3=0,则c=+5,
选项中氯元素的化合价为:
NaCl中Cl的化合价为:
(+1)+e=0,则e=-1;
KClO中Cl的化合价为:
(+1)+f+(-2)=0,则f=+1;
单质中元素的化合价为零,因此Cl2中Cl的化合价为0;
CCl4中Cl的化合价为:
+4+g×
4=0,则g=-1;
在HCl、X、HClO、KClO3中,氯元素化合价由低至高的排列顺序,由计算可知X代表的是Cl2,故选C。
15.FeH2MnO23OH-
①铁元素符号为Fe;
故填:
Fe;
②化学式的意义之一是表示这种物质的一个分子,则氢分子可用化学式H2表示,故填:
H2。
③二氧化锰