高效液相色谱教程文档格式.docx
《高效液相色谱教程文档格式.docx》由会员分享,可在线阅读,更多相关《高效液相色谱教程文档格式.docx(24页珍藏版)》请在冰豆网上搜索。
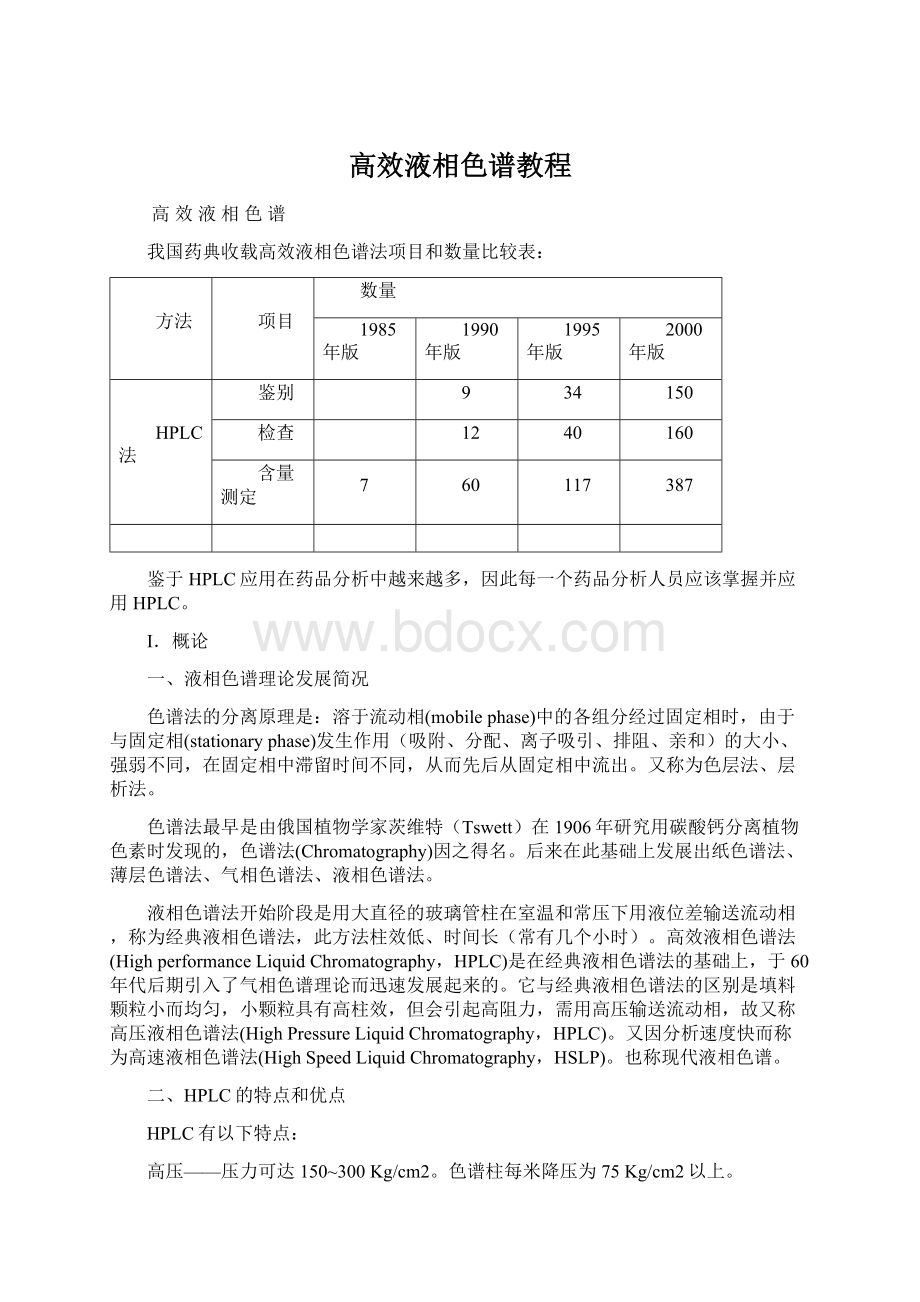
160
含量测定
7
60
117
387
鉴于HPLC应用在药品分析中越来越多,因此每一个药品分析人员应该掌握并应用HPLC。
I.概论
一、液相色谱理论发展简况
色谱法的分离原理是:
溶于流动相(mobilephase)中的各组分经过固定相时,由于与固定相(stationaryphase)发生作用(吸附、分配、离子吸引、排阻、亲和)的大小、强弱不同,在固定相中滞留时间不同,从而先后从固定相中流出。
又称为色层法、层析法。
色谱法最早是由俄国植物学家茨维特(Tswett)在1906年研究用碳酸钙分离植物色素时发现的,色谱法(Chromatography)因之得名。
后来在此基础上发展出纸色谱法、薄层色谱法、气相色谱法、液相色谱法。
液相色谱法开始阶段是用大直径的玻璃管柱在室温和常压下用液位差输送流动相,称为经典液相色谱法,此方法柱效低、时间长(常有几个小时)。
高效液相色谱法(HighperformanceLiquidChromatography,HPLC)是在经典液相色谱法的基础上,于60年代后期引入了气相色谱理论而迅速发展起来的。
它与经典液相色谱法的区别是填料颗粒小而均匀,小颗粒具有高柱效,但会引起高阻力,需用高压输送流动相,故又称高压液相色谱法(HighPressureLiquidChromatography,HPLC)。
又因分析速度快而称为高速液相色谱法(HighSpeedLiquidChromatography,HSLP)。
也称现代液相色谱。
二、HPLC的特点和优点
HPLC有以下特点:
高压——压力可达150~300Kg/cm2。
色谱柱每米降压为75Kg/cm2以上。
高速——流速为0.1~10.0ml/min。
高效——可达5000塔板每米。
在一根柱中同时分离成份可达100种。
高灵敏度——紫外检测器灵敏度可达0.01ng。
同时消耗样品少。
HPLC与经典液相色谱相比有以下优点:
速度快——通常分析一个样品在15~30min,有些样品甚至在5min内即可完成。
分辨率高——可选择固定相和流动相以达到最佳分离效果。
灵敏度高——紫外检测器可达0.01ng,荧光和电化学检测器可达0.1pg。
柱子可反复使用——用一根色谱柱可分离不同的化合物。
样品量少,容易回收——样品经过色谱柱后不被破坏,可以收集单一组分或做制备。
三、色谱法分类
按两相的物理状态可分为:
气相色谱法(GC)和液相色谱法(LC)。
气相色谱法适用于分离挥发性化合物。
GC根据固定相不同又可分为气固色谱法(GSC)和气液色谱法(GLC),其中以GLC应用最广。
液相色谱法适用于分离低挥发性或非挥发性、热稳定性差的物质。
LC同样可分为液固色谱法(LSC)和液液色谱法(LLC)。
此外还有超临界流体色谱法(SFC),它以超临界流体(界于气体和液体之间的一种物相)为流动相(常用CO2),因其扩散系数大,能很快达到平衡,故分析时间短,特别适用于手性化合物的拆分。
按原理分为吸附色谱法(AC)、分配色谱法(DC)、离子交换色谱法(IEC)、排阻色谱法(EC,又称分子筛、凝胶过滤(GFC)、凝胶渗透色谱法(GPC)和亲和色谱法。
(此外还有电泳。
)
按操作形式可分为纸色谱法(PC)、薄层色谱法(TLC)、柱色谱法。
四、色谱分离原理
高效液相色谱法按分离机制的不同分为液固吸附色谱法、液液分配色谱法(正相与反相)、离子交换色谱法、离子对色谱法及分子排阻色谱法。
1.液固色谱法 使用固体吸附剂,被分离组分在色谱柱上分离原理是根据固定相对组分吸附力大小不同而分离。
分离过程是一个吸附-解吸附的平衡过程。
常用的吸附剂为硅胶或氧化铝,粒度5~10μm。
适用于分离分子量200~1000的组分,大多数用于非离子型化合物,离子型化合物易产生拖尾。
常用于分离同分异构体。
2.液液色谱法 使用将特定的液态物质涂于担体表面,或化学键合于担体表面而形成的固定相,分离原理是根据被分离的组分在流动相和固定相中溶解度不同而分离。
分离过程是一个分配平衡过程。
涂布式固定相应具有良好的惰性;
流动相必须预先用固定相饱和,以减少固定相从担体表面流失;
温度的变化和不同批号流动相的区别常引起柱子的变化;
另外在流动相中存在的固定相也使样品的分离和收集复杂化。
由于涂布式固定相很难避免固定液流失,现在已很少采用。
现在多采用的是化学键合固定相,如C18、C8、氨基柱、氰基柱和苯基柱。
液液色谱法按固定相和流动相的极性不同可分为正相色谱法(NPC)和反相色谱法(RPC)。
正相色谱法 采用极性固定相(如聚乙二醇、氨基与腈基键合相);
流动相为相对非极性的疏水性溶剂(烷烃类如正已烷、环已烷),常加入乙醇、异丙醇、四氢呋喃、三氯甲烷等以调节组分的保留时间。
常用于分离中等极性和极性较强的化合物(如酚类、胺类、羰基类及氨基酸类等)。
反相色谱法 一般用非极性固定相(如C18、C8);
流动相为水或缓冲液,常加入甲醇、乙腈、异丙醇、丙酮、四氢呋喃等与水互溶的有机溶剂以调节保留时间。
适用于分离非极性和极性较弱的化合物。
RPC在现代液相色谱中应用最为广泛,据统计,它占整个HPLC应用的80%左右。
随着柱填料的快速发展,反相色谱法的应用范围逐渐扩大,现已应用于某些无机样品或易解离样品的分析。
为控制样品在分析过程的解离,常用缓冲液控制流动相的pH值。
但需要注意的是,C18和C8使用的pH值通常为2.5~7.5(2~8),太高的pH值会使硅胶溶解,太低的pH值会使键合的烷基脱落。
有报告新商品柱可在pH1.5~10范围操作。
正相色谱法与反相色谱法比较表
正相色谱法
反相色谱法
固定相极性
高~中
中~低
流动相极性
低~中
中~高
组分洗脱次序
极性小先洗出
极性大先洗出
从上表可看出,当极性为中等时正相色谱法与反相色谱法没有明显的界线(如氨基键合固定相)。
二、塔板理论
1.塔板理论的基本假设
塔板理论是Martin和Synger首先提出的色谱热力学平衡理论。
它把色谱柱看作分馏塔,把组分在色谱柱内的分离过程看成在分馏塔中的分馏过程,即组分在塔板间隔内的分配平衡过程。
塔板理论的基本假设为:
1)色谱柱内存在许多塔板,组分在塔板间隔(即塔板高度)内完全服从分配定律,并很快达到分配平衡。
2)样品加在第0号塔板上,样品沿色谱柱轴方向的扩散可以忽略。
3)流动相在色谱柱内间歇式流动,每次进入一个塔板体积。
4)在所有塔板上分配系数相等,与组分的量无关。
虽然以上假设与实际色谱过程不符,如色谱过程是一个动态过程,很难达到分配平衡;
组分沿色谱柱轴方向的扩散是不可避免的。
但是塔板理论导出了色谱流出曲线方程,成功地解释了流出曲线的形状、浓度极大点的位置,能够评价色谱柱柱效。
2.色谱流出曲线方程及定量参数(峰高h和峰面积A)
根据塔板理论,流出曲线可用下述正态分布方程来描述:
C=e 或 C=e
由色谱流出曲线方程可知:
当t=tR时,浓度C有极大值,Cmax=。
Cmax就是色谱峰的峰高。
因此上式说明:
①当实验条件一定时(即σ一定),峰高h与组分的量C0(进样量)成正比,所以正常峰的峰高可用于定量分析。
②当进样量一定时,σ越小(柱效越高),峰高越高,因此提高柱效能提高HPLC分析的灵敏度。
由流出曲线方程对V(0~∞)求积分,即得出色谱峰面积A=×
σ×
Cmax=C0。
可见A相当于组分进样量C0,因此是常用的定量参数。
把Cmax=h和Wh/2=2.355σ代入上式,即得A=1.064×
Wh/2×
h,此为正常峰的峰面积计算公式。
三、速率理论(又称随机模型理论)
1.液相色谱速率方程
1956年荷兰学者VanDeemter等人吸收了塔板理论的概念,并把影响塔板高度的动力学因素结合起来,提出了色谱过程的动力学理论——速率理论。
它把色谱过程看作一个动态非平衡过程,研究过程中的动力学因素对峰展宽(即柱效)的影响。
后来Giddings和Snyder等人在VanDeemter方程(H=A+B/u+Cu,后称气相色谱速率方程)的基础上,根据液体与气体的性质差异,提出了液相色谱速率方程(即Giddings方程):
H=2λdp++\s\up5(2p+\s\up5(2p+\s\up5(2f
2.影响柱效的因素
1)涡流扩散(eddydiffusion)。
由于色谱柱内填充剂的几何结构不同,分子在色谱柱中的流速不同而引起的峰展宽。
涡流扩散项A=2λdp,dp为填料直径,λ为填充不规则因子,填充越不均匀λ越大。
HPLC常用填料粒度一般为3~10μm,最好3~5μm,粒度分布RSD≤5%。
但粒度太小难于填充均匀(λ大),且会使柱压过高。
大而均匀(球形或近球形)的颗粒容易填充规则均匀,λ越小。
总的说来,应采用细而均匀的载体,这样有助于提高柱效。
毛细管无填料,A=0。
2)分子扩散(moleculardiffusion)。
又称纵向扩散。
由于进样后溶质分子在柱内存在浓度梯度,导致轴向扩散而引起的峰展宽。
分子扩散项B/u=2γDm/u。
u为流动相线速度,分子在柱内的滞留时间越长(u小),展宽越严重。
在低流速时,它对峰形的影响较大。
Dm为分子在流动相中的扩散系数,由于液相的Dm很小,通常仅为气相的10-4~10-5,因此在HPLC中,只要流速不太低的话,这一项可以忽略不计。
γ是考虑到填料的存在使溶质分子不能自由地轴向扩散,而引入的柱参数,用以对Dm进行校正。
γ一般在0.6~0.7左右,毛细管柱的γ=1。
3)传质阻抗(masstransferresistance)。
由于溶质分子在流动相、静态流动相和固定相中的传质过程而导致的峰展宽。
溶质分子在流动相和固定相中的扩散、分配、转移的过程并不是瞬间达到平衡,实际传质速度是有限的,这一时间上的滞后使色谱柱总是在非平衡状态下工作,从而产生峰展宽。
液相色谱的传质阻抗项Cu又分为三项。
①流动相传质阻抗Hm=Cmd2pu/Dm,Cm为常数。
这是由于在一个流路中流路中心和边缘的流速不等所致。
靠近填充颗粒的流动相流速较慢,而中心较快,处于中心的分子还未来得及与固定相达到分配平衡就随流动相前移,因而产生峰展宽。
②静态流动相传质阻抗Hsm=Csmd2pu/Dm,Csm为常数。
这是由于溶质分子进入处于固定相孔穴内的静止流动相中,晚回到流路中而引起峰展宽。
Hsm对峰展宽的影响在整个传质过程中起着主要作用。
固定相的颗粒越小,微孔孔径越大,传质阻力就越小,传质速率越高。
所以改进固定相结构,减小静态流动相传质阻力,是提高液相色谱柱效的关键。
Hm和Hsm都与固定相的粒径平方d2p成正比,与扩散系数Dm成反比。
因此应采用低粒度固定相和低粘度流动相。
高柱温可以增大Dm,但用有机溶剂作流动相时,易产生气泡,因此一般采用室温。
③固定相传质阻抗Hs=Csd2fu/Ds(液液分配色谱),Cs为常数,df为固定液的液膜厚度,Ds为分子在固定液中的扩散系数。
在分配色谱中Hs与df的平方成正比,在吸附色谱中Hs与吸附和解吸速度成反比。
因此只有在厚涂层固定液、深孔离子交换树脂或解吸速度慢的吸附色谱中,Hs才有明显影响。
采用单分子层的化学键合固定相时Hs可以忽略。
从速率方程式可以看出,要获得高效能的色谱分析,一般可采用以下措施:
①进样时间要短。
②填料粒度要小。
③改善传质过程。
过高的吸附作用力可导致严重的峰展宽和拖尾,甚至不可逆吸附。
④适当的流速。
以H对u作图,则有一最佳线速度uopt,在此线速度时,H最小。
一般在液相色谱中,uopt很小(大约0.03~0.1mm/s),在