电化学专题电极反应方程式的书写.docx
《电化学专题电极反应方程式的书写.docx》由会员分享,可在线阅读,更多相关《电化学专题电极反应方程式的书写.docx(8页珍藏版)》请在冰豆网上搜索。
电化学专题电极反应方程式的书写
电化学专题—电极反应方程式的书写
一、原电池与电解池的判断
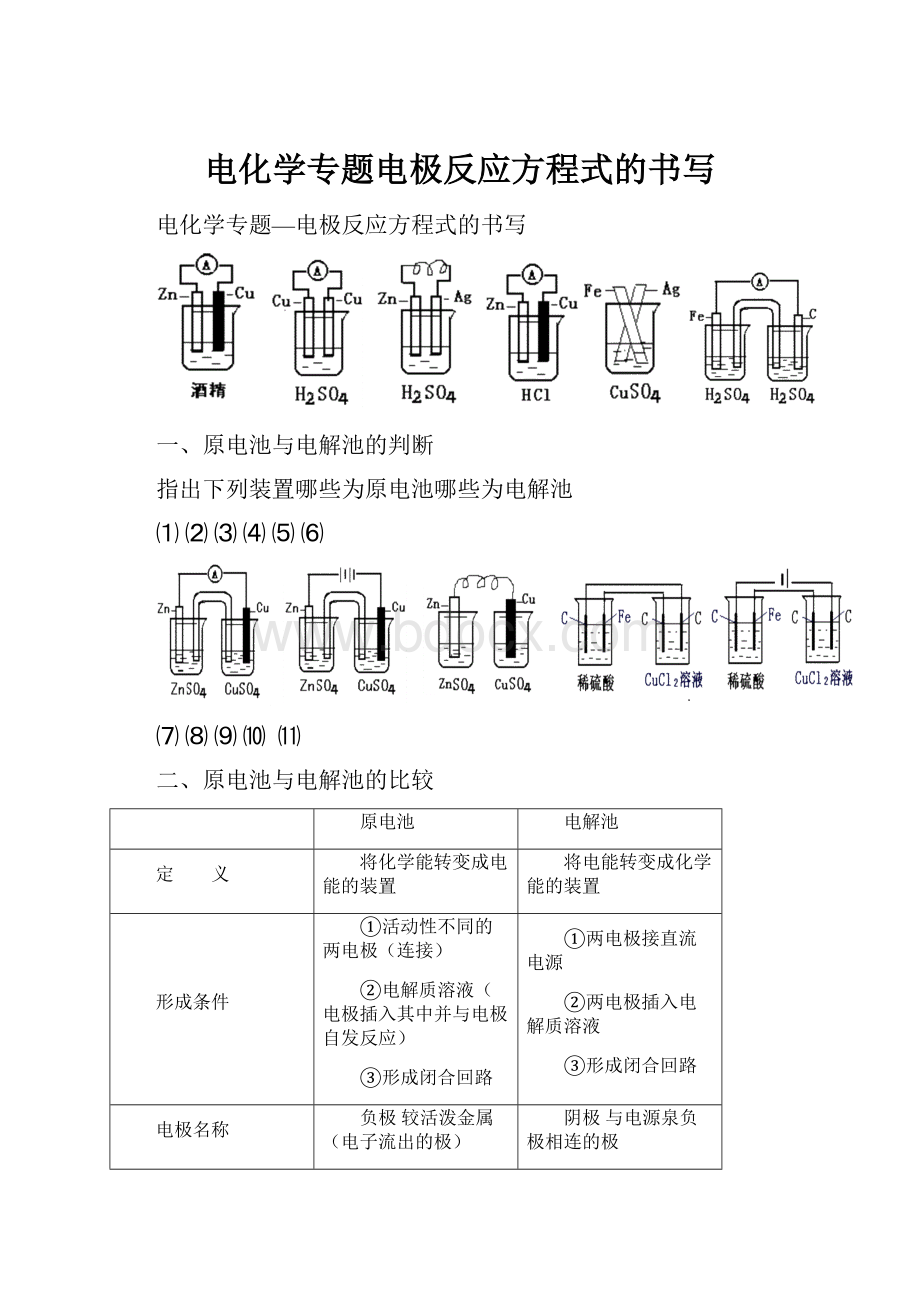
指出下列装置哪些为原电池哪些为电解池
⑴⑵⑶⑷⑸⑹
⑺⑻⑼⑽⑾
二、原电池与电解池的比较
原电池
电解池
定 义
将化学能转变成电能的装置
将电能转变成化学能的装置
形成条件
①活动性不同的两电极(连接)
②电解质溶液(电极插入其中并与电极自发反应)
③形成闭合回路
①两电极接直流电源
②两电极插入电解质溶液
③形成闭合回路
电极名称
负极较活泼金属(电子流出的极)
正极较不活泼金属或能导电的非金属(电子流入的极)
阴极与电源泉负极相连的极
阳极与电源正极相连的极
电极反应
负极氧化反应;金属或还原性气体失电子
正极还原反应;溶液中的阳离子得电子或者氧化性气体得电子(吸氧腐蚀)
阳极氧化反应;溶液中的阴离子失电子,或电极金属失电子
阴极还原反应;溶液中的阳离子得电子
电子流向
能量转变
化学能转变为电能
电能转化为化学能
装置特点
无外接直流电源
有外接直流电源
相似之处
均能发生氧化还原反应,且同一装置中两个电极在反应过程中转移电子总数相等。
举 例
⑴铜锌原电池;⑵氢氧燃烧电池
⑴氯碱工业装置;⑵电解精炼铜
三、原电池的电极反应和总反应式书写方法
1、仅有一电极材料参与反应方法:
规律:
参与反应的金属电极本身为负极,另一电极往往为正极,负极是参与反应的金属失电子,正极是介质溶液中的微粒得电子(反应一般为析氢、吸氧、析Cu、Ag等)
(1)酸性较强介质:
正极一般是析氢反应。
例:
图1电极反应:
负极:
Zn-2e=Zn2+正极:
2H++2e=H2↑
(2)接近中性介质:
正极一般是吸氧反应。
例:
图2电极反应:
负极:
2Fe-4e=2Fe2+正极:
O2+4e+2H2O=4OH-
练习1.我国首创的以铝—空气—海水电池为能源的新型海水标志灯,它以海水为电解质溶液,利用空气中的氧使铝不断氧化产生电流,写出这种电池的电极材料、电极反应式及总反应式。
答:
负极(Al):
4Al-12e-=4Al3+
正极(C):
3O2+12e-+6H2O=12OH-
总反应式:
4Al+6H2O+3O2=4Al(OH)3
分析:
负极本身参加反应被氧化,正极必须能导电而本身不参加反应。
电源负极材料为:
铝;电源正极材料为:
石墨等能导电的惰性材料。
负极反应为:
4Al-12e-=4Al3+;正极反应为:
3O2+6H2O+12e-=12OH-
(3)碱性介质:
正极一般也是吸氧反应。
例:
图3电极反应:
负极:
2Fe-4e=2Fe2+正极:
O2+4e+2H2O=4OH-
(4)含不活泼金属的盐溶液为介质:
正极析出不活泼金属(Cu、Ag等)。
例:
图4电极反应:
负极:
Fe-2e=Fe2+正极:
Cu2++2e=Cu
2、两电极材料均参与反应(常见于蓄电池式或纽扣式电池)
规律:
两电极材料通常由金属和金属化合物构成,金属作负极。
电子得失均由两电极本身发生。
在书写电极反应式时,应考虑电解质对电极的影响(如生成难溶物、弱电解质等)。
介质为酸性溶液时,反应式两边不能出现OH-离子;碱性溶液为介质时,反应式两边不能出现H+离子。
(1)酸性介质例:
实验室用铅蓄电池作电源电解饱和食盐水制氯气,已知铅蓄电池工作时总的方程式如下:
Pb+PbO2+2H2SO42PbSO4+2H2O试写出放电时的电极反应式。
分析得出:
负极:
Pb-2e+SO42-=PbSO4
正极:
PbO2+2e+SO42-+4H+=PbSO4+2H2O
(2)碱性介质例:
蓄电池在放电时起原电池作用,在充电时起电解池作用。
下式是爱迪生蓄电池分别在充电和放电时发生的反应:
Fe+NiO2+2H2OFe(OH)2+Ni(OH)2
试写出起原电池作用的电极反应式。
负极:
Fe-2e+2OH-=Fe(OH)2
正极:
NiO2+2e+2H2O=Ni(OH)2+2OH-
知识迁移:
蓄电池的充电过程即电解,充电时电极反应式书写,只要将放电时的电极反应式反过来写,然后将负极改为阴极、原来的正极改为阳极即可:
阴极:
Fe(OH)2+2e=Fe+2OH-
阳极:
Ni(OH)2+2OH—2e=NiO2+2H2O
练习2、电子表和电子计算器中常用一种微型纽扣原电池,它以锌为负极,氧化银为正极(即金属银上覆盖一薄层该金属氧化物),氢氧化钾溶液为电解质溶液,这种电池工作时,正极反应是()
AZn+2OH-=ZnO+H2O+2eBZnO+H2O=Zn+2OH--2e
CAg2O+2H+=2Ag+H2O-2eDAg2O+H2O=2Ag+2OH--2e
练习3、氢镍电池是近年来开发的可充电电池,具有质轻、容量大的优良特性,其性能远优于镍镉电池,对环境污染程度也小于镍镉电池。
目前已基本取代了镍镉电池。
氢镍电池的总反应式是H2+2NiO(OH)2Ni(OH)2。
下列叙述中正确的是(C、D)
A.电池放电时,电池负极周围溶液的OH不断增大B.电池放电时,镍元素被氧化
C.电池充电时。
氢元素被还原D.电池放电时,H2是负极
3、电极材料本身均不参与反应(常见于燃料电池)
规律:
两电极材料均为惰性电极(本身不参与反应,仅作导电的载体),负极是还原剂即燃料失电子,正极是氧化剂得电子。
在书写电极反应式时,应考虑电解质对电极反应的影响,介质为酸性溶液时,反应式两边不能出现OH-离子;碱性溶液为介质时,反应式两边不能出现H+离子。
同时参照总方程式中反应物和生成物来确定书写的微粒。
例1:
熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混和物作电解质,CO为阳极燃气,空气和CO2的混和气为阴极助燃气,制得在650℃下工作的燃料电池。
完成有关的电池反应式:
负极反应式:
2CO+2CO32--4e-→4CO2
正极反应式:
总反应式:
答:
正极:
O2+2CO2+4e-=2CO32-总反应式:
2CO+O2=2CO2
例2⑴美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,是一种高效低污染的新型电池,一般用金属铂(是一种惰性电极,并具有催化活性)或活性炭作电极,用40%的KOH溶液作电解质溶液。
氢氧燃料电池的突出优点是把化学能直接转化为电能,而不经过热能中间形式。
电极反应产生的水,经冷凝后又可作为宇航员的饮用水,发生的反应为:
2H2+O2====2H2O,则电极反应式分别为:
负极,正极。
⑵如把KOH改为稀H2SO4作导电物质,则电极反应式为、。
⑴和⑵的电池液不同,反应进行后,其溶液的pH各有何变化
⑶如把H2改为甲烷,KOH作导电物质,则电极反应式为、。
如果用稀H2SO4作导电物质,则电极反应式为、。
分析:
电解质溶液为碱性时,书写电极反应式可出现OH-,但不能出现H+;同样,电解质溶液为酸性时,书写电极反应式可出现H+,但不能出现OH-。
答案:
⑴负极:
2H2+4OH--4e-=4H2O,正极:
O2+2H2O+4e-=4OH-。
⑵负极:
2H2-4e-=4H+;正极:
O2+4H++4e-=2H2O。
⑶负极:
CH4+10OH--8e-=CO32-+7H2O;正极:
O2+2H2O+4e-=4OH-。
负极:
CH4+2H2O-8e-=CO2+8H+;正极:
O2+4H++4e-=2H2O。
点评:
解决此题的关键是理解原电池的有关概念,注意溶液环境(即酸性、碱性或中性),熟悉原电池电极反应式的一般书写方法。
练习4、将两铂片插入KOH溶液中作为电极,在两极区分别通入甲烷(或氢气、一氧化碳等可燃性气体)和氧气构成燃料电池,则通入甲烷气体的极是原电池的,该极的电极反应是,电池工作时的总反应的离子方程式是。
通入一氧化碳时的电极反应式:
负极:
,正极:
,
总反应的化学方程式:
。
原电池电极反应式书写的一般步骤第一步确定电极的正、负;第二步根据溶液中离子参加反应情况确定电极反应;第三步将电极反应相加得总反应式。
总结:
书写电极反应式是学习电化学的基本功,也是高考所必须掌握的知识点。
一般来讲,书写原电池的电极反应式应注意如下四点:
1、准确判断原电池的正负极
如果电池的正负极判断失误,则电极反应式必然写错,这是正确书写电极反应式的前提。
一般而言,较活泼的金属成为原电池的负极,但不是绝对的。
如将铜片和铝片同时插入浓硝酸中组成原电池时,铜却是原电池的负极被氧化,因为铝在浓硝酸中表面产生了钝化。
此时,其电极反应式为:
负极:
Cu-2e-=Cu2+正极:
2NO3-+4H++2e-==2NO2+2H2O
又如将镁铝合金放入6mol/L的NaOH溶液中构成原电池时,尽管镁比铝活泼,但镁不和NaOH溶液反应,所以铝成为负极,其电极反应式为:
负极:
2Al+8OH--6e-=2AlO2-+4H2O正极:
6H2O+6e-=3H2+6OH-
2、高度注意电解质的酸碱性
在正、负极上发生的电极反应不是孤立的,它往往与电解质溶液紧密联系。
如氢—氧燃料电池有酸式和碱式两种,在酸溶液中负极反应式为:
2H2-4e-=4H+正极反应式为:
O2+4H++4e-=2H2O;如是在碱溶液中,则不可能有H+出现,在酸溶液中,也不可能出现OH-。
又于CH4、CH3OH等燃料电池,在碱溶液中C元素以CO32-离子形式存在,而不是放出CO2。
3、牢牢抓住总的反应方程式
从理论上讲,任何一个自发的氧化还原反应均可设计成原电池。
而两个电极反应相加即得总的反应方程式。
所以,对于一个陌生的原电池,只要知道总反应方程式和其中的一个电极反应式,即可迅速写出另一个电极反应式。
4、不能忽视电子转移数相等
在同一个原电池中,负极失去的电子数必等于正极得到的电子数,所以在书写电极反应式时,要注意电荷守恒。
这样可以避免由电极反应式写总反应方程式,或由总反应方程式改写成电极反应式所带来的失误,同时,也可避免在有关计算中产生误差。
四、电解池的电极反应和总反应式书写方法
书写电解池的电极反应式时,要注意阴离子和阳离子的放电顺序:
阴极放电顺序Au3+>Ag+>Fe3+>Hg2+>Cu2+>H+>Pb2+>Sn2+>Ni2+>Fe2+>Zn2+>Mn2+>Al3+>Mg2+>Na+>Ca2+>K+
阳极放电顺序S2->I->Br->Cl->OH->NO3->F-
1.电解水型:
含氧酸、强碱、活泼金属的含氧酸盐(如NaOH、H2SO4、K2SO4等)的电解。
阴极:
阳极:
总反应:
2.分解电解质型:
无氧酸(除HF外)、不活泼的无氧酸盐(氟化物除外)(如HCl、CuCl2等)溶液的电解。
阴极:
阳极:
总反应:
3.放氢生碱型:
活泼金属的无氧酸盐(氟化物除外)(如NaCl、MgBr2)溶液的电解。
阴极:
阳极:
总反应:
4.放氧生酸型:
不活泼金属的含氧酸盐(如CuSO4、AgNO3等)溶液的电解。
阴极:
阳极:
总反应:
启示:
电极反应的书写与下列几个因素有关
1、与装置类型有关
2、与电极类型及电极材料有关
3、与反应类型有关
4、与电子守恒有关
5、与电解质环境有关
6、与总反应式有关
7、与题给信息有关
8、与离子的氧化还原性强弱有关